Adenosiinideaminaasi - Adenosine deaminase
| Adenosiini/AMP -deaminaasi | |||||||||
|---|---|---|---|---|---|---|---|---|---|
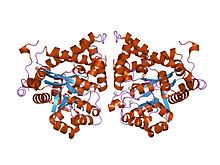 plasmodium yoelii -adenosiinideaminaasin kiderakenne (py02076)
| |||||||||
| Tunnisteet | |||||||||
| Symboli | A_deaminaasi | ||||||||
| Pfam | PF00962 | ||||||||
| Pfam klaani | CL0034 | ||||||||
| InterPro | IPR001365 | ||||||||
| PROSITE | PDOC00419 | ||||||||
| SCOP2 | 1Lisää / Scope / SUPFAM | ||||||||
| CDD | cd01320 | ||||||||
| |||||||||
| Adenosiinideaminaasi (editase) -domeeni | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Tunnisteet | |||||||||
| Symboli | A_deamin | ||||||||
| Pfam | PF02137 | ||||||||
| InterPro | IPR002466 | ||||||||
| PROSITE | PDOC00419 | ||||||||
| SCOP2 | 1Lisää / Scope / SUPFAM | ||||||||
| |||||||||
| Adenosiini/AMP-deaminaasi N-terminaali | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Tunnisteet | |||||||||
| Symboli | A_deaminase_N | ||||||||
| Pfam | PF08451 | ||||||||
| InterPro | IPR013659 | ||||||||
| |||||||||
Adenosiinideaminaasi (tunnetaan myös nimellä adenosiiniaminohydrolaasi tai ADA ) on entsyymi ( EC 3.5.4.4 ), joka osallistuu puriinin metaboliaan . Sitä tarvitaan adenosiinin hajoamiseen ruoasta ja nukleiinihappojen kiertoon kudoksissa.
Sen ensisijainen tehtävä ihmisillä on immuunijärjestelmän kehittäminen ja ylläpito. ADA: n koko fysiologista roolia ei kuitenkaan ole vielä täysin ymmärretty.
Rakenne
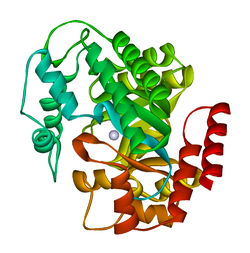
ADA esiintyy sekä pienessä muodossa (monomeerinä) että suuressa muodossa (dimeerikompleksina). Monomeerimuodossa entsyymi on polypeptidiketju, joka on taitettu kahdeksaan yhdensuuntaiseen a/β -tynnyriin, jotka ympäröivät aktiivista kohtaa olevaa keskitaskua. Kahdeksan keskimmäisen β-tynnyrin ja kahdeksan perifeerisen a-heliksin lisäksi ADA sisältää myös viisi lisäkierukkaa: tähteet 19-76 taittuvat kolmeksi heliksiksi, jotka sijaitsevat β1- ja α1-taitosten välillä; ja kaksi rinnakkaista karboksiterminaalista kierukkaa sijaitsevat β-tynnyrin aminoterminaalin poikki.
ADA -aktiivinen kohta sisältää sinkki -ionin, joka sijaitsee aktiivisen paikan syvimmässä syvennyksessä ja jota koordinoi viisi atomia His15-, His17-, His214-, Asp295- ja substraattiatomeista. Sinkki on ainoa aktiivisuuden kannalta välttämätön kofaktori .
Substraatti, adenosiini, stabiloidaan ja sitoutuu aktiiviseen kohtaan yhdeksällä vetysidoksella. Glu217: n karboksyyliryhmä, joka on suunnilleen samantasoinen substraatin puriinirenkaan kanssa, pystyy muodostamaan vetysidoksen substraatin N1: n kanssa. Asp296: n karboksyyliryhmä, myös samantasoinen substraatin puriinirenkaan kanssa, muodostaa vetysidoksen substraatin N7: n kanssa. Gly184: n NH -ryhmä pystyy muodostamaan vetysidoksen substraatin N3: n kanssa. Asp296 muodostaa sidoksia sekä Zn 2+ -ionin että substraatin 6-OH: n kanssa. His238 sitoo myös vetyä substraattiin 6-OH. Substraatin riboosin 3'-OH muodostaa vetysidoksen Asp19: n kanssa, kun taas 5'-OH muodostaa vetysidoksen His17: n kanssa. Substraatin 2'-OH ja 3'-OH muodostavat kaksi muuta vetysidosta vesimolekyyleihin aktiivisen kohdan avauksessa.
Koska aktiivinen kohta on upotettu entsyymin sisään, substraatti, kun se on sitoutunut, erotetaan lähes kokonaan liuottimesta. Alustan pinnan altistuminen liuottimelle sitoutuneena on 0,5% alustan pinnan altistumisesta vapaassa tilassa.
Reaktiot
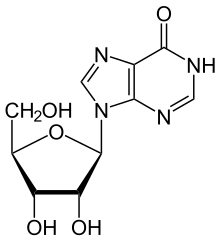
ADA deaminoi peruuttamattomasti adenosiinin ja muuntaa sen vastaavaksi nukleosidi -inosiiniksi korvaamalla aminoryhmän keto -ryhmällä.
Inosiini voidaan sitten deribosyloida (poistaa riboosista ) toisella entsyymillä, jota kutsutaan puriininukleosidifosforylaasiksi (PNP), muuttamalla se hypoksantiiniksi .
Katalyysin mekanismi
Ehdotettu mekanismi ADA-katalysoidulle deaminoinnille on stereospesifinen additio-eliminaatio tetraedrisen välituotteen kautta. Kummallakin mekanismilla Zn 2+ aktivoi vahvan elektrofiilinä vesimolekyylin, jonka emäksinen Asp295 deprotonoi hyökkäävän hydroksidin muodostamiseksi. His238 suuntaa vesimolekyylin ja vakauttaa hyökkäävän hydroksidin varauksen. Glu217 protonoidaan lahjoittamaan protoni substraatin N1: lle.
Reaktio on stereospesifinen johtuen sinkki-, Asp295- ja His238-tähteiden sijainnista, jotka kaikki ovat substraatin puriinirenkaan B-puolella.
Kilpailukykyinen esto on havaittu ADA: n tapauksessa, jossa tuote -inosiini vaikuttaa kilpailevaan entsymaattisen aktiivisuuden estäjään.
Toiminto
ADA: ta pidetään yhtenä puriinin aineenvaihdunnan tärkeimmistä entsyymeistä. Entsyymiä on löydetty bakteereista, kasveista, selkärangattomista, selkärankaisista ja nisäkkäistä, ja aminohapposekvenssi on säilynyt hyvin . Aminohapposekvenssin korkea säilyvyys viittaa ADA: n ratkaisevaan luonteeseen puriinien pelastusreitillä.
Ensisijaisesti ihmisten ADA osallistuu immuunijärjestelmän kehittämiseen ja ylläpitoon. ADA -assosiaatiota on kuitenkin havaittu myös epiteelisolujen erilaistumisen , välittäjäsiirron ja raskauden ylläpidon yhteydessä. On myös ehdotettu, että ADA stimuloi adenosiinin hajoamisen lisäksi kiihottavien aminohappojen vapautumista ja on välttämätön A1 -adenosiinireseptorien ja heterotrimeeristen G -proteiinien kytkemiseksi . Adenosiinideaminaasin puute johtaa keuhkofibroosiin, mikä viittaa siihen, että krooninen altistuminen korkeille adenosiinipitoisuuksille voi pahentaa tulehdusreaktioita sen sijaan, että ne estäisivät niitä. On myös tunnustettu, että adenosiinideaminaasiproteiini ja -aktiivisuus on säädetty hiiren sydämissä, jotka yliekspressoivat HIF1α: ta , mikä osittain selittää heikentyneet adenosiinipitoisuudet HIF-1a: ta ilmentävissä sydämissä iskeemisen stressin aikana .
Patologia
Jotkut mutaatiot adenosiinideaminaasin geenissä estävät sen ilmentymisen. Tuloksena oleva puute on yksi syy vakavaan yhdistettyyn immuunikatoa (SCID), erityisesti autosomaaliseen resessiiviseen perintöön. ADA: n puutteellisiin tasoihin on myös liittynyt keuhkotulehdusta, kateenkorvan solukuolemaa ja viallista T-solureseptorin signalointia.
Sitä vastoin mutaatiot, jotka aiheuttavat tämän entsyymin yliekspression, ovat yksi syy hemolyyttiseen anemiaan .
On joitakin todisteita siitä, että eri alleeli (ADA2) voi johtaa autismiin .
ADA: n kohoaminen on myös yhdistetty aidsiin .
Isoformit
ADA: lla on 2 isomuotoa : ADA1 ja ADA2.
- ADA1: tä esiintyy useimmissa kehon soluissa, erityisesti lymfosyyteissä ja makrofageissa , joissa se on läsnä paitsi sytosolissa ja ytimessä myös ekto- muodossa solukalvossa, joka on kiinnitetty dipeptidyylipeptidaasi-4: een (alias, CD26). ADA1 osallistuu pääasiassa solunsisäiseen aktiivisuuteen, ja sitä esiintyy sekä pienessä muodossa (monomeeri) että suuressa muodossa (dimeeri). Pienten ja suurten muotojen keskinäistä muuntumista säätelee keuhkojen '' muuntokerroin ''.
- ADA2 tunnistettiin ensimmäisen kerran ihmisen pernassa. Myöhemmin se todettiin muissa kudoksissa, mukaan lukien makrofagit, joissa se esiintyy samanaikaisesti ADA1: n kanssa. Nämä kaksi isomuotoa säätelevät adenosiinin ja deoksiadenosiinin suhdetta, mikä tehostaa loisten tappamista. ADA2: ta esiintyy pääasiassa ihmisen plasmassa ja seerumissa, ja se esiintyy yksinomaan homodimeerinä.
Lääketieteellinen merkitys
ADA2 on hallitseva muoto ihmisen veriplasmassa, ja se lisääntyy monissa sairauksissa, erityisesti immuunijärjestelmään liittyvissä sairauksissa: esimerkiksi nivelreumassa , psoriaasissa ja sarkoidoosissa . Plasman ADA2 -isoformi on myös lisääntynyt useimmissa syövissä. ADA2 ei ole kaikkialla, mutta se esiintyy rinnakkain ADA1: n kanssa vain monosyyteissä-makrofageissa.
Plasman ADA voidaan mitata käyttämällä korkean suorituskyvyn nestekromatografiaa tai entsymaattisia tai kolorimetrisiä tekniikoita. Ehkä yksinkertaisin järjestelmä on adenosiinista vapautuneen ammoniakin mittaus inosiiniksi hajotettuna. Kun plasma on inkuboitu puskuroidulla adenosiiniliuoksella, ammoniakki saatetaan reagoimaan Berthelot -reagenssin kanssa sinisen värin muodostamiseksi, joka on verrannollinen entsyymiaktiivisuuden määrään. ADA2: n mittaamiseksi lisätään ennen inkubaatiota erytro-9- (2-hydroksi-3-nonyyli) adeniini (EHNA) ADA1: n entsymaattisen aktiivisuuden estämiseksi. ADA1: n puuttuminen aiheuttaa SCID: n .
ADA: ta voidaan käyttää myös lymfosyyttisten keuhkopussin effuusioiden tai peritoneaalisen askitesin valmistelussa , koska tällaiset näytteet, joilla on alhainen ADA -taso, jättävät tuberkuloosin olennaisesti huomiotta.
Tuberkuloosin keuhkopussin effuusiot voidaan nyt diagnosoida tarkasti lisäämällä keuhkopussin nesteen adenosiinideaminaasia, yli 40 U litrassa.
Kladribiini ja pentostatiini ovat antineoplastisia aineita, joita käytetään karvasoluleukemian hoidossa ; niiden vaikutusmekanismi on adenosiinideaminaasin esto.
Katso myös
Viitteet
Lue lisää
- da Cunha JG (1992). "[Adenosiinideaminaasi. Monialainen entsyymi]". Acta Médica Portuguesa . 4 (6): 315–23. PMID 1807098 .
- Franco R, Casadó V, Ciruela F, Saura C, Mallol J, Canela EI, Lluis C (heinäkuu 1997). "Solupinnan adenosiinideaminaasi: paljon enemmän kuin ektoentsyymi". Neurobiologian edistyminen . 52 (4): 283–94. doi : 10.1016/S0301-0082 (97) 00013-0 . PMID 9247966 . S2CID 40318396 .
- Valenzuela A, Blanco J, Callebaut C, Jacotot E, Lluis C, Hovanessian AG, Franco R (1997). "HIV-1-kirjekuori gp120 ja viruspartikkelit estävät adenosiinideaminaasin sitoutumisen ihmisen CD26: een". Kokeellisen lääketieteen ja biologian edistysaskeleet . 421 : 185–92. doi : 10.1007/978-1-4757-9613-1_24 . ISBN 978-1-4757-9615-5. PMID 9330696 .
- Moriwaki Y, Yamamoto T, Higashino K (lokakuu 1999). "Puriinin aineenvaihduntaan osallistuvat entsyymit-katsaus histokemiallisesta lokalisoinnista ja toiminnallisista vaikutuksista". Histologia ja histopatologia . 14 (4): 1321–40. PMID 10506947 .
- Hirschhorn R (1993). "Kahden uuden missense-mutaation (R156C ja S291L) tunnistaminen kahdella ADA-SCID-potilaalla, jotka ovat epätavallisia vasteessa hoitoon osittaisilla verensiirroilla". Ihmisen mutaatio . 1 (2): 166–8. doi : 10.1002/humu.1380010214 . PMID 1284479 . S2CID 44617309 .
- Berkvens TM, van Ormondt H, Gerritsen EJ, Khan PM, van der Eb AJ (elokuu 1990). "Identtinen 3250 emäsparin deleetio kahden AluI-toiston välillä etuyhteydettömien ADA-SCID-potilaiden ADA-geeneissä". Genomiikka . 7 (4): 486–90. doi : 10.1016/0888-7543 (90) 90190-6 . PMID 1696926 .
- Aran JM, Colomer D, Matutes E, Vives-Corrons JL, Franco R (elokuu 1991). "Adenosiinideaminaasin läsnäolo mononukleaaristen verisolujen pinnalla: immunokemiallinen lokalisointi valon ja elektronimikroskopian avulla" . Journal of Histochemistry and Cytochemistry . 39 (8): 1001–8. doi : 10.1177/39.8.1856451 . PMID 1856451 .
- Bielat K, Tritsch GL (huhtikuu 1989). "Ihmisen punasolujen adenosiinideaminaasin ektoentsyymiaktiivisuus". Molekyylien ja solujen biokemia . 86 (2): 135–42. doi : 10.1007/BF00222613 . PMID 2770711 . S2CID 20850552 .
- Hirschhorn R, Tzall S, Ellenbogen A, Orkin SH (helmikuu 1989). "Lämpölabiiliseen adenosiinideaminaasiin (ADA) johtavan pistemutaation tunnistaminen kahdella etuyhteydettömällä lapsella, joilla on osittainen ADA-puutos" . Journal of Clinical Investigation . 83 (2): 497–501. doi : 10.1172/JCI113909 . PMC 303706 . PMID 2783588 .
- Murray JL, Perez-Soler R, Bywaters D, Hersh EM (tammikuu 1986). "Adenosiinideaminaasin (ADA) ja 5' -nukleotidaasin (5NT) aktiivisuuden väheneminen perifeerisen veren T -soluissa Hodgkinin taudissa". American Journal of Hematology . 21 (1): 57–66. doi : 10.1002/ajh.2830210108 . PMID 3010705 . S2CID 25540139 .
- Wiginton DA, Kaplan DJ, States JC, Akeson AL, Perme CM, Bilyk IJ, Vaughn AJ, Lattier DL, Hutton JJ (joulukuu 1986). "Ihmisen adenosiinideaminaasin geenin täydellinen sekvenssi ja rakenne". Biokemia . 25 (25): 8234–44. doi : 10.1021/bi00373a017 . PMID 3028473 .
- Akeson AL, Wiginton DA, Dusing MR, States JC, Hutton JJ (marraskuu 1988). "Mutantit ihmisen adenosiinideaminaasialleelit ja niiden ilmentyminen transfektoimalla fibroblasteiksi" . Journal of Biological Chemistry . 263 (31): 16291–6. doi : 10.1016/S0021-9258 (18) 37591-4 . PMID 3182793 .
- Glader BE, Backer K (helmikuu 1988). "Kohonnut punasolujen adenosiinideaminaasiaktiivisuus: häiriötekijöiden erytropoieesin merkki Diamond-Blackfan-anemiassa ja muissa hematologisissa sairauksissa". British Journal of Hematology . 68 (2): 165–8. doi : 10.1111/j.1365-2141.1988.tb06184.x . PMID 3348976 . S2CID 44789636 .
- Petersen MB, Tranebjaerg L, Tommerup N, Nygaard P, Edwards H (helmikuu 1987). "Adenosiinideaminaasigeenilokuksen uusi määrittäminen kromosomiin 20q13 X 11 tutkimalla potilasta, jolla on interstitiaalinen deleetio 20q" . Journal of Medical Genetics . 24 (2): 93–6. doi : 10.1136/jmg.24.2.93 . PMC 1049896 . PMID 3560174 .
- Orkin SH, Goff SC, Kelley WN, Daddona PE (huhtikuu 1985). "Ihmisen adenosiinideaminaasi -cDNA: iden ohimenevä ilmentyminen: toimimattoman kloonin tunnistaminen, joka johtuu yksittäisestä aminohapposubstituutiosta" . Molekyyli- ja solubiologia . 5 (4): 762-7. doi : 10.1128/mcb.5.4.762 . PMC 366780 . PMID 3838797 .
- Valerio D, Duyvesteyn MG, Dekker BM, Weeda G, Berkvens TM, van der Voorn L, van Ormondt H, van der Eb AJ (helmikuu 1985). "Adenosiinideaminaasi: geenin karakterisointi ja ilmentyminen merkittävän promoottorin kanssa" . EMBO -lehti . 4 (2): 437–43. doi : 10.1002/j.1460-2075.1985.tb03648.x . PMC 554205 . PMID 3839456 .
- Bonthron DT, Markham AF, Ginsburg D, Orkin SH (elokuu 1985). "Pistemutaation tunnistaminen immuunikatosta vastuussa olevasta adenosiinideaminaasigeenistä" . Journal of Clinical Investigation . 76 (2): 894-7. doi : 10.1172/JCI112050 . PMC 423929 . PMID 3839802 .
- Daddona PE, Shewach DS, Kelley WN, Argos P, Markham AF, Orkin SH (lokakuu 1984). "Ihmisen adenosiinideaminaasi. CDNA ja täydellinen primaarinen aminohapposekvenssi" . Journal of Biological Chemistry . 259 (19): 12101–6. doi : 10.1016/S0021-9258 (20) 71325-6 . PMID 6090454 .
- Valerio D, Duyvesteyn MG, Meera Khan P, Geurts van Kessel A, de Waard A, van der Eb AJ (marraskuu 1983). "CDNA -kloonien eristäminen ihmisen adenosiinideaminaasia varten". Gene . 25 (2–3): 231–40. doi : 10.1016/0378-1119 (83) 90227-5 . PMID 6198240 .
Ulkoiset linkit
- ADA -ihmisen geenin sijainti UCSC -genomiselaimessa .
- ADA ihmisen geeni yksityiskohtia UCSC Genome selain .
- PDBe-KB tarjoaa yleiskatsauksen kaikista ATE: ssä saatavilla olevista rakennetiedoista ihmisen adenosiinideaminaasia varten
- PDBe-KB tarjoaa yleiskatsauksen hiiren adenosiinideaminaasia koskevista ATE: n rakenteista