Kannabinoidireseptorin tyyppi 2 - Cannabinoid receptor type 2
Kannabinoidireseptorin tyyppi 2 , lyhennettynä CB 2 , on G-proteiiniin kytketty reseptori päässä kannabinoidin reseptorin perhe, joka ihmisillä on koodaa CNR2 geeni. Se liittyy läheisesti tyypin 1 kannabinoidireseptoriin (CB 1 ), joka on suurelta osin vastuussa endokannabinoidivälitteisen presynaptisen eston tehokkuudesta, kannabiksen aktiivisen aineen tetrahydrokannabinolin (THC) ja muiden fytokannabinoidien (kasvin ) psykoaktiivisista ominaisuuksista. kannabinoidit). Pääasiallinen endogeeninen ligandi CB 2 -reseptori on 2-arakidonoyyliglyserolin (2-AG).
CB 2 on kloonattiin vuonna 1993 tutkimuksen ryhmä Cambridge etsii toisen kannabinoidireseptorin, joka voisi selittää farmakologisia ominaisuuksia tetrahydrokannabinolin . Reseptori tunnistettiin cDNA: iden joukossa sen perusteella, että se oli aminohapposekvenssissä samanlainen kuin vuonna 1990 löydetty kannabinoidireseptorin tyyppi 1 (CB 1 ) -reseptori. Tämän reseptorin löytäminen auttoi tarjoamaan molekyylisen selityksen kannabinoidien vakiintuneille vaikutuksille immuunijärjestelmään. järjestelmään.
Rakenne
CB 2 -reseptoria koodaa CNR2 geeni. Noin 360 aminohappoa käsittävät ihmisen CB 2 -reseptorin, joten se on jonkin verran lyhyempi kuin 473-aminohappoa pitkä CB 1 -reseptoriin.
Kuten havaitaan yleisesti G-proteiiniin kytkettyjen reseptorien, CB 2 reseptorilla on seitsemän solukalvon läpi ulottuva domeenit, joka on glykosyloitunut N-pää , ja solunsisäinen C-pään . C-päähän CB 2 reseptorien näyttää olevan kriittinen rooli säätelyssä ligandin indusoiman reseptorin herkkyyden väheneminen ja downregulation toistuvan agonistin sovellus, ehkä aiheuttaa reseptorin tulla vähemmän herkkä tietyille ligandeja.
Ihmisen CB 1 ja CB 2 -reseptoreihin oltava noin 44% aminohappojen samankaltaisuuteen. Kun otetaan huomioon vain reseptorien kalvojen läpäisevät alueet, aminohappojen samankaltaisuus kahden reseptorin alatyypin välillä on noin 68%. Aminohapposekvenssi CB 2 -reseptori on vähemmän voimakkaasti konservoitunut ihmisen ja jyrsijöiden verrattuna aminohapposekvenssiin CB 1 -reseptoriin. Joka perustuu tietokoneella mallintamista, ligandi-vuorovaikutusten CB 2 -reseptorin tähteet S3.31 ja F5.46 näkyy välisten erojen määrittämiseksi CB 1 ja CB 2 -reseptorin selektiivisyyttä. CB 2 -reseptoreihin, lipofiiliset ryhmät vuorovaikutuksessa kanssa F5.46 jäännös, joiden avulla ne voivat muodostaa vetysidoksen kanssa S3.31 jäännös. Nämä vuorovaikutukset aiheuttavat konformatiivisen muutoksen reseptorirakenteessa, joka laukaisee useiden solunsisäisten signalointireittien aktivoitumisen. Lisätutkimuksia tarvitaan signalointireitin aktivaation tarkkojen molekyylimekanismien määrittämiseksi.
Mekanismi
Kuten CB 1 -reseptoreihin, CB 2 -reseptorit inhiboivat adenylaattisyklaasia kautta Gi / Go α -alayksiköitä. CB 2 voi myös pari stimuloivia Ga : n alayksiköitä, jotka johtavat solunsisäisten cAMP, kuten on osoitettu ihmisen leukosyyteistä. Kautta niiden G βγ alayksiköt, CB 2 -reseptorien tiedetään myös kytkeä MAPK-ERK-reitin , monimutkainen ja erittäin konservoituneita signaalitransduktion reaktiotie, joka säätelee useiden solun prosessien kypsä ja kehittää kudoksissa. Aktivointi MAPK-ERK-reitin CB 2 -reseptorin agonistit toimivat kautta G βγ alayksikön lopulta johtaa muutoksiin solujen vaeltamiseen .
Viisi tunnettua kannabinoidia tuotetaan endogeenisesti: arakidonoyylietanoliamiini (anandamidi), 2-arakidonoyyliglyseroli (2-AG), 2-arakidonyyliglyseryylieetteri (noladiinieetteri), virodamiini sekä N-arakidonoyylidopamiini (NADA). Monet näistä ligandien näyttävät osoittavan ominaisuuksien toiminnallinen valikoivuus on CB 2 -reseptori: 2-AG aktivoi MAPK-ERK-reitin, kun taas noladin inhiboi adenylyylisyklaasia.
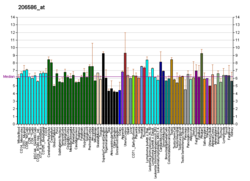
Ilmaisu
Kiista
Alun perin ajateltiin, että CB2-reseptori ilmentyi vain ääreiskudoksessa, kun taas CB1-reseptori on endogeeninen reseptori hermosoluissa. Viimeaikainen työ immunohistokemiallisen värjäyksen kanssa on osoittanut ekspressiota hermosoluissa. Myöhemmin osoitettiin, että CB2-hiiret hävisivät, tuottivat saman immunohistokemiallisen värjäytymisen , mikä osoittaa CB2-reseptorin läsnäolon, jossa yhtään ei ilmentynyt. Tämä on luonut pitkän historian keskustelun CB2-reseptorin keskushermoston ilmentymisestä. Vuonna 2014 kuvattiin uusi hiirimalli, joka ilmentää fluoresoivaa proteiinia aina, kun CB2 ilmentyy solussa. Tämä voi ratkaista kysymyksiä CB2-reseptorien ilmentymisestä eri kudoksissa.
Immuunijärjestelmä
Alustavien tutkimusten CB 2 -reseptorin ilmentymisen kuviot keskittyvät läsnä ollessa CB 2 reseptorien perifeerisissä kudoksissa ja immuunijärjestelmän , ja löysi CB 2 -reseptori -mRNA: n että perna , nielurisat , ja kateenkorva . CB 2 : n ilmentymistä ihmisen perifeerisen veren mononukleaaristen solujen kerääntyminen proteiinin taso on varmistettu kokosolu radioligandin sitoutumisen. Northern blot -analyysi osoittaa edelleen CNR2-geenin ilmentymisen immuunikudoksissa, joissa ne ovat ensisijaisesti vastuussa sytokiinien vapautumisen välittämisestä . Nämä reseptorit lokalisoitiin immuunisoluihin, kuten monosyytteihin , makrofageihin , B-soluihin ja T-soluihin .
Aivot
Lisätutkimisesta ilmentymismalleihin CB 2 -reseptoreihin paljasti, että CB 2 -reseptorin geenin transkripteja on myös ilmaistu aivoissa , mutta ei niin tiheästi kuin CB 1 -reseptorin ja sijaitsevat eri soluissa. Toisin kuin CB 1 -reseptorit, aivoissa CB 2 -reseptorit löytyvät pääasiassa mikrogliasta . CB 2 -reseptoria ekspressoidaan joissakin keskushermoston hermosoluissa (esim. Aivorungossa ), mutta ilmentyminen on hyvin vähäistä. CB2R: t ilmentyvät joillakin rotan verkkokalvosolutyypeillä. Funktionaalinen CB 2 reseptorit ilmentyvät hermosoluissa vatsanpuoleisen tegmentaalialueeseen ja hippokampuksessa vaatineet, että laaja ilmentyminen ja toiminnallinen merkitys keskushermostossa ja erityisesti hermosolujen signaalin lähetyksen.
Ruoansulatuskanava
CB 2 -reseptoreita esiintyy myös koko maha- järjestelmä, jossa ne moduloivat suoliston tulehdusvastetta. Siten, CB 2 -reseptori on potentiaalinen terapeuttinen kohde tulehduksellisten suolistosairauksien , kuten Crohnin tauti ja haavainen koliitti . Endokannabinoidien roolilla sinänsä on tärkeä rooli estettäessä tarpeetonta immuunitoimintaa luonnollisessa suolistofloorassa. Tämän järjestelmän toimintahäiriö, mahdollisesti FAAH: n liiallisen toiminnan vuoksi, voi johtaa IBD: hen. CB 2 aktivointi voi myös olla rooli hoitoon ärtyvän suolen oireyhtymä . Kannabinoidireseptorin agonistit vähentävät suoliston liikkuvuutta IBS-potilailla.
Perifeerinen hermosto
Soveltaminen CB 2 erityisiä antagonistien on havaittu, että nämä reseptorit ovat mukana myös välittäjänä kipulääke vaikutuksia ääreishermostossa. Nosiseptiiviset aistihermot eivät kuitenkaan ekspressoi näitä reseptoreita, ja niiden uskotaan nykyään olevan määrittelemättömässä, ei-hermosoluissa. Mahdollisia ehdokkaita ovat syöttösolut , joiden tiedetään helpottavan tulehdusreaktiota. Näiden vastausten kannabinoidivälitteinen esto voi aiheuttaa haitallisten ärsykkeiden käsityksen heikkenemisen.
Toiminto
Immuunijärjestelmä
Ensisijainen tutkimus toiminnasta CB 2 -reseptori on keskittynyt reseptorin vaikutuksia immunologista aktiivisuutta leukosyyttien . Spesifisyyden vuoksi tämä reseptori on ollut osallisena monissa moduloivissa toiminnoissa, mukaan lukien immuunijärjestelmän suppressio, apoptoosin indusointi ja solujen migraation indusointi. Kautta niiden adenyylisyklaasin inhiboinnin kautta Gi / Go α -alayksiköt, CB 2 -reseptorin agonistit aiheuttavat vähentää solunsisäisiä tasoja syklisen adenosiinimonofosfaatin (cAMP). CB 2 signaloi myös Ga: n kautta ja lisää solunsisäistä cAMP: tä ihmisen leukosyyteissä, mikä johtaa interleukiinien 6 ja 10 induktioon. Vaikka cAMP-kaskadin tarkasta roolista immuunivasteiden säätelyssä keskustellaan parhaillaan, laboratoriot ovat aiemmin osoittaneet, että adenylyylisyklaasia CB 2 reseptorin agonistit johtaa vähenemiseen sitoutuminen transkriptiotekijä CREB (cAMP-vaste-elementtiin sitoutuva proteiini) ja DNA: ta . Tämä väheneminen aiheuttaa muutoksia kriittisten immunoregulointigeenien ilmentymisessä ja lopulta immuunijärjestelmän toiminnan tukahduttamisen.
Myöhemmät tutkimukset, joissa tutkittiin synteettisen kannabinoidiagonistin JWH-015 vaikutusta CB 2 -reseptoreihin, paljastivat, että muutokset cAMP-tasoissa johtavat leukosyyttireseptorityrosiinikinaasin fosforylaatioon Tyr-505: ssä, mikä johtaa T- solureseptorisignaloinnin estoon . Siten, CB 2 -agonistit voivat myös olla käyttökelpoisia hoidettaessa tulehdusta ja kipua, ja tällä hetkellä tutkitaan, erityisesti kivun muotoja, jotka eivät reagoi hyvin tavanomaisiin hoitoihin, kuten neuropaattista kipua . Näiden havaintojen mukaisia ovat tutkimukset, jotka osoittavat lisääntyneen CB 2 -reseptorin ilmentymisen selkäytimessä, selkäjuuren ganglionissa ja aktivoidussa mikrogliassa jyrsijän neuropaattisen kipumallissa sekä ihmisen heptosellulaarisen karsinoomakasvaimen näytteissä.
CB 2 -reseptorit on myös liitetty säätelyssä itseohjautuva ja säilyttäminen reunavyöhykkeen B-solujen . Tutkimus käyttäen knock-out-hiirillä havaittu, että CB 2 -reseptori on olennainen ylläpitämiseksi sekä MZ B-solujen ja niiden esiastesolujen T2-MZP , mutta ei niiden kehittämistä. Sekä B-soluja että niiden esiasteita, joilta puuttuu tämä reseptori, löydettiin pienemmässä määrin, selitettynä toissijaisella havainnolla, jonka mukaan 2-AG-signaloinnin osoitettiin indusoivan asianmukaista B-solujen migraatiota MZ: hen. Ilman reseptoria MZ B -linjasolujen veripitoisuudessa tapahtui ei-toivottu piikki ja IgM : n tuotannon merkittävä väheneminen . Vaikka tämän prosessin taustalla olevaa mekanismia ei ole täysin ymmärretty, tutkijat ehdottivat, että tämä prosessi voi johtua aktivaatiosta riippuvasta cAMP- pitoisuuden vähenemisestä , mikä johtaa CREB: n säätelemien geenien vähentyneeseen transkriptioon, mikä lisää epäsuorasti TCR-signalointia ja IL-2- tuotantoa. Yhdessä nämä havainnot osoittavat, että endokannabinoidijärjestelmää voidaan hyödyntää immuniteetin parantamiseksi tietyille patogeeneille ja autoimmuunisairauksille.
Kliiniset sovellukset
CB 2 reseptorit voivat olla mahdollisia terapeuttisia rooleja neurodegeneratiivisten häiriöiden, kuten Alzheimerin tauti . Erityisesti, CB 2 agonisti JWH-015: n osoitettiin indusoivan makrofagien poistamiseksi natiivin beeta-amyloidi -proteiinin jäädytetty ihmisen kudoksissa. Alzheimerin tautia sairastavilla potilailla beeta-amyloidiproteiinit muodostavat aggregaatteja, joita kutsutaan seniiliksi plakkeiksi , jotka häiritsevät hermoston toimintaa.
Muutokset endokannabinoiditasot ja / tai CB 2 reseptorin ilmaisuja on raportoitu lähes kaikissa sairauksien ihmisille, jotka vaihtelevat kardiovaskulaaristen, maha, maksa, munuaiset, hermoston, psykiatriset, luu, iho, autoimmuunisairaus, keuhkosairaudet kipua ja syöpään. Esiintyvyys tämä suuntaus viittaa siihen, että moduloiva CB 2 -reseptorin aktiivisuutta joko selektiivinen CB 2 reseptorin agonistit tai käänteiset agonistit / antagonistit riippuen sairaudesta ja sen etenemisen pitää ainutlaatuinen terapeuttista potentiaalia näiden patologioiden
Kokaiinipalkkion mukauttaminen
Tutkijat tutkivat CB 2 -agonistien vaikutuksia kokaiinin itsensä antamiseen hiirillä. JWH-133: n systeeminen anto vähensi kokaiinin itseinfuusioiden määrää hiirissä sekä vähensi liikkumisaktiivisuutta ja murtumispistettä (korkein tasoisten puristimien määrä kokaiinin saamiseksi). JWH-133: n paikallisen injektion ytimeen accumbensiin havaittiin tuottavan samat vaikutukset kuin systeemisellä annolla. JWH-133: n systeeminen anto vähensi myös solunulkoisen dopamiinin kohoamista basaalista ja kokaiinista . Nämä havainnot jäljitellä toinen, rakenteellisesti erilaisia CB 2 -agonisti, GW-405833 , ja purettiin antamalla CB 2 -antagonisti, AM-630 .
Ligandit
Monet selektiivisiä ligandeja CB 2 -reseptorin ovat nyt saatavilla.
Agonistit
Osittaiset agonistit
Määrittelemättömät tehon agonistit
Yrtti
Käänteiset agonistit
Sitovat affiniteetit
| CB 1 affiniteetti (K i ) | Tehokkuus CB: tä kohtaan 1 | CB 2 affiniteetti (K i ) | Tehokkuus CB 2: ta kohtaan | Tyyppi | Viitteet | |
|---|---|---|---|---|---|---|
| Anandamidi | 78 nM | Osittainen agonisti | 370 nM | Osittainen agonisti | Endogeeninen | |
| N-arakidonoyylidopamiini | 250 nM | Agonisti | 12000 nM | ? | Endogeeninen | |
| 2-arakidonoyyliglyseroli | 58,3 nM | Täysi agonisti | 145 nM | Täysi agonisti | Endogeeninen | |
| 2-arakidonyyliglyseryylieetteri | 21 nM | Täysi agonisti | 480 nM | Täysi agonisti | Endogeeninen | |
| Tetrahydrokannabinoli | 10 nM | Osittainen agonisti | 24 nM | Osittainen agonisti | Fytogeeninen | |
| EGCG | 33,6 μM | Agonisti | > 50 μM | ? | Fytogeeninen | |
| EGC | 35,7 μM | Agonisti | > 50 μM | ? | Fytogeeninen | |
| EKG | 47,3 μM | Agonisti | > 50 μM | ? | Fytogeeninen | |
| N- alkyyliamidi | - | - | <100 nM | Osittainen agonisti | Fytogeeninen | |
| β- karyofylleeni | - | - | <200 nM | Täysi agonisti | Fytogeeninen | |
| Falcarinoli | <1 μM | Käänteinen agonisti | ? | ? | Fytogeeninen | |
| Rutamarin | - | - | <10 μM | ? | Fytogeeninen | |
| 3,3'-diindolyylimetaani | - | - | 1 μM | Osittainen agonisti | Fytogeeninen | |
| AM-1221 | 52,3 nM | Agonisti | 0,28 nM | Agonisti | Synteettinen | |
| AM-1235 | 1,5 nM | Agonisti | 20,4 nM | Agonisti | Synteettinen | |
| AM-2232 | 0,28 nM | Agonisti | 1,48 nM | Agonisti | Synteettinen | |
| UR-144 | 150 nM | Täysi agonisti | 1,8 nM | Täysi agonisti | Synteettinen | |
| JWH-007 | 9,0 nM | Agonisti | 2,94 nM | Agonisti | Synteettinen | |
| JWH-015 | 383 nM | Agonisti | 13,8 nM | Agonisti | Synteettinen | |
| JWH-018 | 9,00 ± 5,00 nM | Täysi agonisti | 2,94 ± 2,65 nM | Täysi agonisti | Synteettinen |
Katso myös
Viitteet
Ulkoiset linkit
- "Kannabinoidireseptorit: CB 2 " . IUPHAR-reseptoreiden ja ionikanavien tietokanta . Kansainvälinen perus- ja kliinisen farmakologian liitto. Arkistoitu alkuperäisestä 2012-03-05 . Haettu 25.11.2008 .
Tämä artikkeli sisältää Yhdysvaltojen kansallisen lääketieteellisen kirjaston tekstiä , joka on julkista .