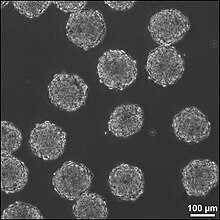
Alkion runko - Embryoid body
Alkiokappaleet ( EB ) ovat kolmiulotteisia aggregaatteja pluripotentteista kantasoluista .
EB: t ovat ihmisen alkion kantasolujen erilaistumista alkiokappaleiksi, jotka vaarantavat kolme alkion alkukerrosta.
Tausta
Pluripotentteja solutyyppejä, jotka käsittävät alkion kappaleita, ovat alkion kantasolut (ESC), jotka ovat peräisin hiiren (mESC), kädellisten ja ihmisen (hESC) lähteistä peräisin olevien alkioiden blastokystivaiheesta . Lisäksi EB: itä voidaan muodostaa alkion kantasoluista, jotka on johdettu vaihtoehtoisilla tekniikoilla, mukaan lukien somaattisten solujen ydinsiirto tai somaattisten solujen uudelleenohjelmointi indusoitujen pluripotenttisten kantasolujen (iPS) tuottamiseksi. Samankaltaisia kuin yksikerroksisissa muodoissa viljeltyjä ESC: itä , alkiokappaleissa olevat ESC: t erilaistuvat ja solut määritellään kolmen alkiolinjan - endodermin, ektodermin ja mesodermin - pitkin , jotka käsittävät kaikki somaattiset solutyypit.
Toisin kuin yksikerroksiset viljelmät, pallomaiset rakenteet, jotka muodostuvat, kun ESC: t aggregoituvat, mahdollistavat tarttumattoman EB-viljelyn suspensiossa, mikä tekee EB-viljelmistä luontaisesti skaalautuvia, mikä on hyödyllistä bioprosessointimenetelmissä, jolloin suuria solutuottoja voidaan tuottaa mahdollisia kliinisiä sovelluksia. Lisäksi, vaikka EB: llä on suurelta osin erilaistuneiden solutyyppien heterogeenisia kuvioita, ESC: t pystyvät vastaamaan samanlaisiin vihjeisiin, jotka ohjaavat alkion kehitystä . Siksi kolmiulotteinen rakenne, mukaan lukien monimutkaisten soluadheesioiden luominen ja parakriiniset signaloinnit EB-mikroympäristössä, mahdollistaa erilaistumisen ja morfogeneesin, joka tuottaa mikrokudoksia, jotka ovat samanlaisia kuin natiivi kudosrakenteet. Tällaiset mikrokudokset lupaavat korjata suoraan tai epäsuorasti vaurioituneen tai sairaan kudoksen regeneratiivisen lääketieteen sovelluksissa sekä in vitro -testauksessa lääketeollisuudessa ja mallina alkion kehityksestä.
Muodostus
EB: t muodostuvat Ca2+ -riippuvaisen adheesiomolekyylin E-kadheriinin homofiilisestä sitoutumisesta , joka ilmentyy voimakkaasti erilaistumattomissa ESC: issä. Kun ESC: itä viljellään yksittäisinä soluina ilman erilaistumista estäviä tekijöitä, ne aggregoituvat spontaanisti muodostaen EB: itä. Tällainen spontaani muodostuminen tapahtuu usein irtotavarana olevissa suspensioviljelmissä, joissa malja päällystetään ei-tarttuvilla materiaaleilla, kuten agarilla tai hydrofiilisillä polymeereillä, edistääkseen ensisijaista tarttumista yksittäisten solujen välille viljelysubstraatin sijasta. Koska hESC: lle tehdään apoptoosi, kun sitä viljellään yksittäisinä soluina, EB: n muodostuminen edellyttää usein rho-assosioituneen kinaasin (ROCK) reitin estäjien käyttöä , mukaan lukien pienet molekyylit Y-27632 ja 2,4 disubstituoitu tiatsoli (Thiazovivin/Tzv). Vaihtoehtoisesti, dissosiaation välttämiseksi yksittäisiksi soluiksi, EB: itä voidaan muodostaa hESC: stä erottamalla manuaalisesti kiinnittyneet pesäkkeet (tai pesäkkeiden alueet) ja viljellä sitten suspensiossa. EB: n muodostuminen suspensiossa on mahdollista muodostaa suuria määriä EB: itä, mutta se ei juurikaan hallitse syntyvien aggregaattien kokoa, mikä johtaa usein suuriin, epäsäännölliseen muotoon. Vaihtoehtoisesti sekoitetuille viljelyalustoille annetut hydrodynaamiset voimat lisäävät EB -kokojen homogeenisuutta, kun ESC: itä siirretään irtosuspensioihin.
EB: ien muodostumista voidaan myös kontrolloida tarkemmin siirtämällä tunnetut solutiheydet yksittäisiin pisaroihin (10-20 µL), jotka on ripustettu Petri-maljan kannesta, jotka tunnetaan roikkuvina pisaroina. Vaikka tämä menetelmä mahdollistaa EB-koon hallinnan muuttamalla solujen lukumäärää tippaa kohti, roikkuvien pisaroiden muodostuminen on työvoimavaltaista eikä ole helposti mukautettavissa skaalautuviin viljelmiin. Lisäksi väliainetta ei voi helposti vaihtaa perinteisen riippuvan tipan muodossa, mikä edellyttää ripustettavien pisaroiden siirtämistä irtotavarana suspensioviljelmiin 2-3 päivän muodostumisen jälkeen, jolloin yksittäiset EB: t pyrkivät agglomeroitumaan. Viime aikoina on kehitetty uusia tekniikoita, jotka mahdollistavat medianvaihdon muokatussa roikkuvassa pudotusmuodossa. Lisäksi on kehitetty tekniikoita solujen fyysiseksi erottamiseksi pakottamalla aggregaatit ESC: iin yksittäisten kuoppien sisällä tai rajoittamalla liima -alustoille, mikä mahdollistaa suuremman läpäisykyvyn ja hallitun EB -muodostumisen. Viime kädessä EB: n muodostamiseen käytetyt menetelmät voivat vaikuttaa EB -populaatioiden heterogeenisuuteen aggregaatiokinetiikan, EB -koon ja tuoton sekä erilaistumisratojen suhteen.
Erilaisuus EB: n sisällä
ESC: n erilaistumisprotokollien puitteissa EB: n muodostumista käytetään usein menetelmänä spontaanin erilaistumisen aloittamiseksi kohti kolmea alkiolinjaa . EB -erilaistuminen alkaa ulkoisten solujen määrittelystä kohti primitiivistä endodermin fenotyyppiä. Ulkopuolella olevat solut tallettavat sitten solunulkoisen matriisin (ECM), joka sisältää kollageeni IV: tä ja laminiinia , samankaltaisia kuin peruskalvon koostumus ja rakenne . Vasteena ECM-kerrostumalle EB: t muodostavat usein kystisen ontelon, jolloin peruskalvon kanssa kosketuksiin joutuvat solut pysyvät elinkykyisinä ja sisäpuolella olevat solut käyvät apoptoosiin, mikä johtaa nesteellä täytettyyn onteloon, jota ympäröivät solut. Myöhempi erilaistuminen muodostaa johdannaisia kolmesta ituradasta. Jos lisäravinteita ei ole, ESC: iden "oletus" -erotus on suurelta osin kohti ektodermiä ja sen jälkeisiä hermolinjoja . Kuitenkin vaihtoehtoisia väliainekoostumuksia, mukaan lukien naudan sikiön seerumin käyttö sekä määritellyt kasvutekijälisäaineet, on kehitetty edistämään erilaistumista kohti mesodermi- ja endodermilinjoja .
Kolmiulotteisen EB-rakenteen seurauksena EB-erilaistumisen aikana esiintyy monimutkaista morfogeneesiä, mukaan lukien sekä epiteeli- että mesenkymaalisten kaltaisten solupopulaatioiden ilmestyminen sekä epiteeli-mesenkymaaliseen siirtymään (EMT) liittyvien merkkien ilmaantuminen . Lisäksi EB -solupopulaatioiden välisen signaloinnin aiheuttamat induktiiviset vaikutukset johtavat alueellisesti ja ajallisesti määriteltyihin muutoksiin, jotka edistävät monimutkaista morfogeneesiä . Kudoksen kaltaisia rakenteita esitetään usein EB: ssä, mukaan lukien varhaisten verisuonien rakenteita muistuttavien verisaarten esiintyminen kehittyvässä alkiossa, samoin kuin neuriittipidennysten kuviointi (joka viittaa hermosolujen organisoitumiseen) ja spontaanit supistumistoiminnot (osoittavat sydänlihassolujen erilaistumista) ), kun EB: t levitetään liima -alustoille, kuten gelatiinille . Viime aikoina monimutkaisia rakenteita, mukaan lukien optiset kuppimaiset rakenteet, luotiin in vitro EB-erilaistumisen seurauksena.
Rinnakkaisuuksia alkion kehityksen kanssa
Suuri osa alkion kantasolujen erilaistumiseen ja morfogeneesiin liittyvistä tutkimuksista on peräisin kehitysbiologian ja nisäkkäiden alkion syntyyn liittyvistä tutkimuksista. Esimerkiksi heti blastokystin kehitysvaiheen jälkeen (josta ESC: t ovat peräisin) alkio kokee mahalaukun , jolloin sisäisen solumassan soluspesifikaatio johtaa viskeraalisen endodermin ja epiblastin muodostumiseen . Kun etu- ja taka-akseli muodostuu, alkio kehittää ohimenevän rakenteen, joka tunnetaan primitiivisenä juovana. Suuri osa alkeellisesta kuvioinnista, joka tapahtuu primitiivisen juovan muodostumisen ja migraation aikana, johtuu agonistien ja antagonistien erittymisestä eri solupopulaatioissa, mukaan lukien Wnt -kasvutekijät ja transformoiva kasvutekijä β (TGFβ) -perheet (Lefty 1, Nodal) ), samojen molekyylien repressorit (Dkk-1, Sfrp1, Sfrp5). Alkiogeneesin ja ESC: n erilaistumisen samankaltaisuuksien vuoksi monet samoista kasvutekijöistä ovat keskeisiä suuntautuneissa erilaistumismenetelmissä.
Lisäksi EB-kulttuurin edistyminen johti alkion organoidien (Gastruloids) kehittämiseen, jotka osoittavat huomattavia rinnakkaisuuksia alkion kehitykseen, kuten symmetriaa rikkova, paikallinen brachyury- ilmentyminen, alkion akselien (anteroposterior, dorsoventral ja vasen-oikea) muodostuminen ja gastrulaation kaltaiset liikkeet.
Haasteita erilaisuuden ohjaamiseen
Toisin kuin ESC: iden erilaistuminen yksikerroksisissa viljelmissä, jolloin liukoisten morfogeenien lisäämistä ja solunulkoista mikroympäristöä voidaan hallita tarkasti ja homogeenisesti, EB: iden kolmiulotteinen rakenne asettaa haasteita suunnatulle erilaistumiselle. Esimerkiksi viskeraalinen endodermipopulaatio, joka muodostaa EB: n ulkopuolen, luo ulkopuolisen "kuoren", joka koostuu tiiviisti kytkeytyneistä epiteelin kaltaisista soluista sekä tiheästä ECM: stä . Tällaisten fyysisten rajoitusten vuoksi yhdessä EB -koon kanssa EB: ssä esiintyy kuljetusrajoituksia , jotka muodostavat morfogeenien, metaboliittien ja ravinteiden kaltevuudet. On arvioitu, että hapen kuljetus on rajoitettu solukokoonpanoissa, joiden halkaisija on suurempi kuin noin 300 µm; tällaisten gradienttien kehitykseen vaikuttavat kuitenkin myös molekyylien koko ja solujen imeytymisnopeudet. Siksi morfogeenien toimittaminen EB: hen johtaa erilaistuneiden solupopulaatioiden heterogeenisyyden lisääntymiseen ja tehokkuuden laskuun verrattuna yksikerroksisiin viljelmiin. Yksi tapa käsitellä kuljetusrajoituksia EB: n sisällä on ollut morfogeenien polymeerinen toimitus EB -rakenteen sisältä. Lisäksi EB: itä voidaan viljellä yksittäisinä mikrokudoksina ja koota myöhemmin suuremmiksi rakenteiksi kudostekniikan sovelluksia varten. Vaikka kolmiulotteisista kiinnittymisistä ja signaloinnista johtuva monimutkaisuus voi tiivistää natiivimpia kudosrakenteita, se luo myös haasteita ymmärtää mekaanisten, kemiallisten ja fyysisten signaalien suhteellisia vaikutuksia tuloksena oleviin solujen fenotyyppeihin ja morfogeneesiin.