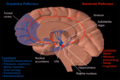
Nucleus accumbens - Nucleus accumbens
| Ydin accumbens | |
|---|---|
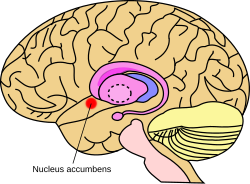 Arvioitu ydin accumbensin sijainti aivoissa
| |
 Hiiren aivojen ytimet
| |
| Yksityiskohdat | |
| Osa |
Mesolimbiseen basaaliganglioissa ( Vatsanpuoleisen striatumissa ) |
| Osat | Nucleus accumbens -kuori Nucleus accumbens -ydin |
| Tunnisteet | |
| latinan kieli | ydin accumbens septi |
| Lyhenteet | NAc tai NAcc |
| MeSH | D009714 |
| NeuroNames | 277 |
| NeuroLex -tunnus | birnlex_727 |
| TA98 | A14.1.09.440 |
| TA2 | 5558 |
| FMA | 61889 |
| Neuroanatomian anatomiset termit | |
Tumakkeen ( NAc tai NACC ; tunnetaan myös accumbensiin ydin , tai aiemmin kuin accumbens-tumakkeen septi , Latinalaisen varten " ydin vieressä väliseinän ") on alue etuaivojen rostraalisen on preoptinen alue on hypotalamuksen . Ydin accumbens ja haju tuberkuli muodostavat yhdessä ventraalisen striatumin . Vatsakalvon ja selkärangan muodostavat yhdessä striatumin , joka onbasaaliset ganglionit . Dopaminergisten neuronien on mesolimbiseen hankkeen päälle GABAergisillä keskipitkällä piikkinen neuronien Nucleus accumbens -alueen ja hajunystyrässä. Jokaisella aivopuoliskolla on oma ydin accumbens, joka voidaan jakaa kahteen rakenteeseen: nucleus accumbens -ydin ja ydin accumbens -kuori. Näillä alarakenteilla on erilainen morfologia ja toiminnot.
Eri NAcc-alialueet (ydin vs kuori) ja neuronien alipopulaatiot kullakin alueella ( D1-tyypin vs D2-tyypin keskipitkät piikkisolut) ovat vastuussa erilaisista kognitiivisista toiminnoista . Kaiken kaikkiaan ytimellä accumbens on merkittävä rooli motivaation , vastenmielisyyden , palkkion (eli kannustavan huomion , nautinnon ja positiivisen vahvistumisen ) kognitiivisessa prosessoinnissa ja vahvistavan oppimisen (esim. Pavlovialainen instrumentaalinen siirto ); siksi sillä on merkittävä rooli riippuvuudessa . Lisäksi osa ytimen accumbens-ytimestä on keskitetysti mukana hitaan aallon indusoimisessa . Ydin accumbensilla on pienempi rooli pelon (vastenmielisyyden), impulsiivisuuden ja lumelääkkeen käsittelyssä . Se on mukana myös uusien moottoriohjelmien koodauksessa .
Rakenne
Ydin accumbens on neuronien yhdistelmä, jonka kuvataan sisältävän ulkokuoren ja sisemmän ytimen.
Syöttö
Merkittävä glutamatergisen panoksia accumbens-tumakkeessa ovat etuaivokuoren (erityisesti prelimbic aivokuori ja infralimbic aivokuori ), basolateraalinen amygdala , vatsa- hippokampuksessa , talamuksen ytimet (erityisesti keskiviivan talamuksen ytimet ja lamellien sisäisten ytimet talamuksen ), ja glutamatergisen ennusteet ventraalisen tegmental alueella (VTA). Ydin accumbens vastaanottaa dopaminergisiä tuloja ventraaliselta tegmental -alueelta, jotka yhdistyvät mesolimbisen reitin kautta . Ydin accumbens kuvataan usein osana aivokalvon-basaalisen ganglion-thalamo-aivokuoren silmukkaa .
VTA: n dopaminergiset tulot moduloivat GABAergisten neuronien toimintaa ytimen ytimessä. Nämä hermosolut aktivoituvat suoraan tai epäsuorasti euforisilla lääkkeillä (esim. Amfetamiini , opiaatit jne.) Ja osallistumalla palkitseviin kokemuksiin (esim. Seksi, musiikki, liikunta jne.).
Toinen merkittävä lähde panos tulee CA1 ja ventraalinen subiculum että hippokampuksen on dorsomedial alueen accumbens-tumakkeessa. Solujen lievä depolarisaatio ytimen accumbensissa korreloi hippokampuksen neuronien positiivisuuden kanssa, mikä tekee niistä kiihottavampia. Näiden jännittyneiden tilojen korreloidut solut keskipitkien piikkien neuronien ytimessä accumbensissa jaetaan tasaisesti subiculumin ja CA1: n kesken. Subiculum -neuronien havaitaan hyperpolarisoituvan (lisäävän negatiivisuutta), kun taas CA1 -neuronit "aaltoilevat" (tuli> 50 Hz) tämän alukkeen aikaansaamiseksi.
Ydin accumbens on yksi harvoista alueista, jotka saavat histaminergisiä projektioita tuberomammillary -ytimestä (ainoa histamiinin neuronien lähde aivoissa).
Lähtö
Lähtö neuronien accumbens-tumakkeessa lähettää aksonaalisessa ulokkeet on basaaliganglioiden ja vatsanpuoleinen analogi linssitumakkeen pallo , joka tunnetaan nimellä ventraalinen pallidum (VP). VP puolestaan projisoi dorsaalisen talamuksen mediaaliseen dorsaaliseen ytimeen , joka heijastuu prefrontaaliseen kuoreen sekä takaisin vatsan ja selkä striatumiin . Muut, kun vievät päässä accumbens-tumakkeessa ovat yhteydet hännän vatsanpuoleisen tegmentaalialueeseen , substantia nigra ja aivoverkostossa ja aivosillan .
Kuori
Nucleus accumbens kuori ( NACC kuori ) on alusrakenne tumakkeessa. Kuori ja ydin muodostavat yhdessä koko ytimen.
Sijainti: Kuori on ytimen accumbensin uloin alue, ja - toisin kuin ydin - sen katsotaan olevan osa laajennettua amygdalaa , joka sijaitsee sen rostraalinapalla.
Solutyypit: Ytimen accumbensin neuronit ovat enimmäkseen keskikokoisia neuroneja (MSN), jotka sisältävät pääasiassa D1-tyypin (eli DRD1 ja DRD5 ) tai D2-tyypin (eli DRD2 , DRD3 ja DRD4 ) dopamiinireseptoreita . MSN: ien alaryhmä sisältää sekä D1-tyypin että D2-tyypin reseptoreita, ja noin 40% striataalisista MSN: istä ilmentää sekä DRD1- että DRD2- mRNA: ta. Nämä sekatyyppiset NAcc MSN: t, joissa on sekä D1- että D2-tyyppisiä reseptoreita, rajoittuvat enimmäkseen NAcc-kuoreen. Kuoren neuroneilla on ytimeen verrattuna pienempi dendriittisten selkärankojen tiheys , vähemmän terminaalisegmenttejä ja vähemmän haarasegmenttejä kuin ytimessä. Kuoren neuronit ulottuvat ventral pallidumin subcommissural -osaan sekä ventral tegmental -alueelle ja laajoille alueille hypotalamuksessa ja laajennetussa amygdalassa.
Tehtävä: Ytimen accumbensin kuori osallistuu palkinnon kognitiiviseen käsittelyyn , mukaan lukien subjektiiviset "mieltymys" -reaktiot tiettyihin miellyttäviin ärsykkeisiin , motivoiva huomio ja positiivinen vahvistuminen . Tämän NAcc-kuoren on myös osoitettu välittävän tiettyä Pavlovian-instrumentaalista siirtoa , ilmiötä, jossa klassisesti ehdollinen ärsyke muuttaa operatiivista käyttäytymistä . "Hedoninen hotspot" tai huvikeskus, joka vastaa joidenkin luontaisten palkintojen miellyttävästä tai "miellyttävästä" komponentista, sijaitsee myös pienessä osastossa NAcc -kuoren keskellä. Riippuvuutta aiheuttavilla lääkkeillä on suurempi vaikutus kuoren dopamiinin vapautumiseen kuin ytimessä.
Ydin
Nucleus accumbens ydin ( NACC ydin ) on sisempi alusrakenteeseen accumbens-tumakkeessa.
Sijainti: Ydin accumbensin ydin on osa ventraalista striatumia , joka sijaitsee basaalisten ganglionien sisällä. Solutyypit: NAcc : n ydin koostuu pääasiassa keskikokoisista neuroneista, jotka sisältävät pääasiassa D1- tai D2-tyypin dopamiinireseptoreita. D1-tyypin keskipitkät piikkiset neuronit välittävät palkitsemiseen liittyviä kognitiivisia prosesseja, kun taas D2-tyypin keskikokoiset piikkisolut välittävät vastenmielisyyteen liittyvää kognitiota. Ytimen neuroneilla, verrattuna kuoren neuroneihin, on lisääntynyt dendriittisten selkärankojen, haarasegmenttien ja terminaalisegmenttien tiheys. Neuronit ulottuvat ytimestä muihin aivokuoren alueisiin, kuten globus pallidus ja substantia nigra. GABA on yksi NAcc: n tärkeimmistä välittäjäaineista, ja myös GABA -reseptoreita on runsaasti.
Tehtävä: Ydin accumbensin ydin on mukana motorisen toiminnan kognitiivisessa prosessoinnissa, joka liittyy palkitsemiseen ja vahvistamiseen sekä hitaan aallon säätelyyn . Erityisesti ydin koodaa uusia moottoriohjelmia, jotka helpottavat tietyn palkinnon hankkimista tulevaisuudessa. Epäsuora reitti (eli D2-tyypin) neuronit NAcc-ytimessä, jotka ilmentävät yhdessä adenosiini A 2A -reseptorien aktivaatiota, edistävät riippuvasti hitaasta unesta. NAcc-ytimen on myös osoitettu välittävän yleistä Pavlovin-instrumentaalista siirtoa , ilmiötä, jossa klassisesti ehdollinen ärsyke muuttaa operatiivista käyttäytymistä.
Solutyypit
Noin 95% NAcc: n neuroneista on GABAergic medium spiny neuroneja (MSN), jotka pääasiassa ilmentävät joko D1- tai D2-tyyppisiä reseptoreita; noin 1-2% jäljellä hermosolujen tyypit ovat suuria aspiny kolinergisiä interneuroneista ja toinen 1-2% ovat GABAergisten interneuroneista. Verrattuna kuoren GABAergic -MSN: iin, ytimessä olevilla on lisääntynyt dendriittisten piikien, haarasegmenttien ja terminaalisegmenttien tiheys. Neuronit ulottuvat ytimestä muihin aivokuoren alueisiin, kuten globus pallidus ja substantia nigra. GABA on yksi NAcc: n tärkeimmistä välittäjäaineista, ja myös GABA -reseptoreita on runsaasti. Nämä neuronit ovat myös ytimen accumbensin tärkeimmät projektio- tai lähtöneuronit.
Neurokemia
Jotkut välittäjäaineista, neuromodulaattoreista ja hormoneista, jotka signaloivat ytimen accumbens -reseptoreiden kautta, ovat:
Dopamiini : Dopamiini vapautuu ytimeen accumbens altistettuna palkitseville ärsykkeille , mukaan lukien virkistyslääkkeet, kuten korvatut amfetamiinit , kokaiini , nikotiini ja morfiini .
Fenetyyliamiini ja tyramiini : fenetyyliamiini ja tyramiini ovat jäljittää amiinit , jotka syntetisoidaan hermosoluissa, jotka ilmentävät aromaattinen aminohappo hydroksylaasi (AADC) entsyymi , joka sisältää kaikki dopaminergisten neuronien. Molemmat yhdisteet toimivat dopaminergisten neuromodulaattoreina jotka säätelevät takaisinoton ja dopamiinin vapautumista NACC kautta vuorovaikutus VMAT2 ja TAAR1 on Axon päätelaite mesolimbisen dopamiini neuronien.
Glukokortikoidit ja dopamiini: Glukokortikoidireseptorit ovat ainoat kortikosteroidireseptorit ytimen accumbens -kuoressa. L-DOPA: n , steroidien ja erityisesti glukokortikoidien tiedetään tällä hetkellä olevan ainoat tunnetut endogeeniset yhdisteet, jotka voivat aiheuttaa psykoottisia ongelmia, joten dopamiinergisten projektioiden hormonaalisen hallinnan ymmärtäminen glukokortikoidireseptoreiden suhteen voi johtaa uusiin psykoottisten oireiden hoitoihin. Äskettäinen tutkimus osoitti, että glukokortikoidireseptorien tukahduttaminen johti dopamiinin vapautumisen vähenemiseen, mikä voi johtaa tulevaisuudessa glukokortikoidilääkkeiden tutkimukseen psykoottisten oireiden lievittämiseksi.
GABA: Tuore tutkimus rotilla, että käytetyt GABA-agonistit ja antagonistit osoittivat, että GABA reseptoreihin NACC kuori on inhiboiva valvonnan kääntämällä käyttäytymiseen vaikuttavat dopamiini, ja GABA B -reseptoreihin on inhiboiva hallita kiertämällä käyttäytyminen välittämien asetyylikoliinin .
Glutamaatti : Tutkimukset ovat osoittaneet, että glutamatergisten NMDA -reseptorien paikallinen estoNAcc -ytimessä heikensi spatiaalista oppimista. Toinen tutkimus osoitti, että sekä NMDA: lla että AMPA: lla (molemmat glutamaattireseptorit ) on tärkeä rooli instrumentaalisen oppimisen säätelyssä.
Serotoniini (5-HT): Kaiken kaikkiaan 5-HT-synapsit ovat runsaampia ja niillä on enemmän synaptisia kontakteja NAcc-kuorissa kuin ytimessä. Ne ovat myös suurempia ja paksumpia ja sisältävät enemmän suuria tiheitä ydinvesikkeleitä kuin niiden ytimessä olevat vastapuolet.
Toiminto
Palkinto ja vahvistus
Ydin accumbens on osa palkitsemisjärjestelmää ja sillä on tärkeä rooli palkitsevien ärsykkeiden, vahvistavien ärsykkeiden (esim. Ruoka ja vesi) sekä palkitsevien ja vahvistavien (riippuvuutta aiheuttavat lääkkeet, seksi ja liikunta) käsittelyssä. Hallitseva reaktio neuronien tumakkeessa, että palkkio sakkaroosi on esto; päinvastoin on vastaus vastenmielisen kiniinin antamiseen . Farmakologisesta manipuloinnista saadut merkittävät todisteet viittaavat myös siihen, että hermosolujen hermostuneisuuden vähentäminen ytimen ytimessä on palkitsevaa, kuten esimerkiksi μ-opioidireseptorin stimulaation tapauksessa. Veren happipitoisuus riippuvaisen signaalin (lihavoitu) nucleus accumbens -alueen selektiivisesti kasvoi käsitys miellyttävää, emotionaalisesti herättää kuvia ja aikana mielikuvitukseen miellyttävä, emotionaalinen kohtauksia. Kuitenkin, koska BOLDin uskotaan olevan epäsuora mitta alueelliselle nettosäteilylle inhibitioon, ei tiedetä, missä määrin BOLD mittaa valenssista riippuvaista käsittelyä. Koska NAcc -tuloja on runsaasti limbisiltä alueilta ja voimakkaita NAcc -ulostuloja moottorialueille, Gordon Mogensen on kuvannut ytimen accumbensin limbisen ja moottorijärjestelmän välisenä rajapintana.

Ydin accumbens liittyy kausaalisesti nautinnon kokemukseen. Mikroinjektiot μ-opioidiagonisteista, δ-opioidiagonisteista tai κ-opioidiagonisteista mediaalikuoren rostrodorsaalisessa neljänneksessä lisäävät "tykkäämistä", kun taas enemmän kaudaalisia injektioita voivat estää inhoamisreaktioita, tykkäysreaktioita tai molempia. Niiden ytimen alueet, joille voidaan katsoa syy -seuraus nautinnon tuottamisessa, ovat rajalliset sekä anatomisesti että kemiallisesti, koska opioidiagonistien lisäksi vain endokannabinoidit voivat parantaa mieltymystä. Koko ytimessä dopamiini, GABA -reseptorin agonisti tai AMPA -antagonistit muuttavat vain motivaatiota, kun taas sama pätee opioideihin ja endokannabinoideihin hotspotin ulkopuolella mediaalikuorissa. On olemassa rostro-kaudaalinen gradientti, joka parantaa ruokahalua vastaan pelottavia vastauksia, joista jälkimmäisen uskotaan perinteisesti edellyttävän vain D1-reseptoritoimintoa ja joista ensimmäinen vaatii sekä D1- että D2-toimintoa. Tämän tulkinnan yksi tulkinta, estävä hypoteesi, osoittaa, että accumbens -MSN: ien (jotka ovat GABAergisiä) esto estää alavirtarakenteita, mikä mahdollistaa ruokahaluisen tai kuluttavan käyttäytymisen ilmaisemisen. AMPA -antagonistien ja vähemmässä määrin GABA -agonistien motivoivat vaikutukset ovat anatomisesti joustavia. Stressaavat olosuhteet voivat laajentaa pelkoa aiheuttavia alueita, kun taas tuttu ympäristö voi pienentää pelkoa aiheuttavan alueen kokoa. Lisäksi aivokuoren panos orbitofrontal cortexista (OFC) esijännittää vasteen ruokahaluiseen käyttäytymiseen, ja infralimbic input, joka vastaa ihmisen subgenual cingulate cortexia, estää vasteen valenssista riippumatta.
Ydin accumbens ei ole välttämätön eikä riittävä instrumentaaliseen oppimiseen, vaikka manipulaatiot voivat vaikuttaa instrumentaalisten oppimistehtävien suorittamiseen. Yksi tehtävä, jossa NAcc-leesioiden vaikutus on ilmeinen, on Pavlovian-instrumentaalinen siirto (PIT), jossa vihje, joka on yhdistetty tiettyyn tai yleiseen palkkioon, voi parantaa instrumentaalista vastetta. Vauriot NAcc: n ytimeen heikentävät suorituskykyä devalvaation jälkeen ja estävät yleisen PIT: n vaikutusta. Toisaalta kuoren vauriot heikentävät vain tietyn PIT: n vaikutusta. Tämän eron uskotaan heijastavan NAcc -kuoren ja NAcc -ytimen kuluttavia ja ruokahaluisia ehdollisia vastauksia.
Selän striatumissa on havaittu kaksijakoisuus D1-MSN: ien ja D2-MSN: ien välillä, ja ensimmäinen on vahvistanut ja tehostanut liikkuvuutta, ja jälkimmäinen on vastenmielistä ja vähentävää liikkumista. Tällaisen eron on perinteisesti oletettu pätevän myös ydin accumbensiin, mutta farmakologisten ja optogenetiikan tutkimusten todisteet ovat ristiriitaisia. Lisäksi osa NAcc -MSN: istä ilmentää sekä D1- että D2 -MSN: iä, eikä D1 -reseptorien farmakologisen aktivoinnin vs. D2 -reseptorien tarvitse välttämättä aktivoida hermopopulaatioita täsmälleen. Vaikka useimmat tutkimukset eivät osoita D1- tai D2-MSN: ien selektiivisen optogeneettisen stimulaation vaikutusta liikkumisaktiivisuuteen, yksi tutkimus on raportoinut perustoiminnan vähenemisestä D2-MSN-stimulaation kanssa. Vaikka kahdessa tutkimuksessa on raportoitu kokaiinin heikentyneistä vahvistavista vaikutuksista D2-MSN-aktivaation kanssa, yhdessä tutkimuksessa ei ole raportoitu vaikutusta. NAcc D2-MSN -aktivaation on myös raportoitu parantavan motivaatiota PIT: n arvioimana, ja D2-reseptorin aktiivisuus on välttämätön VTA-stimulaation vahvistavien vaikutusten kannalta. Vuonna 2018 tehdyssä tutkimuksessa raportoitiin, että D2 MSN: n aktivaatio lisäsi motivaatiota estämällä ventral pallidumia estäen siten VTA: n.
Äidin käyttäytyminen
Vuonna 2005 tehdyssä fMRI -tutkimuksessa havaittiin, että kun äiti -rotat olivat pentujensa läsnä, vahvistamiseen osallistuneet aivojen alueet, mukaan lukien ydin accumbens, olivat erittäin aktiivisia. Dopamiinitasot lisääntyvät ytimen accumbensissa äidin käyttäytymisen aikana, kun taas leesiot tällä alueella häiritsevät äidin käyttäytymistä. Kun naisille esitetään kuvia etuyhteydettömistä imeväisistä, fMRI -tutkimukset osoittavat lisääntyneen aivotoiminnan ytimessä ytimessä ja viereisessä caudate -ytimessä suhteessa siihen, missä määrin naiset pitävät näitä pikkulapsia "söpöinä".
Vastenmielisyys
D1-tyyppisten MSN: ien aktivointi ytimen accumbensissa liittyy palkitsemiseen, kun taas D2-tyypin MSN: ien aktivointi ytimen accumbensissa edistää vastenmielisyyttä .
Hidas aaltoilu
Loppuvuodesta 2017 optogeneettisiä ja kemogeneettisiä menetelmiä hyödyntäneissä jyrsijöissä tehdyissä tutkimuksissa havaittiin, että epäsuora reitti (eli D2-tyypin) keskipitkät piikkiset neuronit ytimen accumbens-ytimessä, jotka ilmentävät yhdessä adenosiini A 2A -reseptoreita ja heijastavat vatsakalvon, ovat mukana hitaan aallon säätely . Erityisesti näiden epäsuoran reitin NAcc-ydinneuronien optogeneettinen aktivointi indusoi hitaan aallon unen ja samojen neuronien kemogeneettinen aktivaatio lisää hitaiden aaltojaksojen määrää ja kestoa. Näiden NAcc -ydinneuronien kemogeneettinen esto tukahduttaa unen. Sitä vastoin adenosiini A 2A -reseptoreita ilmentävillä D2-tyypin keskikokoisilla neuroneilla NAcc-kuorella ei ole mitään roolia hitausaallon säätelyssä.
Lääketieteellinen merkitys
Riippuvuus
Nykyiset mallit riippuvuuden kroonisesta huumeiden käytöstä liittyy muutoksia geenien ilmentyminen on mesokortikolimbisiä projektio . Tärkeimmät transkriptiotekijät, jotka aiheuttavat nämä muutokset, ovat ΔFosB , syklisen adenosiinimonofosfaatin ( cAMP ) vaste -elementtiä sitova proteiini ( CREB ) ja ydintekijä kappa B ( NFκB ). ΔFosB on merkittävin geenin transkriptiotekijä riippuvuudessa, koska sen virus- tai geneettinen yliakspressio ytimessä ytimessä on välttämätöntä ja riittävää monille hermosopeutumisille ja käyttäytymisvaikutuksille (esim. Ilmentymisestä riippuvainen lisääntyminen itsehallinnossa ja palkitseminen ) huumeriippuvuus. ΔFosB: n yliekspressio on liittynyt muun muassa alkoholiriippuvuuteen (etanoli) , kannabinoideihin , kokaiiniin , metyylifenidaattiin , nikotiiniin , opioideihin , fensyklidiiniin , propofoliin ja substituoituihin amfetamiiniin . Ytimen accumbensin ΔJunD -ilmentymisen lisääntyminen voi vähentää tai suurella kasvulla jopa estää useimmat kroonisessa huumeidenkäytössä havaitut hermomuutokset (ts. ΔFosB: n välittämät muutokset).
ΔFosB: llä on myös tärkeä rooli säätelemällä käyttäytymisvasteita luonnollisiin palkintoihin, kuten maukasta ruokaa, seksiä ja liikuntaa. Luonnolliset palkinnot, kuten väärinkäytön lääkkeet, indusoivat ΔFosB: tä ytimessä, ja näiden palkintojen krooninen hankkiminen voi johtaa samanlaiseen patologiseen riippuvuutta aiheuttavaan tilaan ΔFosB -yliekspression kautta. Näin ollen ΔFosB on keskeinen transkriptiotekijä, joka liittyy myös riippuvuuksiin luonnollisista palkkioista; erityisesti ΔFosB ytimessä accumbens on kriittinen seksuaalisen palkkion vahvistavien vaikutusten kannalta. Luonnollisten ja lääkepalkkioiden välisen vuorovaikutuksen tutkimus viittaa siihen, että psykostimulantit ja seksuaalinen käyttäytyminen vaikuttavat samanlaisiin biomolekyylimekanismeihin indusoidakseen ΔFosB: n ytimessä ytimessä ja niillä on ristiinherkistäviä vaikutuksia, jotka välittyvät ΔFosB: n kautta.
Samoin kuin lääkepalkinnot, ei-lääkkeelliset palkinnot lisäävät myös solunulkoisen dopamiinin määrää NAcc-kuorissa. Huumeiden aiheuttama dopamiinin vapautuminen NAcc-kuorissa ja NAcc-ytimessä ei yleensä ole altis tottumiselle (eli lääkkeen sietokyvyn kehittyminen : dopamiinin vapautumisen väheneminen tulevasta lääkeainealtistuksesta johtuen toistuvasta lääkeainealtistuksesta); päinvastoin, toistuva altistuminen lääkkeille, jotka indusoivat dopamiinin vapautumista NAcc -kuoreen ja ytimeen, johtaa tyypillisesti herkistymiseen (eli dopamiinin määrä, joka vapautuu NAcc: ssa tulevasta lääkeainealtistuksesta, kasvaa toistuvan lääkeainealtistuksen seurauksena). Dopamiinin vapautumisen herkistäminen NAcc-kuoressa toistuvan lääkeainealtistuksen jälkeen vahvistaa ärsyke-lääkeyhdistyksiä (eli klassista hoitoa, joka tapahtuu, kun huumeiden käyttö yhdistetään toistuvasti ympäristön ärsykkeisiin), ja nämä yhdisteet tulevat vähemmän alttiiksi sukupuuttoon (eli "oppimattomuudelle") nämä klassisesti ehdolliset yhteydet huumeiden käytön ja ympäristön ärsykkeiden välillä vaikeutuvat). Toistuvien pariliitosten muodostamisen jälkeen näistä klassisesti ehdollisista ympäristöärsykkeistä (esim. Konteksteista ja esineistä, jotka yhdistetään usein huumeidenkäyttöön) tulee usein huumeiden vihjeitä, jotka toimivat huumeiden käytön toissijaisina vahvistimina (eli kun nämä yhdistykset on muodostettu, altistuminen parilliselle ympäristön ärsykkeelle) herättää halun tai halun käyttää lääkettä, johon he ovat liittyneet ).
Toisin kuin lääkkeet, dopamiinin vapautuminen NAcc-kuoreen monentyyppisten palkitsevien ei-lääkkeellisten ärsykkeiden tyypillisesti tottuu toistuvan altistumisen jälkeen (eli dopamiinin määrä, joka vapautuu tulevasta altistumisesta palkitsevalle ei-lääkkeelliselle ärsykkeelle, yleensä pienenee ärsykkeen toistuvan altistumisen seurauksena).
| Muoto neuroplasticity tai käyttäytymiseen plastisuus |
Tyyppinen vahvistajana | Lähteet | |||||
|---|---|---|---|---|---|---|---|
| Opiaatit | Psykostimulantit | Rasvainen tai sokerinen ruoka | Seksuaalinen kanssakäyminen |
Liikunta (aerobinen) |
Ympäristön rikastaminen |
||
|
ΔFosB- ilmentyminen ytimessä accumbens D1-tyypin MSN: issä |
↑ | ↑ | ↑ | ↑ | ↑ | ↑ | |
| Käyttäytymisen plastisuus | |||||||
| Saannin lisääntyminen | Joo | Joo | Joo | ||||
| Psykostimulanttien ristiherkistyminen |
Joo | Ei sovellettavissa | Joo | Joo | Vaimennettu | Vaimennettu | |
| Psykostimulantti itsehallinto |
↑ | ↑ | ↓ | ↓ | ↓ | ||
| Psykostimulantti ehdollinen paikka |
↑ | ↑ | ↓ | ↑ | ↓ | ↑ | |
| Huumeidenkäyttäytymisen palauttaminen | ↑ | ↑ | ↓ | ↓ | |||
| Neurokemiallinen plastisuus | |||||||
|
CREB fosforylaatio on makaavassa tumakkeessa |
↓ | ↓ | ↓ | ↓ | ↓ | ||
| Herkistettyjä dopamiinin vastaus on makaavassa tumakkeessa |
Ei | Joo | Ei | Joo | |||
| Muutettu striatalin dopamiinin signalointi | ↓ DRD2 , ↑ DRD3 | ↑ DRD1 , ↓ DRD2 , ↑ DRD3 | ↑ DRD1 , ↓ DRD2 , ↑ DRD3 | ↑ DRD2 | ↑ DRD2 | ||
| Muutettu striatalin opioidisignaali | Ei muutoksia tai ↑ μ-opioidireseptoreita |
↑ μ-opioidireseptorit ↑ κ-opioidireseptorit |
↑ μ-opioidireseptorit | ↑ μ-opioidireseptorit | Ei muutosta | Ei muutosta | |
| Muutokset striatalin opioidipeptideissä | ↑ dynorfiini Ei muutosta: enkefaliini |
↑ dynorfiini | ↓ enkefaliini | ↑ dynorfiini | ↑ dynorfiini | ||
| Mesokortikolimbinen synaptinen plastisuus | |||||||
| Lukumäärä dendriittien on makaavassa tumakkeessa | ↓ | ↑ | ↑ | ||||
|
Dendriittiokasten tiheys makaavassa tumakkeessa |
↓ | ↑ | ↑ | ||||
Masennus
Huhtikuussa 2007 kaksi tutkimusryhmää ilmoitti asettaneensa elektrodit ytimen ytimeen syvän aivostimulaation käyttämiseksi vakavan masennuksen hoitoon . Vuonna 2010 kokeet raportoivat, että ytimen syvä aivostimulaatio onnistui vähentämään masennusoireita 50%: lla potilaista, jotka eivät vastanneet muihin hoitoihin, kuten sähkökonvulsiiviseen hoitoon . Nucleus accumbensia on myös käytetty kohteena hoidettaessa pieniä potilasryhmiä, joilla on hoito-refraktorinen pakko-oireinen häiriö.
Ablaatio
Riippuvuuden hoitoon ja mielisairauksien hoitoon on suoritettu ytimen accumbensin radiotaajuinen ablaatio . Tulokset ovat epäselviä ja kiistanalaisia.
Lumelääkevaikutus
NAcc: n aktivoitumisen on osoitettu tapahtuvan odottaessaan lääkkeen tehokkuutta, kun käyttäjälle annetaan lumelääkettä , mikä osoittaa, että ydin accumbens vaikuttaa rokotteeseen lumelääkkeessä .
Lisäkuvia
Katso myös
Viitteet
Ulkoiset linkit
- Ydin accumbensin rooli palkitsemispiirissä. Osa "Aivot ylhäältä alas". osoitteessa thebrain.mcgill.ca
- Nucleus Accumbens - solukeskinen tietokanta
- Mosaiikki aivoviipaleviljelmien kuvia, jotka ovat "ydin% 20accumbens" on BrainMaps hanke