RNA: n aiheuttama äänenvaimennuskompleksi - RNA-induced silencing complex
RNA-indusoitu vaimentamiskompleksiin , tai RISC , on moniproteiinikompleksin , nimenomaan ribonukleoproteiini , joka toimii geeninhiljentämistä kautta eri reittejä on transkription ja translaation tasolla. Käyttämällä yksijuosteisia RNA (ssRNA) -fragmentteja, kuten mikroRNA: ta (miRNA) tai kaksijuosteista pientä häiritsevää RNA: ta (siRNA), kompleksi toimii keskeisenä työkaluna geenisäätelyssä. RNA: n yksittäinen juoste toimii mallina RISC: lle tunnistamaan komplementaarinen lähetti -RNA (mRNA) -transkripti . Kun löydetty, yksi RISC: n proteiineista, Argonaute , aktivoi ja katkaisee mRNA: n. Tätä prosessia kutsutaan RNA -häiriöksi (RNAi) ja sitä esiintyy monissa eukaryooteissa ; se on keskeinen prosessi puolustautumisessa virusinfektioita vastaan , koska sen laukaisee kaksijuosteinen RNA (dsRNA).
Löytö
Biokemiallinen tunnistaminen RISC suoritettiin Gregory Hannon ja hänen kollegansa Cold Spring Harbor Laboratory . Tämä oli vain pari vuotta sen jälkeen, kun Andrew Fire ja Craig Mello , jotka jakoivat vuoden 2006 fysiologian tai lääketieteen Nobelin palkinnon, havaitsivat RNA -häiriön vuonna 1998 .
Hannon ja hänen kollegansa yrittivät tunnistaa RNAi -mekanismit, jotka liittyvät geenien vaimentamiseen dsRNA: iden avulla Drosophila -soluissa. Drosophila S2 -solut oli transfektoitu kanssa lacZ- ekspressiovektori määrällisesti geenin ilmentymisen kanssa β-galaktosidaasin aktiivisuus. Niiden tulokset osoittivat, että rinnakkaisinfektio lacZ dsRNA: n kanssa vähensi merkittävästi β-galaktosidaasin aktiivisuutta verrattuna kontrollin dsRNA: han. Siksi dsRNA: t kontrolloivat geeniekspressiota sekvenssin komplementaarisuuden kautta .
S2 -solut transfektoitiin sitten Drosophila cyclin E dsRNA: lla. Sykliini E on olennainen geeni solusyklin etenemiseen S -vaiheeseen . Sykliini E dsRNA pidätettiin solusyklin on G 1 vaihe (ennen S-vaiheessa). Siksi RNAi voi kohdistaa endogeenisiin geeneihin.
Lisäksi sykliini E dsRNA vain vähentynyt sykliini E RNA - samanlainen tulos näytetään myös dsRNA: ta, joka vastaa sykliini A: joka toimii S, G 2 ja M vaiheiden solusyklin. Tämä osoittaa RNAi: n tunnusomaisen tunnusmerkin: alennetut mRNA -tasot vastaavat lisätyn dsRNA: n tasoja.
Testatakseen, johtuiko heidän havaittujen alentuneiden mRNA -tasojensa seurauksena mRNA: n kohdistamisesta suoraan (kuten muiden järjestelmien tiedot viittaavat ), Drosophila S2 -solut transfektoitiin joko Drosophila cyclin E dsRNA: lla tai lacZ dsRNA: lla ja inkuboitiin sitten sykliini E: n synteettisten mRNA: iden kanssa tai lacZ .
Sykliini E dsRNA: lla transfektoidut solut osoittivat vain hajoamista sykliini E -transkripteissä - lacZ -transkriptit olivat stabiileja. Päinvastoin, lacZ dsRNA: lla transfektoidut solut osoittivat hajoamista vain lacZ -transkripteissä eivätkä sykliini E -transkripteissä. Niiden tulokset saivat Hannonin ja hänen kollegansa ehdottamaan, että RNAi hajottaa kohde-mRNA: ta "sekvenssispesifisen nukleaasiaktiivisuuden " kautta. Ne kutsutaan nukleaasi entsyymi RISC.
Toiminta RNA -häiriöissä
SiRNA/miRNA: n sisällyttäminen
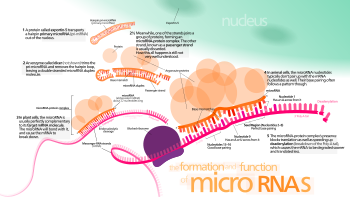
RNaasi III Dicer on kriittinen jäsen RISC, joka aloittaa RNA-interferenssiä tuottamalla kaksijuosteisen siRNA tai yksijuosteista miRNA. DsRNA: n entsymaattinen pilkkominen solun sisällä tuottaa lyhyitä siRNA-fragmentteja, joiden pituus on 21-23 nukleotidia ja joissa on kahden nukleotidin 3 ' uloke. Dicer käsittelee samalla tavalla myös pre-miRNA: ta, joka muodostaa hiusneulalenkin rakenteen jäljittelemään dsRNA: ta. dsRNA -fragmentit ladataan RISC: hen, ja jokaisella juosteella on erilainen kohtalo epäsymmetrisääntöilmiön perusteella, jolloin yksi juoste valitaan opas juosteeksi toisen suhteen termodynaamisen vakauden perusteella. Äskettäin luotu miRNA tai siRNA toimivat yksijuosteisina ohjaussekvensseinä RISC: lle kohdistamaan mRNA: ta hajoamista varten.
- Säike, jolla on vähemmän termodynaamisesti vakaa 5' -pää, valitaan Argonaute -proteiinilla ja integroidaan RISC: hen. Tämä juoste tunnetaan ohjaavana juosteena ja kohdistaa mRNA: n hajoamiseen.
- RISC heikentää toista osa -aluetta, joka tunnetaan matkustajaosana.
Geenien säätely
RISC: n, Ago2: n, SND1: n ja AEG-1: n tärkeimmät proteiinit toimivat ratkaisevasti tekijöinä kompleksin geeninvaimennustoiminnassa.
RISC käyttää miRNA: n tai siRNA: n ohjainlankaa kohdistaakseen mRNA-transkriptien komplementaariset 3'-kääntämättömät alueet (3'UTR) Watson-Crick-emäsparin kautta , jolloin se voi säätää mRNA-transkriptin geeniekspressiota useilla tavoilla.
mRNA: n hajoaminen
RISC: n ymmärrettävin tehtävä on kohde -mRNA: n hajoaminen, mikä vähentää transkriptitasoja, joita ribosomit voivat kääntää . RISC: n ohjauslankaa komplementaarisen mRNA: n endonukleolyyttinen katkaisu Argonaute -proteiinilla on avain RNAi: n aloittamiseen. MRNA: n hajoamiselle on kaksi päävaatimusta:
- lähes täydentävä vastaavuus ohjainlangan ja kohde-mRNA-sekvenssin välillä, ja
- katalyyttisesti aktiivinen Argonaute -proteiini, jota kutsutaan "viipaloijaksi" kohde -mRNA: n katkaisemiseksi.
MRNA: n hajoamisella on kaksi pääreittiä katkaisun jälkeen. Molemmat aloitetaan mRNA: n poly (A) hännän hajoamisen seurauksena , mikä johtaa mRNA: n 5' -korkin poistamiseen.
- 5'-to-3' hajoamista transkriptin tapahtuu XRN1 eksonukle- on sytoplasman elimiä, P-elimet .
- Transkriptin 3'-5'-hajoaminen suoritetaan eksosomilla ja Ski-kompleksilla .
Käännösten sorto
RISC voivat moduloida lastaus ribosomin ja lisävaruste tekijät käännös ja repressoivat ilmentymisen sitoutuneen mRNA-transkripti. Translaation tukahduttaminen vaatii vain osittaisen sekvenssin vastaavuuden ohjainlangan ja kohde -mRNA: n välillä.
Käännöstä voidaan säätää aloitusvaiheessa seuraavasti:
- estää eukaryoottisen translaation aloitustekijän (eIF) sitoutumisen 5' -korkkiin . On havaittu, että RISC voi lopettaa 3' -poly (A) hännän kuoleman, mikä voi edistää tukahduttamista 5' -korkin kautta.
- 60S ribosomaalisen alayksikön sitoutumisen estäminen mRNA: han voi estää translaation.
Käännöstä voidaan säätää aloittamisen jälkeisissä vaiheissa seuraavasti:
- peptidien hajoaminen,
- edistämällä translaation ribosomien ennenaikaista lopettamista tai
- venymä hidastuu.
Vielä spekuloidaan, ovatko translaation tukahduttaminen aloittamisen ja aloittamisen jälkeen toisensa poissulkevat.
Heterokromatiinin muodostuminen
Jotkut RISCs pystyvät suoraan kohdistamaan genomiin rekrytoimalla histoni metyylitransferaasit muodostamiseksi heterokromatiini geeni- lokuksessa , vaientaa geenin. Nämä RISC: t ovat RNA: n indusoiman transkription vaimentavan kompleksin (RITS) muodossa. Paras tutkittu esimerkki on hiiva RITS.
RITS: n on osoitettu ohjaavan heterokromatiinin muodostumista sentromeereillä tunnistamalla sentromeeriset toistot. Yhdistämällä siRNA: n (ohjainlanka) emäspariksi kohdekromatiinisekvensseihin histonimodifioivia entsyymejä voidaan värvätä.
Mekanismia ei ymmärretä hyvin; RITS kuitenkin hajottaa syntyviä mRNA -transkripteja. On ehdotettu, että tämä mekanismi toimii "itseään vahvistavana takaisinkytkentäsilmukana ", koska RNA-riippuvainen RNA-polymeraasi (RdRp) käyttää hajoavia syntyviä transkripteja lisää siRNA: ita varten.
In Schizosaccharomyces pombe ja Arabidopsis , käsittely dsRNA tavoitteet huomioon siRNA Dicer RNaasit voi aloittaa geenin hiljentäminen reitin Hetero- kromatiinin muodostumista. AGG4: nä tunnettu Argonaute -proteiini on vuorovaikutuksessa pienten RNA: iden kanssa, jotka määrittelevät heterokromaattisia sekvenssejä. Histoni metyyli transferaasi (HMT), H3K9 , methylates histonin H3 ja rekrytoi chromodomain proteiinien metylaatiokohtia. DNA -metylaatio ylläpitää geenien vaimentamista, kun heterokromatiinisekvenssit voidaan luoda tai levittää.
DNA: n poistaminen
SiRNA tuottamat RISCs näyttää olevan rooli alentava DNA aikana somaattiset macronucleus kehitystä alkueläinten Tetrahymenan . Se on samanlainen kuin heterokromatiinin muodostumisen epigeneettinen valvonta, ja sen oletetaan puolustavan hyökkääviä geneettisiä elementtejä vastaan.
Samanlainen kuin heterokromatiinin muodostuminen S. pombessa ja Arabidopsisissa , Tetrahymena -proteiini, joka liittyy Argonaute -perheeseen, Twi1p, katalysoi kohdesekvenssien DNA -eliminaation, joka tunnetaan nimellä sisäiset eliminaatiosekvenssit (IES). Metyylitransferaaseja ja kromodomeeniproteiineja käyttämällä IES: t heterokromatisoidaan ja eliminoidaan DNA: sta.
RISC: hen liittyvät proteiinit
RISC: n koko rakenne on edelleen ratkaisematta. Monissa tutkimuksissa on raportoitu erilaisia kokoja ja komponentteja RISC: lle, mutta ei ole täysin varmaa, johtuuko tämä useiden RISC -kompleksien olemassaolosta vai eri tutkimusten eri lähteistä.
| Monimutkainen | Lähde | Tunnetut/ilmeiset komponentit | Arvioitu koko | Näennäinen toiminta RNAi -reitillä |
|---|---|---|---|---|
| Dcr2-R2D2 | D. melanogaster S2 -solut | Dcr2 , R2D2 | ~ 250 kDa | dsRNA -prosessointi, siRNA -sitoutuminen |
| RLC (A) | D. melanogaster -alkioita | Dcr2, R2D2 | NR | dsRNA -prosessointi, siRNA -sitoutuminen, RISC: n esiaste |
| Holo-RISC | D. melanogaster -alkioita | Ago 2 , Dcr1, Dcr2, Fmr1 / Fxr , R2D2, Tsn , Vig | ~ 80S | Kohde-RNA: n sitoutuminen ja katkaisu |
| RISC | D. melanogaster S2 -solut | Ago2, Fmr1/Fxr, Tsn, Vig | ~ 500 kDa | Kohde-RNA: n sitoutuminen ja katkaisu |
| RISC | D. melanogaster S2 -solut | Ago2 | ~ 140 kDa | Kohde-RNA: n sitoutuminen ja katkaisu |
| Fmr1-yhdistelmä | D. melanogaster S2 -solut | L5 , L11 , 5S rRNA , Fmr1/Fxr, Ago2, Dmp68 | NR | Mahdollinen kohde-RNA-sitoutuminen ja katkaisu |
| Minimaalinen RISC | HeLa -solut | eIF2C1 (Ago1) tai eIF2C2 (Ago2) | ~ 160 kDa | Kohde-RNA: n sitoutuminen ja katkaisu |
| miRNP | HeLa -solut | eIF2C2 (ago2), Gemin3 , Gemin4 | ~ 550 kDa | miRNA-assosiaatio, kohde-RNA: n sitoutuminen ja katkaisu |
Ago, Argonaute; Dcr, Dicer; Dmp68, D. melanogaster -ortologi nisäkkään p68 -RNA: n purkamisesta; eIF2C1, eukaryoottisen translaation aloitustekijä 2C1; eIF2C2, eukaryoottisen translaation aloitustekijä 2C2; Fmr1/Fxr, D. hauraan X-henkisen hidastumisen proteiinin melanogaster- ortologi; miRNP, miRNA-proteiinikompleksi; NR, ei ilmoitettu; Tsn, Tudor-stafylokokki-nukleaasi; Vig, vasa intronic -geeni.
Siitä huolimatta on ilmeistä, että Argonaute -proteiineja on läsnä ja ne ovat välttämättömiä toiminnalle. Lisäksi on tietoa joistakin kompleksin avainproteiineista (Argonauten lisäksi), joiden avulla RISC voi suorittaa tehtävänsä.
Argonaute -proteiinit
Argonauttiproteiinit ovat prokaryooteissa ja eukaryooteissa esiintyvien proteiinien perhe . Niiden toiminta prokaryooteissa on tuntematon, mutta eukaryooteissa ne ovat vastuussa RNAi: sta. Ihmisen Argonauteissa on kahdeksan perheenjäsentä, joista vain Argonaute 2 osallistuu yksinomaan kohdennettuun RNA: n pilkkomiseen RISC: ssä.
RISC-latauskompleksi
RISC-latauskompleksi (RLC) on olennainen rakenne, jota tarvitaan dsRNA-fragmenttien lataamiseen RISC: hen mRNA: n kohdentamiseksi. RLC koostuu diceristä, transaktivoivasta vaste-RNA: ta sitovasta proteiinista ( TRBP ) ja Argonaute 2: sta.
- Dicer on RNaasi III -endonukleaasi, joka tuottaa ladattavia dsRNA -fragmentteja, jotka ohjaavat RNAi: ta.
- TRBP on proteiini, jossa on kolme kaksijuosteista RNA: ta sitovaa domeenia .
- Argonaute 2 on RNaasi ja RISC: n katalyyttinen keskus.
Dicer toimii TRBP: n ja Argonaute 2: n kanssa helpottaakseen Dicerin tuottamien dsRNA -fragmenttien siirtoa Argonaute 2: een.
Uusimmat tutkimukset ovat osoittaneet, että ihmisen RNA -helikaasi A voi auttaa helpottamaan RLC: tä.
Muut proteiinit
Äskettäin tunnistetut RISC: n jäsenet ovat SND1 ja MTDH . SND1 ja MTDH ovat onkogeenejä ja säätelevät erilaisia geeniekspressioita.
| Proteiini | Laji, josta proteiini löytyy |
|---|---|
| Dcr1 | D. melanogaster |
| Dcr2 | D. melanogaster |
| R2D2 | D. melanogaster |
| Ago2 | D. melanogaster |
| Dmp68 | D. melanogaster |
| Fmr1/Fxr | D. melanogaster |
| Tsn | D. melanogaster |
| Vig | D. melanogaster |
| Polyribosomit , ribosomikomponentit | D. melanogaster , T. brucei |
| eIF2C1 (Ago1) | H. sapiens |
| eIF2C2 (Ago2) | H. sapiens |
| Gemin 3 | H. sapiens |
| Gemin 4 | H. sapiens |
Ago, Argonaute; Dcr, Dicer; Dmp68, D. melanogaster -ortologi nisäkkään p68 -RNA: n purkamisesta; eIF2C1, eukaryoottisen translaation aloitustekijä 2C1; eIF2C2, eukaryoottisen translaation aloitustekijä 2C2; Fmr1/Fxr, D. hauraan X-henkisen hidastumisen proteiinin melanogaster- ortologi; Tsn, Tudor-stafylokokki-nukleaasi; Vig, vasa intronic -geeni.
MRNA: n sitoutuminen
Vielä on epäselvää, miten aktivoitu RISC -kompleksi paikantaa mRNA -kohteet solussa, vaikka on osoitettu, että prosessi voi tapahtua tilanteissa, jotka eivät ole käynnissä mRNA: n proteiinien translaation ulkopuolella.
Endogeenisesti ekspressoitu miRNA metasoaaneissa ei yleensä täydennä täydellisesti suurta määrää geenejä ja siten ne moduloivat ekspressiota translaation tukahduttamisen avulla. Kuitenkin laitoksissa , prosessi on paljon suurempi spesifisyys kohde- mRNA- ja yleensä jokainen miRNA vain sitoutuu yhteen mRNA: han. Suurempi spesifisyys tarkoittaa, että mRNA: n hajoaminen tapahtuu todennäköisemmin.
Katso myös
- RNA: n aiheuttama transkription vaimennus (RITS)
- RNA -häiriö
Viitteet
Lue lisää
- Sontheimer, EJ (2005). "RNA -vaimennuskompleksien kokoonpano ja toiminta". Nature Reviews Molecular Cell Biology . 6 (2): 127–138. doi : 10.1038/nrm1568 . PMID 15654322 . S2CID 27294007 .
- Fu Q, Yuan YA (maaliskuu 2013). "Rakenteelliset oivallukset RISC-kokoonpanoon, jota helpottavat ihmisen RNA-helikaasi A: n (DHX9) dsRNA: ta sitovat domeenit" . Nukleiinihappotutkimus . 41 (5): 3457–70. doi : 10.1093/nar/gkt042 . PMC 3597700 . PMID 23361462 .
- Schwarz DS, Tomari Y, Zamore PD (2004). "RNA: n aiheuttama vaimennuskompleksi on Mg 2+ -riippuvainen endonukleaasi" . Nykyinen biologia . 14 (9): 787–91. doi : 10.1016/j.cub.2004.03.008 . PMID 15120070 .
Ulkoiset linkit
- RNA-indusoitu+vaimennus+-kompleksi Yhdysvaltain kansallisessa kirjastossa Medical Subject Headings (MeSH)