Kromofori - Chromophore

Kromofori on osa molekyyliä, joka vastaa sen väri . Väri, joka on nähdä silmät on yksi ei imeytynyt joita heijastavan kohteen tietyn aallonpituuden spektrin näkyvän valon . Kromofori on alue molekyylissä, jossa kahden eri molekyylipallon välinen energiaero on näkyvän spektrin alueella. Näkyvä valo osuu kromofori voidaan siis absorboi virittämiseksi elektroni sen perustilassa osaksi innostunut tilaan . Biologisissa molekyyleissä, jotka toimivat valon energian sieppaamiseen tai havaitsemiseen, kromofori on osa, joka aiheuttaa molekyylin konformaatiomuutoksen valon osuessa siihen.
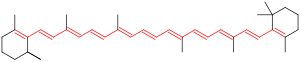
Konjugoidut pi-bond-järjestelmän kromoforit


Aivan kuten kaksi vierekkäistä p-orbitaalia molekyylissä muodostaa pi-sidoksen , kolme tai useampia vierekkäisiä p-orbitaaleja molekyylissä voivat muodostaa konjugoidun pi-järjestelmän . Konjugoidussa pi-järjestelmässä elektronit kykenevät sieppaamaan tiettyjä fotoneja, kun elektronit resonoivat tietyllä etäisyydellä p-orbitaaleista-samalla tavalla kuin radioantenni havaitsee fotonit koko pituudeltaan. Tyypillisesti mitä konjugoituneempi (pidempi) pi-järjestelmä on, sitä pidempi fotonin aallonpituus voidaan kaapata. Toisin sanoen, jokaisen lisättynä vierekkäisellä kaksoissidoksella, jonka näemme molekyylikaaviossa, voimme ennustaa, että järjestelmä näyttää asteittain todennäköisemmin keltaiselta silmillemme, koska se on vähemmän todennäköistä absorboida keltaista valoa ja todennäköisemmin absorboida punaista valoa. ("Alle kahdeksan konjugoidun kaksoissidoksen konjugoidut järjestelmät absorboivat vain ultraviolettialueella ja ovat värittömiä ihmissilmälle", "Siniset tai vihreät yhdisteet eivät tyypillisesti luota pelkästään konjugoituihin kaksoissidoksiin.")
On konjugoitu kromoforit, elektronit hypätä energiatasojen välillä , jotka ovat laajennettu pi orbitaalit , joka on muodostettu sarjan vuorottelevia yhden ja kaksoissidoksia , usein aromaattisia järjestelmiä. Yleisiä esimerkkejä ovat verkkokalvo (käytetään silmään valon havaitsemiseen), erilaiset elintarvikevärit , kangasvärit ( atsoyhdisteet ), pH-indikaattorit , lykopeeni , β-karoteeni ja antosyaanit . Eri tekijät kromoforin rakenteessa määrittävät, millä aallonpituusalueella spektrissä kromofori absorboi. Konjugoidun järjestelmän pidentäminen tai laajentaminen , jossa on enemmän tyydyttymättömiä (useita) sidoksia molekyylissä, pyrkii siirtämään absorptiota pitemmille aallonpituuksille. Woodward – Fieser -sääntöjä voidaan käyttää likimääräisen ultraviolettisäteilyn näkyvän maksimiabsorptioaallonpituuden arvioimiseen orgaanisissa yhdisteissä, joissa on konjugoitu pi -sidosjärjestelmä.
Jotkut näistä ovat metallikompleksikromoforeja, jotka sisältävät metallia koordinointikompleksissa ligandien kanssa. Esimerkkejä ovat klorofylli , jota kasvit käyttävät fotosynteesiin, ja hemoglobiini , hapen kuljettaja selkärankaisten eläimissä. Näissä kahdessa esimerkissä metalli on kompleksoitunut tetrapyrrolin makrosyklirenkaan keskelle : metalli on rauta hemoglobiinin heemiryhmässä (rauta porfyriinirenkaassa ) tai magnesium, joka on kompleksoitunut kloorityyppiseen renkaaseen, jos kyseessä on klorofylli . Makrosyklirenkaan erittäin konjugoitu pi-sidosjärjestelmä absorboi näkyvää valoa. Keskusmetallin luonne voi myös vaikuttaa metalli-makrosyklikompleksin absorptiospektriin tai ominaisuuksiin, kuten viritystilan käyttöikään. Tetrapyrroliosa orgaanisissa yhdisteissä, joka ei ole makrosyklinen, mutta jolla on edelleen konjugoitu pi-sidosjärjestelmä, toimii edelleen kromoforina. Esimerkkejä tällaisista yhdisteistä ovat bilirubiini ja urobiliini , joilla on keltainen väri.
Auxochrome
Auksokromiryhmiä on funktionaalinen ryhmä atomien kiinnitetty kromofori, joka muuttaa kyky kromoforin absorboivat valoa, muuttamalla aallonpituus ja intensiteetti imeytymistä.
Halokromismi
Halokromismi tapahtuu, kun aine muuttaa väriä pH -arvon muuttuessa. Tämä on ominaisuus pH -indikaattoreille , joiden molekyylirakenne muuttuu ympäröivän pH: n tiettyjen muutosten vuoksi. Tämä rakenteen muutos vaikuttaa kromoforiin pH -indikaattorimolekyylissä. Esimerkiksi fenolftaleiini on pH -indikaattori, jonka rakenne muuttuu pH -arvon muuttuessa seuraavan taulukon mukaisesti:
| Rakenne | 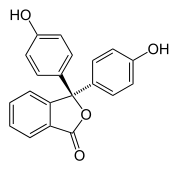 |

|
|---|---|---|
| pH | 0-8,2 | 8.2-12 |
| Ehdot | hapan tai lähes neutraali | perus |
| Värin nimi | väritön | vaaleanpunaisesta fuksiaan |
| Väri |
PH-alueella noin 0-8 molekyylissä on kolme aromaattista rengasta, jotka kaikki ovat sitoutuneet tetraedriseen sp 3- hybridisoituneeseen hiiliatomiin keskellä, mikä ei tee aromaattisten renkaiden π-sidosta konjugaatiksi. Rajoitetun laajuutensa vuoksi aromaattiset renkaat absorboivat valoa vain ultraviolettialueella, joten yhdiste näyttää värittömältä pH-alueella 0-8. Kuitenkin, kuten pH: n noustessa yli 8,2, että keskeinen hiili tulee osa kaksoissidoksen tulossa sp 2 hybridisoidaan ja jättää ap kiertoradan on päällekkäisyyttä π-liimaus renkaat. Tämä saa kolme rengasta konjugoitumaan yhteen muodostaen pidennetyn kromoforin, joka absorboi pidemmän aallonpituuden näkyvää valoa ja näyttää fuksiavärin. Kun pH-alueet ovat 0–12: n ulkopuolella, muut molekyylirakenteen muutokset aiheuttavat muita värimuutoksia; katso Fenolftaleiinin tiedot.
Yleiset kromoforin absorptioaallonpituudet
| Toiminnallinen ryhmä tai yhdiste | Absorptiotaallonpituus |
|---|---|
| Bromofenolisininen (keltainen muoto) | 591 nm |
Katso myös
Viitteet
Ulkoiset linkit
- Värin syyt : fyysiset mekanismit, joiden avulla väri syntyy.
- Nopea nanokokoinen elektroniikka voi olla mahdollista Chromophores - Azonano.com

