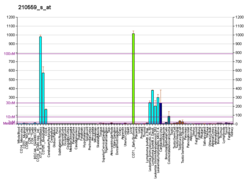
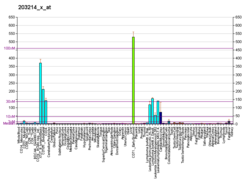
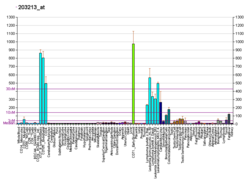
Sykliiniriippuvainen kinaasi 1 - Cyclin-dependent kinase 1
Sykliinikinaasi-1 tunnetaan myös CDK1 tai solunjakautumiskierron proteiini 2 homologi on erittäin konservoitunut proteiini, joka toimii seriini / treoniini -kinaasin , ja on avainasemassa solusyklin säätely. Se on erittäin tutkittu Analysis hiivassa S. cerevisiae , ja halkeamisprosessin hiiva S. pombe , jossa se koodataan geenien CDC28 ja cdc2 , vastaavasti. Ihmisillä Cdk1 koodaa CDC2 -geeni. Kanssa sen sykliini kumppanit, Cdk1 muodostaa komplekseja että fosforyloida erilaisia kohdesubstraatteja (yli 75 on tunnistettu Analysis hiiva); näiden proteiinien fosforylaatio johtaa solusyklin etenemiseen.
Rakenne
Cdk1 on pieni proteiini (noin 34 kilodaltonia) ja se on erittäin säilynyt. Cdk1: n ihmisen homologilla, CDC2 , on noin 63% aminohappoidentiteetti hiivahomologinsa kanssa. Lisäksi ihmisen CDC2 pystyy pelastamaan fd -hiivan, joka sisältää cdc2 -mutaation. Cdk1 koostuu enimmäkseen paljaasta proteiinikinaasimotiivista, jota muut proteiinikinaasit jakavat. Cdk1 sisältää muiden kinaasien tavoin halkeaman, johon ATP sopii. Cdk1-substraatit sitoutuvat halkeaman suun lähellä, ja Cdk1-jäännökset katalysoivat y-fosfaatin kovalenttisen sidoksen substraatin hydroksyyliseriinin /treoniinin happiin.
Tämän katalyyttisen ytimen lisäksi Cdk1 sisältää muiden sykliiniriippuvaisten kinaasien tavoin T-silmukan, joka vuorovaikutteisen sykliinin puuttuessa estää substraatin sitoutumisen aktiiviseen Cdk1-kohtaan. Cdk1 sisältää myös PSTAIRE -kierukan, joka sykliinin sitoutumisen jälkeen siirtää ja järjestää aktiivisen kohdan uudelleen helpottaen Cdk1 -kinaasiaktiivisuutta.
Toiminto
Sidottuina sykliinikumppaneisiinsa Cdk1 -fosforylaatio johtaa solusyklin etenemiseen. Cdk1 -aktiivisuus ymmärretään parhaiten S. cerevisiaessa , joten Cdk1 S. cerevisiae -aktiivisuus kuvataan tässä.
Orastavassa hiivassa solusyklin alkamista ohjataan kahdella säätelykompleksilla, SBF: llä (SCB: tä sitova tekijä) ja MBF: llä (MCB: tä sitova tekijä). Nämä kaksi kompleksit ohjaavat G 1 / S-geenin transkriptio; ne ovat kuitenkin yleensä passiivisia. Whi5 -proteiini estää SBF: ää ; kuitenkin, kun fosforyloituu 3O-Cdk1, Whi5 työnnetään ulos tumasta, mikä mahdollistaa transkription G 1 / S -regulonin , joka sisältää G 1 / S-sykliinit Cln1,2. G 1 /S-sykliini-Cdk1-aktiivisuus johtaa valmistautumiseen S-vaiheen tuloon (esim. Sentromeerien tai karan napakappaleen päällekkäisyys) ja S-sykliinien nousuun (Clb5,6 S. cerevisiaessa ). Clb5,6-Cdk1-kompleksit johtavat suoraan replikaation alkuperän aloittamiseen; Sic1 kuitenkin estää niitä , mikä estää S -vaiheen ennenaikaisen alkamisen.
Cln1,2- ja/tai Clb5,6-Cdk1-kompleksiaktiivisuus johtaa Sic1-tasojen äkilliseen laskuun, mikä mahdollistaa johdonmukaisen S-vaiheen tulon. Lopuksi M -sykliinien (esim. Clb1, 2, 3 ja 4) fosforylaatio kompleksissa Cdk1: n kanssa johtaa karan kokoonpanoon ja sisarkromatidien kohdistamiseen. Cdk1-fosforylaatio johtaa myös ubikvitiiniproteiiniligaasin APC Cdc20 aktivoitumiseen, joka aktivointi mahdollistaa kromatidien erottamisen ja lisäksi M-faasin sykliinien hajoamisen. Tämä M -sykliinien tuhoaminen johtaa mitoosin viimeisiin tapahtumiin (esim. Karan purkaminen, mitoottinen poistuminen).
Säätö
Ottaen huomioon sen keskeisen roolin solusyklin etenemisessä, Cdk1 on erittäin säännelty. Kaikkein ilmeisimmin Cdk1: tä säännellään sen sitoutumisella sen sykliinikumppaneiden kanssa. Sykliinin sitoutuminen muuttaa pääsyä Cdk1: n aktiiviseen kohtaan, mikä mahdollistaa Cdk1 -aktiivisuuden; lisäksi sykliinit antavat spesifisyyttä Cdk1 -aktiivisuudelle. Ainakin jotkut sykliinit sisältävät hydrofobisen laastarin, joka voi olla suoraan vuorovaikutuksessa substraattien kanssa ja antaa kohdespesifisyyden. Lisäksi sykliinit voivat kohdistaa Cdk1 tiettyihin solun alle.
Sykliinien säätelyn lisäksi Cdk1: tä säätelee fosforylaatio. Konservoitunut tyrosiini (Tyr15 ihmisillä) johtaa Cdk1: n inhibitioon; tämän fosforylaation uskotaan muuttavan ATP -orientaatiota estäen tehokkaan kinaasiaktiivisuuden. Esimerkiksi S. pombessa epätäydellinen DNA -synteesi voi johtaa tämän fosforylaation vakautumiseen estäen mitoottista etenemistä. Wee1 , joka on säilynyt kaikkien eukaryoottien joukossa, fosforyloi Tyr15: n, kun taas Cdc25 -perheen jäsenet ovat fosfataaseja, jotka estävät tätä toimintaa. Näiden kahden tasapainon uskotaan auttavan hallitsemaan solusyklin etenemistä. Wee1: tä ohjaavat ylävirtaan Cdr1, Cdr2 ja Pom1 .
Cdk1-sykliinikomplekseja ohjaa myös Cdk-inhibiittoriproteiinien (CKI) suora sitoutuminen. Yksi tällainen proteiini, josta on jo keskusteltu, on Sic1. Sic1 on stökiometrinen estäjä, joka sitoutuu suoraan Clb5,6-Cdk1-komplekseihin. Sic1: n monen sivuston fosforylaation Cdk1-Cln1/2: n uskotaan ajavan Sic1: n ubikvitinaatiota ja tuhoamista, ja laajentamalla S-vaiheen tulon ajoitusta. Vasta kunnes Sic1 -esto on voitettu, Clb5,6 -aktiivisuutta voi esiintyä ja S -vaiheen aloitus voi alkaa.
Vuorovaikutukset
Cdk1: n on osoitettu olevan vuorovaikutuksessa seuraavien kanssa:
Katso myös
Mastl
Viitteet
Lue lisää
- Draetta G, Eckstein J (1997). "Cdc25 -proteiinifosfataasit solujen lisääntymisessä". Biochim. Biophys. Acta . 1332 (2): M53–63. doi : 10.1016/S0304-419X (96) 00049-2 . PMID 9141461 .
- Kino T, Pavlakis GN (2004). "Ihmisen immuunikatoviruksen tyypin 1 lisäproteiinin Vpr kumppanimolekyylit" . DNA Cell Biol . 23 (4): 193–205. doi : 10.1089/104454904773819789 . PMID 15142377 .
- Kino T, Chrousos GP (2004). "Ihmisen immuunikatoviruksen tyypin 1 lisäproteiini Vpr: AIDSiin liittyvän insuliiniresistenssin/lipodystrofian oireyhtymän aiheuttaja?" . Ann. NY Acad. Sei . 1024 (1): 153–167. Bibcode : 2004NYASA1024..153K . doi : 10.1196/annals.1321.013 . PMID 15265780 . S2CID 23655886 .
- Zhao LJ, Zhu H (2005). "HIV-1-lisäsäätelyproteiinin Vpr rakenne ja toiminta: uusia vihjeitä lääkkeen suunnitteluun". Curr. Lääkkeen kohteet Immuunijärjestelmä. Metabolia. Häiriö . 4 (4): 265–275. doi : 10.2174/1568008043339668 . PMID 15578977 .
- Le Rouzic E, Benichou S (2006). "HIV-1: n Vpr-proteiini: erilliset roolit viruksen elinkaaren aikana" . Retrovirologia . 2 : 11. doi : 10.1186/1742-4690-2-11 . PMC 554975 . PMID 15725353 .
- Zhao RY, vanhin RT (2005). "Virusinfektiot ja solusyklin G2/M -säätely" . Cell Res . 15 (3): 143–149. doi : 10.1038/sj.cr.7290279 . PMID 15780175 .
- Zhao RY, Bukrinsky M, vanhin RT (2005). "HIV-1-virusproteiini R (Vpr) ja isäntäsoluvasteet". Intialainen J. Med. Res . 121 (4): 270–86. PMID 15817944 .
- Kaldis P, Aleem E (2007). "Solusyklin sisaruskilpailu: Cdc2 vs. Cdk2" . Solusykli . 4 (11): 1491–1494. doi : 10.4161/cc.4.11.2124 . PMID 16258277 .
- Li L, Li HS, Pauza CD, Bukrinsky M, Zhao RY (2006). "HIV-1-apuproteiinien roolit viruksen patogeneesissä ja isäntä-patogeeni-vuorovaikutuksessa" . Cell Res . 15 (11–12): 923–934. doi : 10.1038/sj.cr.7290370 . PMID 16354571 .
- Rietbrock N, Keller F (1977). "[Biologinen saatavuus ja lääkkeiden" ensimmäinen kerta "-vaikutus]". Fortschr. Med . 95 (28): 1765–6, 1774–80. PMID 914146 .
- Azzi L, Meijer L, Reed SI, Pidikiti R, Tung HY (1992). "Solusyklin ohjausproteiinien p34cdc2 ja p9CKShs2 vuorovaikutus. Todisteita kahdesta yhteistyöhön sitoutuvasta domeenista p9CKShs2: ssa" . Eur. J. Biochem . 203 (3): 353–360. doi : 10.1111/j.1432-1033.1992.tb16557.x . PMID 1310466 .
- Dutta A, Stillman B (1992). "cdc2 -perheen kinaasit fosforyloivat ihmisen solun DNA: n replikaatiotekijän, RPA, ja aktivoivat DNA: n replikaation" . EMBO J. . 11 (6): 2189–99. doi : 10.1002/j.1460-2075.1992.tb05278.x . PMC 556686 . PMID 1318195 .
- Koff A, Giordano A, Desai D, Yamashita K, Harper JW, Elledge S, Nishimoto T, Morgan DO, Franza BR, Roberts JM (1992). "Sykliinin E-cdk2-kompleksin muodostuminen ja aktivointi ihmisen solusyklin G1-vaiheen aikana". Tiede . 257 (5077): 1689–1694. Bibcode : 1992Sci ... 257.1689K . doi : 10.1126/science.1388288 . PMID 1388288 .
- Russo GL, Vandenberg MT, Yu IJ, Bae YS, Franza BR, Marshak DR (1992). "Kaseiinikinaasi II fosforyloi p34cdc2 -kinaasin HeLa -solujakautumissyklin G1 -vaiheessa" . J. Biol. Chem . 267 (28): 20317–25. doi : 10.1016/S0021-9258 (19) 88704-5 . PMID 1400350 .
- Rubinfeld B, Crosier WJ, Albert I, Conroy L, Clark R, McCormick F, Polakis P (1992). "Rap1GAP -katalyyttisen domeenin lokalisointi ja fosforylaatiokohdat mutaatioanalyysillä" . Mol. Solu. Biol . 12 (10): 4634–42. doi : 10.1128/MCB.12.10.4634 . PMC 360390 . PMID 1406653 .
- van der Sluijs P, Hull M, Huber LA, Mâle P, Goud B, Mellman I (1992). "Käänteinen fosforylaatio-defosforylaatio määrittää rab4: n lokalisoinnin solusyklin aikana" . EMBO J. . 11 (12): 4379–89. doi : 10.1002/j.1460-2075.1992.tb05538.x . PMC 557012 . PMID 1425574 .
- Seth A, Alvarez E, Gupta S, Davis RJ (1992). "Fosforylaatiokohta, joka sijaitsee c-Mycin NH2-terminaalisessa domeenissa, lisää geeniekspression transaktivaatiota" . J. Biol. Chem . 266 (35): 23521–4. doi : 10.1016/S0021-9258 (18) 54312-X . PMID 1748630 .
- Lees JA, Buchkovich KJ, Marshak DR, Anderson CW, Harlow E (1992). "Retinoblastoomaproteiini fosforyloituu useissa kohdissa ihmisen cdc2: n avulla" . EMBO J. . 10 (13): 4279–90. doi : 10.1002/j.1460-2075.1991.tb05006.x . PMC 453181 . PMID 1756735 .
- Nazarenko SA, Ostroverhova NV, Spurr NK (1991). "Ihmisen solusyklin säätögeenin CDC2 alueellinen kohdistaminen kromosomiin 10q21 in situ -hybridisaatiolla". Hyräillä. Genet . 87 (5): 621–2. doi : 10.1007/BF00209025 . PMID 1916766 . S2CID 25673088 .
- Nissen MS, Langan TA, Reeves R (1991). "Fosforylaatio cdc2 -kinaasin avulla moduloi suuren liikkuvuuden ryhmän I ei -histonikromatiiniproteiinin DNA -sitoutumisaktiivisuutta" . J. Biol. Chem . 266 (30): 19945–52. doi : 10.1016/S0021-9258 (18) 54874-2 . PMID 1939057 .
Ulkoiset linkit
- Yleiskatsaus kaikista ATE : ssä saatavilla olevista rakenteellisista tiedoista UniProtille : P06493 (sykliiniriippuvainen kinaasi 1) PDBe-KB: ssä .