Schwannin solu - Schwann cell
| Schwannin solu | |
|---|---|
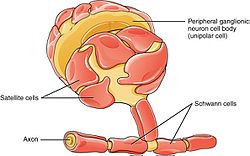 PNS: ssä on satelliitti- ja Schwann -soluja.
| |
| Tunnisteet | |
| MeSH | D012583 |
| FMA | 62121 |
| Neuroanatomian anatomiset termit | |
Schwannin solut tai neurolemmocytes (nimetty Saksan physiologist Theodor Schwannin ) ovat tärkeimmät glia on ääreishermoston (PNS). Gliaaliset solut toimivat tukemalla neuroneja ja PNS: ssä, sisältävät myös satelliittisoluja , hajua ympäröiviä soluja , suoliston limakalvoja ja glia, jotka sijaitsevat aistinvaraisissa hermopäätteissä, kuten Pacinian solu . Kaksi Schwann -solutyyppiä ovat myelinoivia ja ei -myelinoivia. Myelinoivat Schwann -solut kietoutuvat moottori- ja aistineuronien aksonien ympärille muodostaen myeliinivaipan . Schwannin solupromoottori on läsnä alavirtaanihmisen dystrofiinigeenin alue, joka antaa lyhennetyn transkriptin, joka syntetisoidaan jälleen kudosspesifisellä tavalla.
PNS: n kehittämisen aikana myelinaation säätelymekanismeja ohjataan tiettyjen geenien ennakoivalla vuorovaikutuksella, mikä vaikuttaa transkription kaskadiin ja muotoilee myelinoitujen hermokuitujen morfologiaa.
Schwannin solut ovat mukana monissa tärkeitä näkökohtia perifeerisen hermon biologia-johtuminen hermoston impulssien pitkin aksoneita , hermojen kehityksen ja uudistumista , trofia tukea neuronien , tuotanto hermo soluväliaineen, modulaatio neuromuskulaarisen synaptisen aktiivisuuden, ja esittely antigeenien ja T -lymfosyytit .
Charcot – Marie – Tooth -tauti , Guillain – Barrén oireyhtymä (akuutti tulehduksellinen demyelinisoiva polyradikulopatiatyyppi), schwannomatosis , krooninen tulehduksellinen demyelinisoiva polyneuropatia ja lepra ovat kaikki neuropatioita, joihin liittyy Schwannin soluja.
Rakenne
| Schwann -solut kääritty aksonin ympärille |
|---|
Schwann -solut ovat erilaisia glia -soluja, jotka pitävät perifeeriset hermokuidut (sekä myelinoidut että myelinoimattomat) hengissä. Myelinoiduissa aksoneissa Schwann -solut muodostavat myeliinivaipan . Vaippa ei ole jatkuva. Yksittäiset myelinoivat Schwann-solut kattavat noin 1 mm aksonia-mikä vastaa noin 1000 Schwann-solua aksonin 1 metrin pituudella. Viereisten Schwann -solujen välisiä aukkoja kutsutaan Ranvierin solmuiksi .
9-O-asetyyli GD3 gangliosidi on asetyloitu glykolipidi, jota esiintyy monentyyppisten selkärankaisten solujen solukalvoissa. Perifeerisen hermon regeneraation aikana Schwann-solut ilmentävät 9-0-asetyyli-GD3: a.
Toiminto
Selkärankaisen hermostoon perustuu myeliinitupen varten eristys ja menetelmä laskeva kalvo kapasitanssi on Axon. Aktiopotentiaalin hyppää solmusta toiseen, prosessissa, jota kutsutaan saltatory johtuminen , mikä voi lisätä johtuminen nopeus jopa 10 kertaa, lisäämättä aksonaalisen halkaisija. Tässä mielessä, Schwannin solut ovat PNS: n analogeja keskushermoston n oligodendrosyytit . Toisin kuin oligodendrosyytit, jokainen myelinoiva Schwann -solu eristää kuitenkin vain yhden aksonin (katso kuva). Tämä järjestely sallii toimintapotentiaalien suolaisen johtamisen ja lisääntyminen Ranvierin solmuissa. Tällä tavoin myelinaatio lisää huomattavasti johtumisnopeutta ja säästää energiaa.
Ei -myelinoivat Schwann -solut osallistuvat aksonien ylläpitoon ja ovat ratkaisevia hermosolujen selviytymisen kannalta. Jotkut ryhmittyvät pienempien aksonien ympärille ( ulkoinen kuva täällä ) ja muodostavat Remak -nippuja .
Myelinoivat Schwann -solut alkavat muodostaa myeliinivaippaa nisäkkäissä sikiön kehityksen ja työn aikana kiertämällä akselia ympäri, joskus jopa 100 kierrosta. Hyvin kehittynyt Schwann-solu on muotoiltu rullalle paperiarkin muotoiseksi, ja jokaisen kelan välissä on myeliinikerroksia. Käärinnän sisäkerrokset, jotka ovat pääasiassa kalvomateriaalia , muodostavat myeliinivaipan, kun taas ytimisen sytoplasman uloin kerros muodostaa neurilemman . Vain pieni määrä jäännössytoplasmaa mahdollistaa viestinnän sisä- ja ulkokerrosten välillä. Tämä näkyy histologisesti kuin Schmidt-Lantermann incisure .
Regenerointi
Schwann -solut tunnetaan rooleistaan hermojen uudistumisen tukemisessa . PNS: n hermot koostuvat monista Schwann -solujen myelinoimista aksoneista. Jos hermo vaurioituu, Schwann -solut auttavat sen aksonien pilkkomista ( fagosytoosi ). Tämän prosessin jälkeen Schwann -solut voivat ohjata regeneraatiota muodostamalla tunnelityypin, joka johtaa kohde -neuroneihin. Tämä tunneli tunnetaan Büngnerin vyöhykkeenä , joka on reuna -akselien ohjausrata, joka käyttäytyy kuin endoneuraaliputki. Vaurioituneen aksonin kanto pystyy itämään, ja ne versot, jotka kasvavat Schwann-solun "tunnelin" läpi, tekevät sitä noin 1 mm/vrk hyvissä olosuhteissa. Regenerointinopeus hidastuu ajan myötä. Onnistuneet aksonit voivat siis muodostaa yhteyden uudelleen lihaksiin tai elimiin, joita he aiemmin hallitsivat Schwann -solujen avulla, mutta spesifisyys ei säily ja virheitä esiintyy usein, varsinkin kun kyseessä ovat pitkät etäisyydet. Koska Schwann -solut kykenevät vaikuttamaan aksonien uusiutumiseen, ne on myös yhdistetty etuoikeutettuun moottorin uudelleenservointiin . Jos Schwann -soluja estetään liittymästä aksoneihin, aksonit kuolevat. Uudistuvat aksonit eivät saavuta mitään tavoitetta, elleivät Schwann -solut ole siellä tukemassa ja ohjaamassa niitä. Niiden on osoitettu olevan ennen kasvukartioita .
Schwann -solut ovat välttämättömiä terveiden aksonien ylläpitämiseksi. Ne tuottavat erilaisia tekijöitä, mukaan lukien neurotrofiinit , ja siirtävät myös välttämättömiä molekyylejä aksoneille.
Genetiikka
Schwannin solujen muodostuminen
Sox10
SOX10 on alkionkehityksen aikana aktiivinen transkriptiotekijä, ja runsaat todisteet osoittavat, että se on välttämätöntä gliaalisten linjojen luomiseksi rungon harjan soluista. Kun SOX10 inaktivoidaan hiirillä, satelliittiglia ja Schwann -solujen esiasteet eivät kehity, vaikka neuronit syntyvät normaalisti ongelmitta. SOX10: n puuttuessa hermosolujen elossa olevat solut selviävät ja voivat vapaasti tuottaa neuroneja, mutta gliaalinen spesifikaatio estetään. SOX10 saattaa vaikuttaa varhaisiin glia -esiasteisiin reagoimaan neureguliiniin 1 (katso alla).
Neuregulin 1
Neuregulin 1 (NRG1) toimii monella tapaa sekä edistää muodostumista että varmistaa kypsymättömien Schwann -solujen eloonjäämisen. Alkionkehityksen aikana NRG1 estää hermosolujen muodostumista hermosolun soluista, vaan edistää hermosolujen solujen johtamista polulle gliogeneesiin. NRG1 -signalointia ei kuitenkaan vaadita glial -erottumiseen hermostosta.
NRG1: llä on tärkeä rooli hermoharjan johdannaisten kehittämisessä. Neuraalisten harjasolujen on siirryttävä selkäjuuren alueen ohi löytääkseen sympaattisen gangliogeneesin ventraaliset alueet. Se on myös olennainen aksonista johdettu selviytymistekijä ja mitogeeni Schwannin solujen esiasteille. Selkäjuuren ganglionista ja motorisista neuroneista löytyy se hetki, jolloin Schwannin solujen esiasteet alkavat täyttää selkäydinhermoja ja vaikuttavat siksi Schwannin solujen eloonjäämiseen. Alkiohermoissa transmembraaninen III -isomuoto on todennäköisesti NRG1: n ensisijainen variantti, joka vastaa selviytymissignaaleista. Hiirillä, joilta puuttuu transmembraaninen III -isoformi, Schwannin solujen esiasteet poistuvat lopulta selkärangan hermoista.
Myeliinivaipan muodostuminen
P0
Myeliiniproteiinin nolla (P0) on soluadheesiomolekyyli, joka kuuluu immunoglobuliinin superperheeseen ja on perifeerisen myeliinin pääkomponentti, joka muodostaa yli 50% vaipan kokonaisproteiinista. P0: n on osoitettu olevan välttämätön kompaktin myeliinin muodostumiselle, koska P0-nolla-mutanttihiiret (P0-) osoittivat vakavasti poikkeavaa perifeeristä myelinaatiota. Vaikka suuren kaliiperin aksonien myelinointi aloitettiin P0-hiirillä, syntyneet myeliinikerrokset olivat hyvin ohuita ja huonosti tiivistyneitä. Yllättäen P0-hiiret osoittivat myös molempien aksonien ja niiden ympäröivien myeliinivaippojen rappeutumista, mikä viittaa siihen, että P0: lla on rooli sekä myeliinin muodostumisen että sen aksonin rakenteellisen eheyden ylläpitämisessä. P0-hiirille kehittyi käyttäytymishäiriöitä noin 2 viikon iässä, kun hiirissä alkoi näkyä lievää vapinaa. Vakava koordinaatiokyvyttömyys syntyi myös eläinten kehittyessä, kun vapina muuttui vakavammaksi ja joillekin vanhemmille hiirille kehittyi kouristuksia. Huolimatta heikentyneestä motorisesta käyttäytymisestä, näillä eläimillä ei havaittu halvaantumista. P0 on myös tärkeä geeni, joka ilmaistaan varhain Schwannin solulinjassa, ja se ilmennetään Schwannin solujen esiasteissa sen jälkeen, kun se on erotettu muuttuvista hermosolun soluista kehittyvän alkion sisällä.
Krox-20
Myös useita tärkeitä transkriptiotekijöitä ilmaistaan ja ne osallistuvat eri kehitysvaiheisiin muuttamalla Schwann -solujen ominaisuuksia epäkypsästä tilasta kypsäksi. Yksi välttämätön transkriptiotekijä, joka ilmaistaan myelinaatioprosessin aikana, on Krox-20. Se on yleinen sinkki-sormen transkriptiotekijä ja ilmentyy rombomeereissä 3 ja 5.
Krox-20: tä pidetään yhtenä PNS-myelinaation pääsäätelijöistä ja se on tärkeä myeliinin spesifisten rakenneproteiinien transkription edistämisessä. Sen on osoitettu kontrolloivan joukkoa geenejä, jotka ovat vastuussa tämän ominaisuuden häiritsemisestä aksonissa muuttamalla sen pro-myelinoivasta tilasta myelinoivaan tilaan. Tällä tavalla Krox-20-kaksoispoistohiirillä on havaittu, että taka-aivojen segmentoituminen ja Schwann-soluun liittyvien aksonien myelinaatio vaikuttaa. Itse asiassa näissä hiirissä Schwann -solut eivät pysty suorittamaan myelinaatiota kunnolla, koska ne käärivät sytoplasmiset prosessinsa vain puolitoista kierrosta aksonin ympäri ja huolimatta siitä, että ne ilmentävät edelleen varhaista myeliinimarkkeria, myöhäisiä myeliinigeenituotteita ei ole . Lisäksi viimeaikaiset tutkimukset ovat myös osoittaneet tämän transkriptiotekijän merkityksen myelinaatiofenotyypin ylläpitämisessä (ja vaatii Sox 10: n rinnakkaisilmentymistä), koska sen inaktivointi johtaa Schwann-solujen erilaistumiseen.
Lääketieteellinen merkitys
Charcot -Marie -Tooth -tauti (CMT), Guillain -Barrén oireyhtymä (GBS, akuutti tulehduksellinen demyelinisoiva polyradikulopatiatyyppi), schwannomatosis ja krooninen tulehduksellinen demyelinisoiva polyneuropatia (CIDP), lepra ja Zika -virus ovat kaikki neuropatioita, joihin liittyy Schwannin soluja.
Elinsiirto
Useita kokeellisia tutkimuksia vuodesta 2001 istuttaa Schwannin soluja yritettiin saada aikaan remyelinaatioon on multippeliskleroosi -afflicted potilailla. Viimeisten kahden vuosikymmenen aikana monet tutkimukset ovat osoittaneet positiivisia tuloksia ja potentiaalia Schwannin solusiirroille selkäydinvamman hoitona sekä auttamalla vaurioituneiden keskushermoston aksonien uusiutumista että myelinaatiota. Schwannin solusiirrot yhdessä muiden hoitojen, kuten kondroitinaasi ABC: n kanssa, on myös osoitettu olevan tehokkaita toiminnallisessa toipumisessa selkäydinvammasta.
Katso myös
- Elektrofysiologia
- Hodgkin -Huxleyn malli
- Mesaxon
- Neurotransmissio
- Hajua sulava solu
- Schwannoma
- Luettelo alkukerroksista johdetuista ihmisen solutyypeistä
Viitteet
Ulkoiset linkit
- Kaavio osoitteessa clc.uc.edu
- Histologiakuva: 21301loa - Histologian oppimisjärjestelmä Bostonin yliopistossa - "Solun ultrastruktuuri: myelinoitu aksoni ja Schwann -solu"
- Solukeskinen tietokanta - Schwann -solu


