Kaspaasi 3 - Caspase 3
Kaspaasi-3 on kaspaasiproteiini, joka on vuorovaikutuksessa kaspaasi-8: n ja kaspaasi-9: n kanssa . Sitä koodaa CASP3 -geeni. CASP3 ortologeihin on tunnistettu lukuisia nisäkkäillä , joille täydellisen genomin tiedot ovat saatavilla. Ainutlaatuinen ortologeihin esiintyy myös linnuissa , liskot , lissamphibians ja teleosts .
CASP3 proteiini on jäsenenä c ysteine- asp rekka happo prote ase ( kaspaasi ) -perheen. Kaspaasien peräkkäisellä aktivoinnilla on keskeinen rooli solujen apoptoosin toteutusvaiheessa . Kaspaaseja esiintyy inaktiivisina proentsyymeinä, jotka käyvät läpi proteolyyttisen prosessin konservoituneilla asparagiinitähteillä, jolloin muodostuu kaksi alayksikköä, suuria ja pieniä, jotka dimeroituvat muodostaen aktiivisen entsyymin . Tämä proteiini pilkkoo ja aktivoi kaspaaseja 6 ja 7 ; ja itse proteiini käsitellään ja aktivoidaan kaspaasien 8, 9 ja 10 avulla . Se on vallitseva kaspaasi, joka osallistuu amyloidi-beeta-4A-prekursoriproteiinin pilkkomiseen , mikä liittyy hermosolukuolemaan Alzheimerin taudissa . Tämän geenin vaihtoehtoinen silmukointi johtaa kahteen transkriptivarianttiin, jotka koodaavat samaa proteiinia.

TNF -R1: n signalointireitti . Katkoviivat harmaat viivat edustavat useita vaiheita
|
Caspase-3: lla on monia tyypillisiä ominaisuuksia, jotka ovat yhteisiä kaikille tällä hetkellä tunnetuille kaspaaseille. Esimerkiksi sen aktiivinen kohta sisältää kysteiinitähteen (Cys-163) ja histidiinitähteen (His-121), jotka stabiloivat proteiinisekvenssin peptidisidoksen katkeamisen asparagiinihapon karboksipään puolelle , kun se on osa tiettyä 4-aminohapposekvenssi. Tämä spesifisyys sallii kaspaasien olla uskomattoman selektiivisiä, ja asparagiinihappo on 20 000-kertainen etusijalla glutamiinihappoon nähden . Keskeistä kaspaasit solussa on, että ne ovat läsnä tsymogeeneja , kutsutaan procaspases, jotka ovat inaktiivisia, kunnes biokemiallinen muutos aiheuttaa niiden aktivoituminen. Jokaisella prokaspaasilla on N-terminaalinen suuri alayksikkö, noin 20 kDa, jota seuraa pienempi, noin 10 kDa: n alayksikkö, nimeltään p20 ja p10.
Alustan spesifisyys
Normaaleissa olosuhteissa kaspaasit tunnistavat tetra-peptidisekvenssit substraateillaan ja hydrolysoivat peptidisidokset asparagiinihappotähteiden jälkeen . Kaspaasilla 3 ja kaspaasilla 7 on samanlainen substraattispesifisyys tunnistamalla tetra-peptidimotiivi Asp-xx-Asp. C-terminaalinen Asp on ehdottoman välttämätön, kun taas muissa kolmessa asennossa olevat vaihtelut voidaan sietää. Kaspaasisubstraattispesifisyyttä on käytetty laajalti kaspaasipohjaisessa inhibiittori- ja lääkesuunnittelussa.
Rakenne
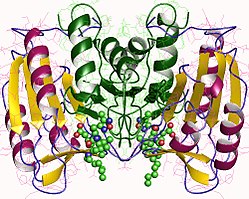
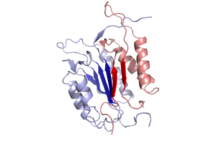
Erityisesti kaspaasi-3 (tunnetaan myös nimellä CPP32/Yama/apopain) muodostuu 32 kDa: n tsymogeenistä, joka pilkotaan 17 kDa: n ja 12 kDa: n alayksiköiksi. Kun prokaspaasi pilkotaan tietystä tähteestä, aktiivinen heterotetrameeri voidaan sitten muodostaa hydrofobisilla vuorovaikutuksilla, jolloin neljä rinnakkaista anti-rinnakkaista beeta-arkkia p17: stä ja kaksi p12: sta tulevat yhteen muodostamaan heterodimeeri, joka vuorovaikutuksessa toisen heterodimeerin kanssa muodostaa koko 12-säikeinen beeta -arkkirakenne, jota ympäröivät alfa-heliksit ja joka on ainutlaatuinen kaspaaseille. Kun heterodimeerit kohdistuvat päästä toisiinsa, aktiivinen kohta sijoitetaan molekyylin kumpaankin päähän, joka on muodostettu molempien osallistuvien alayksiköiden tähteistä, vaikka tarvittavat Cys-163- ja His-121-tähteet löytyvät p17: stä (suurempi ) alayksikkö.
Mekanismi
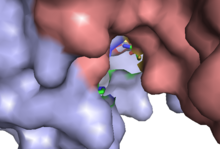
Kaspaasi-3: n katalyyttikohta sisältää Cys-163: n sulfohydryyliryhmän ja His-121: n imidatsolirenkaan . His-121 stabiloi avainaspartaattitähteen karbonyyliryhmän , kun taas Cys-163 hyökkää lopulta katkaisemaan peptidisidoksen. Cys-163 ja Gly-238 toimivat myös stabiloimaan substraatti-entsyymikompleksin tetraedrinen siirtymätila vety- sidoksen avulla . In vitro kaspaasi-3: n on havaittu suosivan peptidisekvenssiä DEVDG (Asp-Glu-Val-Asp-Gly), jonka pilkkoutuminen tapahtuu toisen asparagiinihappotähteen karboksipuolella (D: n ja G: n välissä). Kaspaasi-3 on aktiivinen laajalla pH- alueella, joka on hieman korkeampi (emäksisempi) kuin monet muut teloittajakaspaasit. Tämä laaja alue osoittaa, että kaspaasi-3 on täysin aktiivinen normaaleissa ja apoptoottisissa soluolosuhteissa.
Aktivointi
Kaspaasi-3 aktivoidaan apoptoottisessa solussa sekä ulkoisella (kuoleman ligandi) että sisäisellä (mitokondrio) reitillä. Kaspaasi-3: n zymogeeninen ominaisuus on välttämätön, koska jos sitä ei säädetä, kaspaasiaktiivisuus tappaisi solut erotuksetta. Teloittajakaspaasina kaspaasi-3-zymogeenillä ei ole käytännössä mitään aktiivisuutta, ennen kuin initiaattorikaspaasi katkaisee sen apoptoottisten signalointitapahtumien jälkeen. Yksi tällainen signalointitapahtuma on grantsyymi B: n , joka voi aktivoida initiaattorikaspaaseja, tuominen soluihin, jotka on tarkoitettu tappaja -T -solujen apoptoosille . Tämä ulkoinen aktivointi laukaisee sitten apoptoottiselle reitille tunnusomaisen kaspaasikaskadin, jossa kaspaasi-3: lla on hallitseva rooli. On luontainen aktivointi, sytokromi c: alkaen mitokondrioiden toimii yhdessä kaspaasi-9 , apoptoosiin aktivoiva tekijä 1 ( Apaf-1 ), ja ATP- menetelmän prokaspaasi-3. Nämä molekyylit riittävät aktivoimaan kaspaasi-3: n in vitro, mutta muut säätelyproteiinit ovat välttämättömiä in vivo . Mangosteenin ( Garcinia mangostana ) uutteen on osoitettu estävän kaspaasi 3: n aktivaatiota B-amyloidilla käsitellyissä ihmisen hermosoluissa.
Esto
Yksi keino kaspaasin estämiseen on IAP (apoptoosin estäjä) -proteiiniperheen kautta, joka sisältää c-IAP1, c-IAP2, XIAP ja ML-IAP. XIAP sitoo ja estää initiaattorikaspaasi-9: n, joka on suoraan mukana teloittajakaspaasi-3: n aktivaatiossa. Kaspaasikaskadin aikana kaspaasi-3 kuitenkin estää XIAP-aktiivisuuden katkaisemalla kaspaasi-9: n tietystä kohdasta estäen XIAP: n kykenemästä sitoutumaan estämään kaspaasi-9-aktiivisuutta.
Vuorovaikutukset
Caspase 3: n on osoitettu olevan vuorovaikutuksessa seuraavien kanssa:
Biologinen toiminta
Kaspaasi-3: n on todettu olevan välttämätön aivojen normaalille kehitykselle sekä sen tyypilliselle roolille apoptoosissa, jossa se on vastuussa kromatiinin tiivistymisestä ja DNA: n pirstoutumisesta. Kaspase-3, p17-fragmentin kohonneet tasot verenkierrossa ovat merkki äskettäisestä sydäninfarktista . Nyt on osoitettu, että kaspaasi-3: lla voi olla rooli alkion ja hematopoieettisten kantasolujen erilaistumisessa.
Katso myös
Viitteet
Lue lisää
- Cohen GM (elokuu 1997). "Kaspaasit: apoptoosin teloittajat" . The Biochemical Journal . 326 (Pt 1): 1–16. doi : 10.1042/bj3260001 . PMC 1218630 . PMID 9337844 .
- Roig J, Traugh JA (2001). Sytostaattinen p21 G -proteiiniaktivoitu proteiinikinaasi gamma-PAK . Vitamiinit & Hormonit. 62 . s. 167–98. doi : 10.1016/S0083-6729 (01) 62004-1 . ISBN 9780127098623. PMID 11345898 .
- Zhao LJ, Zhu H (joulukuu 2004). "HIV-1-lisäsäätelyproteiinin Vpr rakenne ja toiminta: uusia vihjeitä lääkkeen suunnitteluun". Nykyiset huumetavoitteet. Immuunijärjestelmä, hormonaaliset ja aineenvaihduntahäiriöt . 4 (4): 265–75. doi : 10.2174/1568008043339668 . PMID 15578977 .
- Le Rouzic E, Benichou S (2006). "HIV-1: n Vpr-proteiini: erilliset roolit viruksen elinkaaren aikana" . Retrovirologia . 2 (1): 11. doi : 10.1186/1742-4690-2-11 . PMC 554975 . PMID 15725353 .
- Sykes MC, Mowbray AL, Jo H (helmikuu 2007). "Kaspaasi-3: n palautuva glutationilaatio glutaredoksiinilla uutena redoksisignaalimekanismina tuumorinekroositekijä-alfa-indusoidussa solukuolemassa" . Kiertotutkimus . 100 (2): 152–4. doi : 10.1161/01.RES.0000258171.08020.72 . PMID 17272816 .
Ulkoiset linkit
- Merops Online tietokanta peptidaaseja ja niiden estäjät: C14.003
- Apoptoosin & Kaspaasi 3 - proteolyysi Kartta -animaatio