Papillomaviridae -Papillomaviridae
Papillomaviridae on vaipattomien DNA-virusten perhe ,jonka jäseniä kutsutaan papilloomaviruksiksi. On tunnistettu useita satoja papilloomaviruslajeja, joita perinteisesti kutsutaan "tyypeiksi" ja jotka tartuttavat kaikkia huolellisesti tutkittuja nisäkkäitä, mutta myös muita selkärankaisia , kuten lintuja, käärmeitä, kilpikonnia ja kaloja. Useimpien papilloomavirustyyppien aiheuttama infektio on tyypistä riippuen joko oireeton (esim. Useimmat beeta-PV: t) tai aiheuttaa pieniä hyvänlaatuisia kasvaimia, jotka tunnetaan nimellä papilloomat tai syyliä (esim. Ihmisen papilloomavirus 1, HPV6 tai HPV11). Joidenkin tyyppien aiheuttamat papilloomat, kuten ihmisen papilloomavirukset 16 ja 18, aiheuttavat kuitenkin syöpää .
Papillomavirukset yleensä pidetään erittäin host- ja kudoksille tropiikissa , ja niiden ajatellaan harvinaisissa tapauksissa tarttua lajien välillä. Papilloomavirukset toistaa yksinomaan tyvikerroksen ja kehon pinnan kudoksiin . Kaikki tunnetut papilloomavirustyypit tartuttavat tietyn kehon pinnan, tyypillisesti sukupuolielinten, peräaukon, suun tai hengitysteiden ihon tai limakalvon epiteelin. Esimerkiksi tyypin 1 ihmisen papilloomavirus (HPV) pyrkii tartuttamaan jalkapohjia ja tyypin 2 HPV -kämmenet, joissa ne voivat aiheuttaa syyliä . Lisäksi on kuvauksia papilloomaviruksen DNA : n läsnäolosta veressä ja perifeerisen veren mononukleaarisoluissa .
Papilloomavirukset tunnistettiin ensimmäisen kerran 1900 -luvun alussa, kun osoitettiin, että suodatettava tartunnanaiheuttaja voi siirtää ihosyylät tai papilloomat yksilöiden välillä. Vuonna 1935 Francis Peyton Rous , joka oli aiemmin osoittanut syöpää aiheuttavan sarkoomaviruksen olemassaolon kanoilla, osoitti edelleen, että papilloomavirus voi aiheuttaa ihosyöpää tartunnan saaneilla kaneilla. Tämä oli ensimmäinen osoitus siitä, että virus voi aiheuttaa syöpää nisäkkäillä.
Papilloomavirusten taksonomia
Tunnistetaan yli 100 papilloomaviruslajia, vaikka ICTV tunnistaa virallisesti pienemmän määrän, luokiteltuina 53 sukuun, vuodesta 2019 lähtien. Kaikilla papilloomaviruksilla (PV) on samankaltaiset genomiset organisaatiot, ja jokainen PV -pari sisältää vähintään viisi homologista geeniä , vaikka nukleotidisekvenssi voi poiketa enemmän kuin 50%. Fylogeneettiset algoritmit, jotka mahdollistavat homologioiden vertailun, johtivat fylogeneettisiin puihin , joilla on samanlainen topologia, riippumatta analysoidusta geenistä.
Fylogeneettiset tutkimukset viittaavat vahvasti siihen, että PV: t kehittyvät normaalisti yhdessä nisäkkäiden ja lintujen isäntälajien kanssa, mutta adaptiivinen säteily , satunnaiset zoonoottiset tapahtumat ja rekombinaatiot voivat myös vaikuttaa niiden monipuolistumiseen. Niiden perusgenominen organisaatio näyttää säilyneen yli 100 miljoonan vuoden ajan, ja nämä sekvenssivertailut ovat luoneet perustan PV -taksonomialle, jonka kansainvälinen virusten taksonomiakomitea on nyt virallisesti tunnustanut . Kaikki PV: t muodostavat Papillomaviridae -perheen , joka eroaa Polyomaviridae -heimoista ja eliminoi termin Papovaviridae . PV: n fylogeneettisen puun tärkeimpiä oksia pidetään sukuina , jotka tunnistetaan kreikkalaisilla kirjaimilla. Pieniä oksia pidetään lajeina ja ne yhdistävät PV -tyyppejä, jotka ovat genomisesti erilaisia, mutta niillä ei ole tunnettuja biologisia eroja. Tämä uusi taksonominen järjestelmä ei vaikuta perinteiseen PV -tyyppien ja niiden itsenäisten isolaattien tunnistamiseen ja karakterisointiin, joilla on pieniä genomisia eroja, joita kutsutaan "alatyypeiksi" ja "variantteiksi", jotka kaikki ovat taksoneja "lajin" tason alapuolella. Lisäksi on ehdotettu fylogeneettisiä ryhmittelyjä korkeammalla taksonomisella tasolla.
Tämä luokitus saattaa vaatia tarkistusta, kun otetaan huomioon papillooma -polyooma -viruksen rekombinanttien olemassaolo. Myös muita lajeja on kuvattu. Sparus aurata papilloomavirus 1 on eristetty kaloista.
Ihmisen papilloomavirukset
Yli 170 ihmisen papilloomavirustyyppiä on sekvensoitu kokonaan. Ne on jaettu viiteen sukuun: Alfapapillomavirus, Betapapillomavirus, Gammapapillomavirus, Mupapillomavirus ja Nupapillomavirus. Ainakin 200 virusta on tunnistettu, jotka odottavat sekvensointia ja luokittelua.
Eläinten papilloomavirukset
Yksittäiset papilloomavirustyypit ovat yleensä hyvin sopeutuneita yhden eläinlajin replikaatioon. Eräässä tutkimuksessa tutkijat pyyhkäisivät useiden eläintarhaeläinten otsan ihon ja monistivat PCR: llä mahdollisen papilloomaviruksen DNA: n. Vaikka tutkimuksessa tunnistettiin laaja valikoima papilloomavirussekvenssejä, kirjoittajat löysivät vain vähän todisteita lajien välisestä tartunnasta. Yksi eläintenhoitaja havaittiin olevan ohimenevästi positiivinen simpanssille spesifiselle papilloomavirusjaksolle. Kirjoittajat huomauttavat kuitenkin, että simpanssispesifinen papilloomavirussekvenssi olisi voinut olla seurausta eläintenhoitajan ihon pintasaastumisesta, toisin kuin tuottava infektio.
Cottontail -kanin papilloomavirus (CRPV) voi aiheuttaa ulkonevia syyliä alkuperäisessä isännässään, Pohjois -Amerikan kanin suvussa Sylvilagus . Nämä sarvi kaltainen syyliä voi olla alkuperäisen perustan kaupunkien legendaa amerikkalaisen antlered kaniinikilogrammaa Jackalope ja Euroopan Wolpertinger . Eurooppalaiset kotikanit (suku Oryctolagus ) voivat saada ohimenevän tartunnan CRPV -laboratoriossa. Koska eurooppalaiset kotikanit eivät kuitenkaan tuota tarttuvaa jälkeläisvirusta, niitä pidetään CRPV: n satunnaisena tai "umpikujaisena" isäntänä.
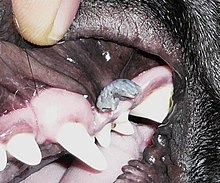
Lajien välinen siirto on myös dokumentoitu nautaeläinten papilloomaviruksen (BPV) tyypin 1 osalta. Luonnollisessa isännässään (naudat) BPV-1 aiheuttaa suuria kuituisia ihosyyliä. Hevosen BPV-1-infektio, joka on viruksen satunnainen isäntä, voi johtaa sarkoideiksi kutsuttujen hyvänlaatuisten kasvainten kehittymiseen . BPV-1: n maataloudellinen merkitys kannusti onnistuneesti pyrkimään kehittämään rokote virusta vastaan.
Muutamissa raporteissa on havaittu papilloomaviruksia pienemmissä jyrsijöissä, kuten syyrialaisissa hamstereissa , afrikkalaisessa multimammate -rotassa ja Euraasian sadonkorjuuhiirissä . Kuitenkin, ei ole olemassa papilloomavirukset tiedetään kykenee infektoimaan laboratorio hiirillä . Papilloomavirusinfektion hoidettavan hiirimallin puute on ollut merkittävä rajoitus papilloomavirusten laboratoriotutkimuksille.
Neljän papilloomaviruksen tiedetään tartuttavan lintuja: Fringilla coelebs papillomavirus 1, Francolinus leucoscepus papillomavirus 1, Psittacus erithacus papillomavirus 1 ja Pygoscelis adeliae papillomavirus 1. Kaikilla näillä lajeilla on tuntematon geeni (E9), mikä viittaa yhteiseen alkuperään.
Evoluutio
Papilloomavirusten kehittymisen uskotaan olevan hidas verrattuna moniin muihin virustyyppeihin, mutta kokeellisia mittauksia ei ole tällä hetkellä saatavilla. Tämä johtuu todennäköisesti siitä, että papilloomaviruksen genomi koostuu geneettisesti stabiilista kaksijuosteisesta DNA: sta, jota isäntäsolun DNA-replikaatiokoneisto replikoi suurella tarkkuudella.
Uskotaan, että papilloomavirukset kehittyvät yleensä yhdessä tietyn isäntäeläinlajin kanssa monien vuosien ajan, vaikka koevolution-hypoteesia vastaan on vahvoja todisteita. Erityisen nopeassa esimerkissä HPV-16 on kehittynyt hieman ihmispopulaatioiden laajentuessa ympäri maailmaa ja vaihtelee nyt eri maantieteellisillä alueilla tavalla, joka todennäköisesti heijastaa ihmisten muuttoliikkeen historiaa. Kutaneotrooppisia HPV -tyyppejä vaihdetaan toisinaan perheenjäsenten välillä koko elämän ajan, mutta myös muita luovuttajia tulisi harkita viruksen siirtämisessä.
Muut HPV-tyypit, kuten HPV-13, vaihtelevat suhteellisen vähän eri ihmispopulaatioissa. Itse asiassa HPV-13-sekvenssi muistuttaa läheisesti bonobojen papilloomavirusta (tunnetaan myös nimellä pygmy simpanssit). Ei ole selvää, johtuuko tämä samankaltaisuus viimeaikaisesta leviämisestä lajien välillä vai siitä, että HPV-13 on yksinkertaisesti muuttunut hyvin vähän kuuden miljoonan vuoden aikana ihmisten ja bonobojen eron jälkeen.
Tämän virusryhmän viimeisimmän yhteisen esi -isän on arvioitu olleen olemassa 424 miljoonaa vuotta sitten .
Ihmisiin tarttuu viisi pääasiallista sukua (alfa, beta, gamma, mu ja nu). Näiden sukujen viimeisin yhteinen esi -isä kehittyi 49,7 miljoonaa vuotta sitten - 58,5 miljoonaa vuotta sitten . Gamma -suvun uusimman esi -isän arvioitiin kehittyneen 45,3 miljoonan vuoden ja 67,5 miljoonan vuoden välillä .
Rakenne
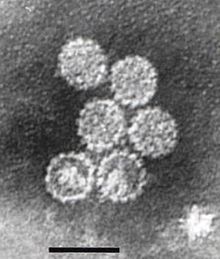
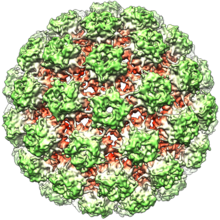
Papilloomavirukset ovat vaipattomia, mikä tarkoittaa, että ulkovaippa tai kapsidin viruksen ei kuulu lipidi kalvo . Yksi virusproteiini, joka tunnetaan nimellä L1, on välttämätön ja riittävä muodostamaan 55–60 nanometrin kapsidin, joka koostuu 72 tähden muotoisesta kapsomeeristä (katso kuva). Kuten useimmat vaipattomat virukset, kapsidi on geometrisesti säännöllinen ja siinä on ikosaedrinen symmetria . Itse kootut viruksen kaltaiset hiukkaset, jotka koostuvat L1: stä, ovat perusta onnistuneelle ryhmälle ennaltaehkäiseviä HPV-rokotteita, jotka on suunniteltu tuottamaan viruksia neutraloivia vasta - aineita, jotka suojaavat HPV-infektiota vastaan. Sellaisena papilloomaviridæ ovat stabiileja ympäristössä .
Papilloomaviruksen genomi on kaksijuosteinen pyöreä DNA-molekyyli , jonka pituus on ~ 8000 emäsparia . Se on pakattu L1 -kuoreen yhdessä solujen histoniproteiinien kanssa , jotka palvelevat DNA: n käärimistä ja tiivistämistä.
Papilloomaviruksen kapsidi sisältää myös virusproteiinin, joka tunnetaan nimellä L2, joka on vähemmän runsas. Vaikka ei ole selvää, miten L2 on järjestetty virioniin, sen tiedetään suorittavan useita tärkeitä toimintoja, mukaan lukien helpottavan viruksen genomin pakkaamista syntyviin virioneihin sekä viruksen tarttuvaa pääsyä uusiin isäntäsoluihin. L2 on kiinnostava mahdollinen kohde laajemmin suojaaville HPV -rokotteille .
Viruksen kapsiidi koostuu 72 kapsomeeristä, joista 12 on viisi koordinoitua ja 60 on kuuden koordinoidun kapsomeerin, jotka on järjestetty T = 7d ikosaedriseen pintahilaan.
Kudoksen spesifisyys
Papilloomavirukset replikoituvat yksinomaan keratinosyyteissä . Keratinosyytit muodostavat ihon uloimmat kerrokset sekä joitain limakalvopintoja , kuten posken sisäpuolen tai emättimen seinät. Nämä pintakudokset, jotka tunnetaan kerrostuneena lantionepiteelinä , koostuvat pinotuista kerroksista litistyneitä soluja. Solukerrokset muodostuvat solujen erilaistumisena tunnetulla prosessilla , jossa keratinosyytit vähitellen erikoistuvat muodostaen lopulta kovan, silloitetun pinnan, joka estää kosteuden menetyksen ja toimii esteenä patogeenejä vastaan. Vähemmän erilaistuneita keratinosyyttien kantasoluja, joita täydennetään pintakerroksessa, uskotaan olevan tuottavien papilloomavirusinfektioiden alkuperäinen kohde. Viruksen elinkaaren myöhemmät vaiheet ovat tiukasti riippuvaisia keratinosyyttien erilaistumisprosessista. Tämän seurauksena papilloomavirukset voivat lisääntyä vain kehon pinnan kudoksissa.
Elinkaari
Tarttuva merkintä
Papilloomavirukset pääsevät keratinosyyttien kantasoluihin ihon tai limakalvojen pienten haavojen kautta, jotka tunnetaan mikrotraumoina. L1: n ja sulfatoituneiden sokerien väliset vuorovaikutukset solun pinnalla edistävät viruksen ensimmäistä kiinnittymistä. Virus kykenee sitten pääsemään sisälle solun pinnalta vuorovaikutuksessa tietyn reseptorin kanssa, todennäköisesti alfa-6-beeta-4-integriinin kautta, ja kuljettamaan kalvon ympäröimiin rakkuloihin, joita kutsutaan endosomeiksi . Kapsidiproteiini L2 rikkoo endosomin kalvon kationisen solun läpäisevän peptidin kautta , jolloin viruksen genomi voi paeta ja liikkua yhdessä L2: n kanssa solun ytimeen.
Viruksellinen pysyvyys
Onnistuneen keratinosyytti -infektion jälkeen virus ilmentää E1- ja E2 -proteiineja, jotka on tarkoitettu replikoimaan ja ylläpitämään virus -DNA: ta pyöreänä episomina . Viruksen onkogeenit E6 ja E7 edistävät solujen kasvua inaktivoimalla tuumorisuppressoriproteiinit p53 ja pRb . Keratinosyyttien kantasolut epiteelin kellarikerroksessa voivat ylläpitää papilloomaviruksen genomeja vuosikymmeniä.
Jälkeläisviruksen tuotanto
Viruksen myöhäisten geenien, L1 ja L2, ilmentyminen rajoittuu yksinomaan ihon tai limakalvon pinnan uloimpien kerrosten erilaistuviin keratinosyyteihin. L1: n ja L2: n lisääntynyt ilmentyminen korreloi tyypillisesti virusgenomin kopioiden määrän dramaattisen kasvun kanssa. Koska kerrostuneen levyepiteelin ulommat kerrokset ovat suhteellisen rajoitetusti immuunijärjestelmän solujen valvonnan alaisia, uskotaan, että tämä viruksen myöhäisen geeniekspression rajoitus edustaa erästä immuunijärjestelmän kiertämistä.
Uudet tarttuvat jälkeläisvirukset kootaan solun ytimeen . Papilloomavirukset ovat kehittäneet mekanismin virionien vapauttamiseksi ympäristöön. Muunlaisia vaipattomia eläinviruksia käytetään aktiivisessa lyyttisessä prosessissa tappamaan isäntäsolu, mikä mahdollistaa jälkeläisviruspartikkeleiden vapautumisen. Usein tämä lyyttinen prosessi liittyy tulehdukseen , joka voi laukaista immuunikohtauksen virusta vastaan. Papilloomavirukset hyödyntävät hilseilyä salamyhkäisenä, ei-tulehduksellisena vapautumismekanismina.
| Suku | Isännän tiedot | Kudosten tropismi | Ilmoittautumisen tiedot | Julkaisutiedot | Toistosivusto | Kokoontumispaikka | Tarttuminen |
|---|---|---|---|---|---|---|---|
| Dyoxipapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Omikronpapillomavirus | Pyöriäiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyodeltapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Omegapapillomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Nupapillomavirus | Ihmiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyomupapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyozetapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Kappapapillomavirus | Kanit | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Upsilonpapillomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyoetapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Sigmapapillomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Lambdapapillomavirus | Kissat; koiria | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Taupapillomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Betapapillomavirus | Ihmiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Xipapillomavirus | Nautaeläimet | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyoepsilonpapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Thetapapillomavirus | Linnut | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Etapapillomavirus | Linnut | Epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Rhopapilloomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyothetapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyoomikronpapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Gammapapillomavirus | Ihmiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Alfapapillomavirus | Ihmiset; apinoita | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Seksi; ottaa yhteyttä |
| Zetapapillomavirus | Hevoset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Deltapapillomavirus | Märehtijät | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyolambdapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyosigmapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyorhopapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Psipapilloomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyokappapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Pipapilloomavirus | Hamsterit | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Iotapapillomavirus | Jyrsijät | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Epsilonpapillomavirus | Nautaeläimet | Epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Phipapillomavirus | Selkärankaiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyonupapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyopipapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Dyoiotapapillomavirus | Selkärankaiset | Ei mitään | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
| Mupapillomavirus | Ihmiset | Epiteeli: limakalvo; epiteeli: iho | Solureseptorin endosytoosi | Lysis | Ydin | Ydin | Ottaa yhteyttä |
Yhteys syöpään
Vaikka jotkut papilloomavirustyypit voivat aiheuttaa syöpää niiden asuttamissa epiteelikudoksissa, syöpä ei ole tyypillinen infektion tulos. Papilloomaviruksen aiheuttamat syövät kehittyvät tyypillisesti monien vuosien aikana. Papilloomavirukset on yhdistetty kohdunkaulasyövän , peniksen syövän ja suun syöpien kehittymiseen . On myös havaittu yhteys vulvaalisyöpään ja uroteelisyöpään, joilla on okasolumuotoinen erilaistuminen potilailla, joilla on neurogeeninen virtsarakko. On syöpää aiheuttavaa papilloomaviruksen genomia, joka koodaa kahta pientä proteiinia nimeltä E6 ja E7, jotka jäljittelevät syöpää aiheuttavia onkogeenejä. He toimivat siten, että ne stimuloivat solujen luonnotonta kasvua ja estävät niiden luonnollisen puolustuksen. Lisäksi ne vaikuttavat moniin signalointiproteiineihin, jotka kontrolloivat lisääntymistä ja apoptoosia.
Laboratoriotutkimus
Se, että papilloomaviruksen elinkaari vaatii ehdottomasti keratinosyyttien erilaistumista, on muodostanut merkittävän esteen papilloomavirusten tutkimukselle laboratoriossa, koska se on estänyt tavanomaisten solulinjojen käytön virusten kasvattamiseen. Koska tarttuvia BPV-1-virioneja voidaan erottaa suurista syyliistä, joita virus aiheuttaa naudoille, se on ollut työhevosmallin papilloomavirustyyppi monien vuosien ajan. CRPV: tä, kanin suun papilloomavirusta (ROPV) ja koiran suun papilloomavirusta (COPV) on myös käytetty laajasti laboratoriotutkimuksissa. Heti kun tutkijat havaitsivat, että nämä virukset aiheuttavat syöpää, he löysivät yhdessä rokotteen sille. Tällä hetkellä tehokkain tapa edetä on jäljitellä virus, joka koostuu L1 -proteiinista, mutta josta puuttuu DNA. Pohjimmiltaan immuunijärjestelmämme rakentaa suojaa infektioita vastaan, mutta jos nämä infektiot eivät aiheuta sairautta, niitä voidaan käyttää rokotteena. ATE: n 6bt3 kohta osoittaa, kuinka vasta -ainepinnat hyökkäävät viruksen pintaan estääkseen sen.
Joitakin sukupuoliteitse tarttuvia HPV-tyyppejä on lisätty käyttämällä hiiren "ksenografti" -järjestelmää, jossa HPV-tartunnan saaneet ihmissolut istutetaan immuunipuutteisiin hiiriin . Viime aikoina jotkut ryhmät ovat onnistuneet eristämään tarttuvan HPV-16: n ihmisen kohdunkaulan leesioista. Kuitenkin tarttuvien virionien eristäminen tällä tekniikalla on vaivalloista ja tarttuvan viruksen saanto on hyvin alhainen.
Keratinosyyttien erilaistumista voidaan jäljitellä in vitro altistamalla viljellyt keratinosyytit ilman/nesteen rajapinnalle. Tällaisten "lautaviljelmä" -järjestelmien mukauttaminen papilloomavirusten tutkimukseen oli merkittävä läpimurto viruksen elinkaaren in vitro -tutkimuksessa. Lautaviljelyjärjestelmät ovat kuitenkin suhteellisen raskaita ja tarttuvien HPV: iden saanto voi olla alhainen.
Hiivapohjaisen järjestelmän kehittäminen, joka mahdollistaa vakaan episomaalisen HPV-replikaation, tarjoaa kätevän, nopean ja edullisen tavan tutkia useita HPV-elinkaaren näkökohtia (Angeletti 2002). Esimerkiksi E2-riippuvainen transkriptio, genomin monistaminen ja täyspitkien HPV-DNA: iden tehokas kapselointi voidaan helposti luoda hiivassa (Angeletti 2005).
Äskettäin on kehitetty ohimeneviä suuren saannon menetelmiä reportterigeenejä kantavien HPV- pseudovirusten tuottamiseksi . Vaikka pseudovirukset eivät sovellu viruksen elinkaaren tiettyjen näkökohtien tutkimiseen, alustavat tutkimukset viittaavat siihen, että niiden rakenne ja tartunnan alkaminen soluihin on todennäköisesti monella tapaa samanlainen kuin aitojen papilloomavirusten.
Ihmisen papilloomavirus sitoutuu tartunnan saaneiden solujen pinnalla oleviin hepariinimolekyyleihin. Tutkimukset ovat osoittaneet, että eristettyjen L1 -kapsomeerien kiteessä on lysiinien tunnistamat hepariiniketjut, jotka viivat urat viruksen pinnalla. Myös vasta -aineita omaavat osoittavat, että ne voivat estää tämän tunnistamisen.
Geneettinen organisaatio ja geenien ilmentyminen
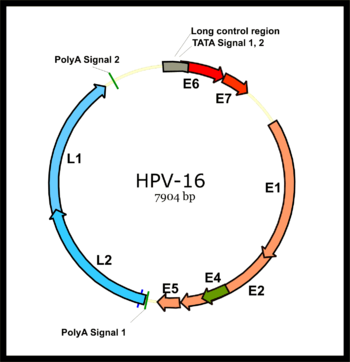
Papilloomaviruksen genomi on jaettu varhaiseen alueeseen (E), joka koodaa kuutta avointa lukukehystä (ORF) (E1, E2, E4, E5, E6 ja E7), jotka ilmentyvät välittömästi isäntäsolun ensimmäisen infektion jälkeen, ja myöhäinen alue (L), joka koodaa suurta kapsidiproteiinia L1 ja pientä kapsidiproteiinia L2. Kaikki virus -ORF: t on koodattu yhteen DNA -juosteeseen (katso kuva). Tämä edustaa dramaattista eroa papilloomavirusten ja polyomavirusten välillä , koska jälkimmäinen virustyyppi ilmentää varhaisia ja myöhäisiä geenejään molempien DNA-juosteiden kaksisuuntaisella transkriptiolla . Tämä ero oli merkittävä tekijä yhteisymmärryksen saavuttamisessa siitä, että papilloomaviruksilla ja polyomaviruksilla ei luultavasti koskaan ollut yhteistä esi -isää huolimatta niiden virionien rakenteista.
Kun isäntäsolu on infektoitu, HPV16: n varhainen promoottori aktivoidaan ja polysistroninen primaarinen RNA, joka sisältää kaikki kuusi varhaista ORF: ää, transkriboidaan. Tämä polysistroninen RNA sisältää kolme eksonia ja kaksi intronia ja käy läpi aktiivisen RNA -silmukoinnin useiden mRNA -isoformien muodostamiseksi. Yksi silmukoituista isoformi -RNA: sta, E6*I, toimii E7 -mRNA: na kääntämään E7 -onkoproteiinia. Sitä vastoin E6 ORF: n introni, joka pysyy ehjänä ilman silmukointia, on tarpeen E6 -onkoproteiinin translaatioon. Kuitenkin viruksen varhainen transkriptio altistaa viruksen E2 -säätelylle ja korkeille E2 -tasoille tukahduttaa transkription. HPV -genomit integroituvat isäntägenomiin katkaisemalla E2 ORF, estäen E2 -tukahduttamisen E6: ssa ja E7: ssä. Siten viruksen genomin integroituminen isäntä -DNA -genomiin lisää E6- ja E7 -ilmentymistä edistääkseen solujen lisääntymistä ja pahanlaatuisuuden mahdollisuutta.
Suuri viruksen myöhäispromoottori viruksen varhaisella alueella tulee aktiiviseksi vain erilaistuneissa soluissa ja sen aktiivisuutta voidaan tehostaa suuresti viruksen DNA: n replikaatiolla. Myöhäinen transkripti on myös polysistroninen RNA, joka sisältää kaksi intronia ja kolme eksonia. Tämän myöhäisen transkriptin vaihtoehtoinen RNA-silmukointi on välttämätöntä L1- ja L2-ilmentymiselle, ja sitä voidaan säätää RNA-cis-elementeillä ja isännän silmukointitekijöillä.
Tekninen keskustelu papilloomaviruksen geenitoiminnoista
Papilloomaviruksen genomissa olevat geenit tunnistetaan yleensä samankaltaisuuden jälkeen muiden aiemmin tunnistettujen geenien kanssa. Jotkut väärät avoimet lukukehykset saattoivat kuitenkin erehtyä geeneiksi yksinkertaisesti niiden sijainnin jälkeen genomissa, eivätkä ne välttämättä ole todellisia geenejä. Tämä koskee erityisesti tiettyjä avoimia lukukehyksiä E3, E4, E5 ja E8 .
E1
Koodaa proteiinin, joka sitoutuu viruksen replikaation alkukohtaan virusgenomin pitkällä kontrollialueella. E1 käyttää ATP: tä helikaasiaktiivisuuden aikaansaamiseksi, joka pakottaa DNA -juosteet erilleen, jolloin virusgenomi valmistellaan solujen DNA: n replikaatiotekijöiden replikaatiota varten .
E2
E2 -proteiini toimii pääasiallisena transkription säätelijänä viruksen promoottoreille, jotka sijaitsevat pääasiassa pitkällä kontrollialueella. Proteiinilla on transaktivaatiodomeeni, joka on liitetty suhteellisen jäsentämättömällä sarana-alueella hyvin karakterisoituun DNA: n sitomisalueeseen. E2 helpottaa E1: n sitoutumista replikaation viruslähteeseen. E2 käyttää myös soluproteiinia, joka tunnetaan nimellä Bromodomain -4 (Brd4) viruksen genomin sitomiseksi solukromosomeihin. Tämä kytkeminen solun ydinmatriisiin takaa viruksen genomien uskollisen jakautumisen jokaiselle tytärsolulle solunjakautumisen jälkeen. Uskotaan, että E2 toimii onkogeenien E6 ja E7 negatiivisena ilmentymisregulaattorina piilevästi HPV-tartunnan saaneissa peruskerroksen keratinosyyteissä . Geneettiset muutokset, kuten virus -DNA: n integrointi isäntäsolun kromosomiin, jotka inaktivoivat E2 -ilmentymisen, pyrkivät lisäämään E6- ja E7 -onkogeenien ilmentymistä, mikä johtaa solujen transformaatioon ja mahdollisesti edelleen geneettiseen epävakauteen.
E3
Tämä pieni oletettu geeni on olemassa vain muutamissa papilloomavirustyypeissä. Geenin ei tiedetä ilmentyvän proteiinina eikä sillä näytä olevan mitään tehtävää.
E4
Vaikka E4 -proteiineja ekspressoidaan alhaisella tasolla virusinfektion alkuvaiheessa, E4: n ilmentyminen lisääntyy dramaattisesti infektion myöhäisessä vaiheessa. Toisin sanoen sen "E" -nimitys voi olla jotain harhaanjohtavaa. HPV-1: n tapauksessa E4 voi muodostaa jopa 30% syylän pinnan kokonaisproteiinista. E4-proteiini Monien papilloomavirustyypeissä uskotaan helpottaa virionin levittämisestä ympäristöön hajottamalla välifilamenttejä Sarveiskalvosoluviljelyjen solun tukirangan . Virusmutantit, jotka eivät kykene ilmentämään E4: ää, eivät tue virus-DNA: n korkean tason replikaatiota, mutta ei ole vielä selvää, miten E4 helpottaa DNA: n replikaatiota. E4: n on myös osoitettu osallistuvan solujen pysäyttämiseen solusyklin G2 -vaiheessa .
E5
E5 ovat pieniä, hyvin hydrofobisia proteiineja, jotka epävakauttavat monien kalvoproteiinien toimintaa tartunnan saaneessa solussa. Joidenkin eläinten papilloomavirustyyppien (pääasiassa naudan papilloomaviruksen tyyppi 1) E5-proteiini toimii onkogeeninä ensisijaisesti aktivoimalla verihiutaleista peräisin olevien kasvutekijäreseptorien solujen kasvua edistävää signalointia . Syöpään liittyvät ihmisen papilloomavirusten E5 -proteiinit näyttävät kuitenkin aktivoivan signaalikaskadin, jonka epidermaalinen kasvutekijä käynnistää ligandin sitoutumisen yhteydessä. HPV16 E5: n ja HPV2 E5: n on myös osoitettu säätelevän alaspäin tärkeimpien luokan I histoyhteensopivuuskompleksien pinta-ilmentymistä , mikä voi estää tartunnan saaneita soluja poistamasta tappaja-T-soluja .
E6
E6 on 151 aminohappopeptidi, joka sisältää tyypin 1 motiivin konsensussekvenssillä- (T/S)-(X)-(V/I) -COOH. Siinä on myös kaksi sinkkisormikuviota .
E6 on erityisen kiinnostava, koska sillä näyttää olevan useita rooleja solussa ja se on vuorovaikutuksessa monien muiden proteiinien kanssa. Sen tärkein rooli on kuitenkin välittää p53: n , suuren tuumorisuppressoriproteiinin , hajoamista , mikä vähentää solun kykyä reagoida DNA -vaurioihin .
E6: n on myös osoitettu kohdistavan muita soluproteiineja muuttamalla siten useita metabolisia reittejä . Yksi tällainen kohde on NFX1-91 , joka tavallisesti estää telomeraasin tuotantoa , proteiinia, joka sallii solujen jakautumisen rajoittamattoman määrän kertoja. Kun E6 hajottaa NFX1-91, telomeraasipitoisuudet nousevat, mikä inaktivoi tärkeän mekanismin, joka pitää solujen kasvun kurissa. Lisäksi E6 voi toimia transkription kofaktorina - erityisesti transkription aktivaattorina - vuorovaikutuksessa solutranskriptiotekijän E2F1/DP1 kanssa.
E6 voi myös sitoutua PDZ-domeeneihin , lyhyisiin sekvensseihin, joita esiintyy usein signalointiproteiineissa. E6: n rakenteellinen motiivi mahdollistaa vuorovaikutuksen PDZ -domeenien kanssa DLG (levyt suuret) ja hDLG (Drosophila large) kasvainsuppressorigeeneissä. Sitoutuminen näihin paikkoihin aiheuttaa DLG -proteiinin muutoksen ja häiriöitä sen tukahdutustoiminnassa. E6-proteiinit ovat myös vuorovaikutuksessa MAGUK (kalvoon liittyvä guanylaattikinaasiperhe) -proteiinien kanssa. Nämä proteiinit, mukaan lukien MAGI-1, MAGI-2 ja MAGI-3, ovat yleensä rakenteellisia proteiineja ja voivat auttaa signaloinnissa. Vielä tärkeämpää on, että niiden uskotaan liittyvän DLG: n tukahduttamistoimintaan. Kun E6 kompleksoituu MAGI -proteiinien PDZ -domeenien kanssa, se vääristää niiden muotoa ja vaikeuttaa siten niiden toimintaa. Kaiken kaikkiaan E6 -proteiini estää normaalin proteiiniaktiivisuuden siten, että solu voi kasvaa ja lisääntyä syövälle ominaisella nopeutetulla nopeudella.
Koska E6: n ilmentyminen on ehdottomasti tarpeen pahanlaatuisen fenotyypin ylläpitämiseksi HPV-indusoiduissa syövissä, se on houkutteleva kohde terapeuttisille HPV-rokotteille, jotka on suunniteltu poistamaan vakiintuneet kohdunkaulasyövät.
E7
Useimmissa papilloomavirustyypeissä E7 -proteiinin ensisijainen tehtävä on inaktivoida tuumorisuppressoriproteiinien pRb -perheen jäsenet . Yhdessä E6: n kanssa E7 estää solukuoleman ( apoptoosin ) ja edistää solusyklin etenemistä, jolloin solu valmistetaan viruksen DNA: n replikaatiota varten. E7 osallistuu myös tartunnan saaneiden solujen kuolemattomuuteen aktivoimalla solujen telomeraasi . Kuten E6, myös E7 on tutkimuksen kohteena ja sen uskotaan aiheuttavan monenlaisia muita vaikutuksia tartunnan saaneisiin soluihin. Kuten E6: n tapauksessa, E7: n jatkuva ilmentyminen tarvitaan syöpäsolulinjojen, kuten HeLa: n , selviämiseen , jotka ovat peräisin HPV: n aiheuttamista kasvaimista.
E8
Vain muutama papilloomavirustyyppi koodaa lyhyttä proteiinia E8 -geenistä. Tapauksessa BPV-4 (papilloomaviruksen suku Xi ), E8 avoin lukukehys voi korvata E6 avoimen lukukehyksen, joka on läsnä tässä papilloomaviruksen sukuun. Nämä E8 -geenit ovat kemiallisesti ja toiminnallisesti samanlaisia kuin joidenkin ihmisen papilloomavirusten E5 -geenit, ja niitä kutsutaan myös E5/E8: ksi.
L1
L1 kokoontuu spontaanisti itsestään pentameerisiksi kapsomeereiksi. Puhdistetut kapsomeerit voivat muodostaa kapsideja, jotka stabiloidaan disulfidisidoksilla naapurimaiden L1 -molekyylien välillä. In vitro kootut L1 -kapsidit ovat perustana ennaltaehkäiseville rokotteille useita HPV -tyyppejä vastaan. Verrattuna muihin papilloomaviruksen geeneihin, useimpien L1-osien aminohapposekvenssit ovat hyvin konservoituneita eri tyyppien välillä. L1: n pintasilmukat voivat kuitenkin poiketa merkittävästi jopa tietyn papilloomaviruslajin eri jäsenille. Tämä todennäköisesti kuvastaa mekanismia, jolla vältetään neutraloivien vasta -ainevasteiden aikaisemmat papilloomavirusinfektiot.
L2
L2 on hapettuneessa tilassa papilloomaviruksen virionissa, ja kaksi konservoitua kysteiinitähdettä muodostavat molekyylisisäisen disulfidisidoksen . Sen lisäksi, että L2 on toiminut yhteistyössä L1: n kanssa viruksen DNA: n pakkaamiseksi virioniin, sen on osoitettu olevan vuorovaikutuksessa useiden soluproteiinien kanssa tarttuvan sisäänmenoprosessin aikana. Alkuvaiheen jälkeen sitova virionin soluun, L2 on pilkkoa solun proteaasi furiinin . Virioni sisäistetään luultavasti klatriinivälitteisen prosessin kautta endosomiksi, jossa happamien olosuhteiden uskotaan johtavan L2: n kalvoa epävakauttavien osien altistumiseen. Soluproteiinit beeta- aktiini ja syntaksiini -18 voivat myös osallistua L2-välitteisiin tapahtumiin. Endosomipakoilun jälkeen L2 ja viruksen genomi tuodaan solun ytimeen, missä ne kulkevat ND-10 -kehoksi tunnetulle ydinalialueelle, joka on runsaasti transkriptiotekijöitä . Pienet L2-osat ovat hyvin säilyneitä eri papilloomavirustyyppien välillä, ja näihin konservoituneisiin alueisiin kohdistuvat kokeelliset rokotteet voivat tarjota suojaa monenlaisia HPV-tyyppejä vastaan.
Katso myös
Viitteet
Ulkoiset linkit
- ICTV -raportti Papillomaviridae
- Virusvyöhyke : Papillomaviridae
- Los Alamos National Laboratory on kattava (vaikkakin hieman päivätty) papilloomaviruksen järjestyksessä tietokantaan . Tämä hyödyllinen tietokanta sisältää yksityiskohtaisia kuvauksia ja viittauksia eri papilloomavirustyypeille.
- Lyhyt video, joka osoittaa papilloomaviruksen vaikutukset indonesialaisen miehen iholle, jolla on epidermodysplasia verruciformis eli geneettinen kyvyttömyys puolustautua tietyntyyppisiä ihon HPV: tä vastaan.
- [2] de Villiers, EM, Bernard, HU, Broker, T., Delius, H. ja zur Hausen, H. Virusindeksi - Papillomaviridae (2006). Julkaisussa: ICTVdB-The Universal Virus Database, versio 4. Büchen-Osmond, C (toim.), Columbia University, New York, USA.
- 00.099. Papillomaviridae kuvaus julkaisussa: ICTVdB-The Universal Virus Database, versio 4. Büchen-Osmond, C. (toim.), Columbia University, New York, USA
- Ihmisen papilloomaviruspartikkelin ja genomin visualisointi
- ICTV