Fc -reseptori - Fc receptor
| Immunoglobuliinin kaltainen reseptori | |
|---|---|
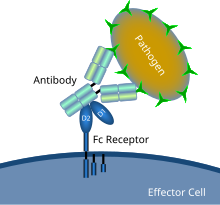 Kaavio, joka esittää Fc-reseptorin vuorovaikutusta vasta-aineella päällystetyn mikrobipatogeenin kanssa
| |
| Tunnisteet | |
| Symboli | Fc -reseptori |
| Membranomi | 10 |
Fc-reseptori on proteiini löytyy tiettyjen solujen pinnalla - mukaan lukien, muun muassa, B-lymfosyytit , follikulaariset dendriittisolut , luonnollisten tappajasolujen , makrofaagit , neutrofiilit , eosinofiilit , basofiilit , ihmisen verihiutaleet , ja syöttösolut - jotka edistävät suojaava immuunijärjestelmän toiminnot . Sen nimi on johdettu sen sitoutumisspesifisyydestä Fc (kiteytyvä fragmentti) -alueena tunnetulle vasta -aineelle . Fc -reseptorit sitoutuvat vasta -aineisiin, jotka ovat kiinnittyneet tartunnan saaneisiin soluihin tai tunkeutuvat patogeeneihin . Niiden aktiivisuus stimuloi fagosyyttisiä tai sytotoksisia soluja tuhoamaan mikrobeja tai tartunnan saaneita soluja vasta-ainevälitteisen fagosytoosin tai vasta-aineesta riippuvaisen soluvälitteisen sytotoksisuuden vuoksi . Jotkut virukset , kuten flavivirukset, käyttävät Fc-reseptoreita auttamaan heitä tartuttamaan soluja mekanismilla, joka tunnetaan vasta-aineesta riippuvaisena infektion tehostamisena .
Luokat
On olemassa useita erityyppisiä Fc -reseptoreita (lyhennetty FcR), jotka luokitellaan tunnistetun vasta -aineen tyypin perusteella . Latinalainen kirjain, jota käytetään vasta -aineen tunnistamiseen, muutetaan vastaavaksi kreikkalaiseksi kirjaimeksi, joka sijoitetaan nimen Fc -osan perään. Esimerkiksi niitä, jotka sitovat yleisimmän vasta -aineryhmän , IgG: n , kutsutaan Fc-gamma-reseptoreiksi (FcyR), niitä, jotka sitovat IgA: ta, kutsutaan Fc-alfa-reseptoreiksi (FcαR) ja niitä, jotka sitovat IgE: tä, kutsutaan Fc-epsilon-reseptoreiksi ( FcεR). FcR -luokat erottuvat myös niitä ilmentävistä soluista (makrofagit, granulosyytit, luonnolliset tappajasolut, T- ja B -solut) ja kunkin reseptorin signalointiominaisuuksista.
Fc-gamma-reseptorit
Kaikki Fcy-reseptorien (FcyR) kuuluvat immunoglobuliinisuperperhe ja ovat tärkeimmät Fc-reseptoreihin indusoi fagosytoosin ja opsonisoitiin (merkitty) mikrobit. Tähän perheeseen kuuluu useita jäseniä, FcyRI (CD64), FcyRIIA ( CD32 ), FcyRIIB (CD32), FcyRIIIA (CD16a), FcyRIIIB (CD16b), jotka eroavat toisistaan vasta -aine affiniteeteista eri molekyylirakenteensa vuoksi . Esimerkiksi FcyRI sitoutuu IgG: hen voimakkaammin kuin FcyRII tai FcyRIII. FcyRI: llä on myös solunulkoinen osa, joka koostuu kolmesta immunoglobuliinin (Ig) kaltaisesta domeenista , yksi domeeni enemmän kuin FcyRII: llä tai FcyRIII: lla. Tämän ominaisuuden ansiosta FcyRI voi sitoa ainoan IgG -molekyylin (tai monomeerin ), mutta kaikkien Fcy -reseptorien on sitottava useita IgG -molekyylejä immuunikompleksissa aktivoituakseen.
Fc-gamma-reseptorit eroavat toisistaan affiniteetiltaan IgG: hen ja samoin eri IgG-alaluokilla on ainutlaatuisia affiniteetteja jokaiseen Fc-gammareseptoriin. Näitä vuorovaikutuksia virittää edelleen glykaani (oligosakkaridi) IgG: n asemassa CH2-84,4. Esimerkiksi luomalla steerinen este, fukoosi, joka sisältää CH2-84,4-glykaaneja, vähentää IgG-affiniteettia FcyRIIIA: ta kohtaan. Sitä vastoin G0 -glykaaneilla, joista puuttuu galaktoosi ja jotka päättyvät GlcNAc -osiin, on lisääntynyt affiniteetti FcyRIIIA: ta kohtaan.
Toinen FcR on ilmaistu useita solutyyppejä, ja se on rakenteeltaan samanlainen kuin MHC-luokan I . Tämä reseptori sitoo myös IgG: tä ja osallistuu tämän vasta -aineen säilyttämiseen. Kuitenkin, koska tämä Fc-reseptori osallistuu myös siirtää IgG äidiltä joko kautta istukan hänen sikiöön tai maidon hänen imeville pikkulasten , sitä kutsutaan vastasyntyneen Fc-reseptorin ( FcRn ). Äskettäin tutkimukset viittasivat siihen, että tällä reseptorilla on rooli IgG -seerumitasojen homeostaasissa.
Fc-alfa-reseptorit
Vain yksi Fc -reseptori kuuluu FcαR -alaryhmään, jota kutsutaan FcαRI: ksi (tai CD89: ksi). FcαRI löytyy neutrofiilien , eosinofiilien, monosyyttien, joidenkin makrofagien (mukaan lukien Kupffer -solut ) ja joidenkin dendriittisolujen pinnalta . Se koostuu kahdesta solunulkoisesta Ig: n kaltaisesta domeenista, ja se on sekä immunoglobuliinin superperheen että moniketjuisen immuunijärjestelmän (MIRR) perheen jäsen. Se signaloi yhdistämällä kaksi FcRγ -signalointiketjua. Toinen reseptori voi myös sitoa IgA: ta, vaikka sillä on suurempi affiniteetti toiseen IgM -nimiseen vasta -aineeseen . Tätä reseptoria kutsutaan Fc-alfa/mu-reseptoriksi (Fcα/μR) ja se on tyypin I transmembraaniproteiini . Kun yksi Ig: n kaltainen domeeni on solunulkoisessa osassaan, tämä Fc-reseptori on myös immunoglobuliinin superperheen jäsen.
Fc-epsilon-reseptorit
Kaksi FcεR -tyyppiä tunnetaan:
- korkean affiniteetin reseptori FcRI on immunoglobuliinin superperheen jäsen (sillä on kaksi Ig: n kaltaista domeenia). FcεRI löytyy epidermaalisista Langerhansin soluista , eosinofiileistä, syöttösoluista ja basofiileistä. Tällä reseptorilla on solujakautumisensa vuoksi tärkeä rooli allergisten vasteiden kontrolloinnissa . FcεRI: tä ekspressoidaan myös antigeenia esittelevissä soluissa ja se ohjaa tulehdusta edistävien tärkeiden immuunivälittäjien, sytokiinien , tuotantoa .
- alhaisen affiniteetin reseptori FcεRII ( CD23 ) on C-tyypin lektiini . FcεRII: llä on useita toimintoja kalvoon sitoutuneena tai liukoisena reseptorina; se kontrolloi B-solujen kasvua ja erilaistumista ja estää eosinofiilien, monosyyttien ja basofiilien IgE-sitoutumisen.
Yhteenvetotaulukko
| Reseptorin nimi | Tärkein vasta -aineen ligandi | Affiniteetti ligandiin | Solujen jakautuminen | Vaikutus vasta -aineeseen sitoutumisen jälkeen |
| FcyRI ( CD64 ) | IgG1 ja IgG3 | Korkea (Kd ~ 10−9 M) |
Makrofagit Neutrofiilit Eosinofiilit Dendriittisolut |
Fagosytoosi Solujen aktivointi Hengityspurskeen aktivointi Mikrobien tappamisen induktio |
| FcγRIIA ( CD32 ) | IgG | Alhainen (Kd> 10−7 M) | Makrofagit Neutrofiilit Eosinofiilit Verihiutaleet Langerhansin solut |
Fagosytoosin degranulaatio (eosinofiilit) |
| FcγRIIB1 (CD32) | IgG | Alhainen (Kd> 10−7 M) |
B -solut Maston solut |
Ei fagosytoosia Solun toiminnan estäminen |
| FcγRIIB2 (CD32) | IgG | Alhainen (Kd> 10−7 M) | Makrofagit Neutrofiilit Eosinofiilit |
Fagosytoosi Solun toiminnan estäminen |
| FcγRIIIA ( CD16a ) | IgG | Alhainen (Kd> 10−6 M) |
NK -solut Makrofagit (tietyt kudokset) |
Induktio vasta-aineesta riippuvainen soluvälitteinen sytotoksisuus (ADCC) induktio sytokiini- makrofagien |
| FcγRIIIB ( CD16b ) | IgG | Alhainen (Kd> 10−6 M) | Eosinofiilit Makrofagit Neutrofiilit Maston solut Follikulaariset dendriittisolut |
Mikrobien tappamisen induktio |
| FcεRI | IgE | Korkea (Kd ~ 10 −10 M) | Maston solut Eosinofiilit Basophils Langerhans -solut Monosyytit |
Degranulaation fagosytoosi |
| FcεRII ( CD23 ) | IgE | Alhainen (Kd> 10−7 M) | B -solut Eosinofiilit Langerhansin solut |
Mahdollinen adheesiomolekyylin IgE-kuljetus ihmisen suoliston epiteelin läpi Positiivinen takaisinkytkentämekanismi parantaa allergista herkistymistä (B-solut) |
| FcαRI ( CD89 ) | IgA | Alhainen (Kd> 10−6 M) | Monosyytit Makrofagit Neutrofiilit Eosinofiilit |
Fagosytoosi Mikrobien tappamisen induktio |
| Fcα/μR | IgA ja IgM | Korkea IgM: lle, keskitaso IgA: lle | B -solut Mesangiaaliset solut Makrofagit |
Endosytoosi Mikrobien tappamisen induktio |
| FcRn | IgG | Monosyytit Makrofagit Dendriittisolut Epiteelisolut Endoteelisolut Hepatosyytit |
Siirrot IgG äidiltä sikiön istukan kautta Siirrot IgG äidiltä lapselle maito- Suojaa IgG hajoamiselta |
Toiminnot
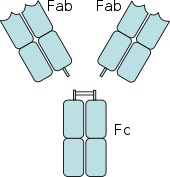
Fc-reseptorit ovat löytyy useita solujen immuunijärjestelmän, mukaan lukien fagosyyttejä , kuten makrofagit ja monosyytit , granulosyytit , kuten neutrofiilit ja eosinofiilit , ja lymfosyytit ja luontaisen immuunijärjestelmän ( luonnollisten tappajasolujen ) tai hankittu immuniteetti (esim, B-solut ). Niiden avulla nämä solut sitoutua vasta-aineita, on kiinnitetty pintaan mikrobeja tai mikrobin infektoituneita soluja, auttaa nämä solut tunnistaa ja poistaa mikrobien taudinaiheuttajia . Fc -reseptorit sitovat vasta -aineita niiden Fc -alueella (tai hännässä), vuorovaikutus, joka aktivoi solun, jolla on Fc -reseptori. Fagosyyttien aktivointi on yleisin Fc -reseptoreihin liittyvä toiminto. Esimerkiksi, makrofagit alkaa niellä ja tappaa IgG- päällystettyjä patogeenin mukaan fagosytoosin jälkeen, kytkennän niiden Fcy-reseptoreihin. Toista Fc-reseptoreihin liittyvää prosessia kutsutaan vasta-aineesta riippuvaiseksi soluvälitteiseksi sytotoksisuudeksi (ADCC). ADCC: n aikana FcγRIII-reseptorit luonnollisten tappajasolujen (NK) pinnalla stimuloivat NK-soluja vapauttamaan sytotoksisia molekyylejä rakeistaan tappamaan vasta-aineen peittämät kohdesolut. FcεRI: llä on erilainen toiminto. FceRI on Fc-reseptori granulosyyttien , että on mukana allergisten reaktioiden ja suojaa parasiitti- infektioita . Kun sopiva allerginen antigeeni tai loinen on läsnä, vähintään kahden IgE- molekyylin ja niiden Fc-reseptorien silloitus granulosyyttien pinnalla saa solun vapauttamaan nopeasti esimuodostetut välittäjät rakeistaan.
Signaalimekanismit - Fc -gammareseptorit
Aktivointi
Fc-gammareseptorit kuuluvat ei-katalyyttisten tyrosiinifosforyloituneiden reseptorien ryhmään, joilla on samanlainen signalointireitti, johon liittyy tyrosiinitähteiden fosforylaatio. Reseptorit tuottavat signaaleja soluissaan tärkeän aktivointimotiivin kautta, joka tunnetaan immunoretseptorityrosiinipohjaisena aktivointimotiivina (ITAM). ITAM on erityinen aminohapposekvenssi (YXXL), joka esiintyy kahdesti peräkkäin reseptorin solunsisäisessä hännässä. Kun fosfaatti ryhmät lisätään tyrosiini (Y) jäännös ITAM jonka kalvo-ankkuroidun entsyymien ja Src-kinaasien perhe , joka on signalointikaskadiin syntyy solun sisällä. Tämä fosforylaatioreaktio seuraa tyypillisesti Fc -reseptorin vuorovaikutusta sen ligandin kanssa . ITAM on läsnä FcyRIIA: n solunsisäisessä hännässä, ja sen fosforylaatio indusoi fagosytoosin makrofageissa. FcγRI: llä ja FcγRIIIA: lla ei ole ITAM: ää, mutta ne voivat lähettää aktivoivan signaalin fagosyytteilleen vuorovaikutuksessa toisen proteiinin kanssa. Tätä adapteriproteiinia kutsutaan Fcy -alayksiköksi ja se sisältää FcyRIA: n tavoin kaksi YAMXL -sekvenssiä, jotka ovat tyypillisiä ITAM: lle.
Esto
Vain yhden YXXL-motiivin läsnäolo ei riitä aktivoimaan soluja, ja se edustaa motiivia (I/VXXYXXL), joka tunnetaan immunoretseptorityrosiinipohjaisena estävänä motiivina (ITIM). FcyRIIB1: llä ja FcyRIIB2: lla on ITIM -sekvenssi ja ne ovat inhiboivia Fc -reseptoreita; ne eivät aiheuta fagosytoosia. Näiden reseptorien estäviä vaikutuksia kontrolloivat entsyymit, jotka poistavat fosfaattiryhmät tyrosiinitähteistä; fosfataasit SHP-1 ja SATAMANOSTURIT 1 inhiboivat signalointi Fcy-reseptoreihin. Ligandin sitoutuminen FcyRIIB: hen johtaa ITAM -motiivin tyrosiinin fosforylaatioon. Tämä muutos luo SH2 -tunnistusdomeenin, fosfataasin, sitoutumiskohdan. ITAM-aktivointisignaloinnin kumoaminen johtuu Src-perheen proteiinityrosiinikinaasien estämisestä ja PIP3-kalvon hydrolysoinnista, joka keskeyttää aktivoivien reseptorien, kuten FcγR: ien, TCR: n, BCR: n ja sytokiinireseptorien (esim. C-Kit) aktivoinnin. ).
FcyRIIB: n negatiivinen signalointi on pääasiassa tärkeää aktivoitujen B -solujen säätelyyn. Positiivinen B -solusignalointi aloitetaan sitomalla vieras antigeeni pinnan immunoglobuliiniin. Sama antigeenispesifinen vasta-aine erittyy ja se voi tukahduttaa palautetta tai edistää negatiivista signalointia. Tämän negatiivisen signaloinnin tarjoaa FcyRIIB: Kokeet, joissa käytetään B-solun deleetiomutantteja ja hallitsevia negatiivisia entsyymejä, ovat vakiinnuttaneet vahvan roolin SH2-domeenia sisältävälle inositoli-5-fosfataasille (SHIP) negatiivisessa signaloinnissa. Negatiivinen signalointi SHIP: n kautta näyttää estävän Ras -reittiä SH2 -domeenikilpailun kautta Grb2: n ja Shc: n kanssa ja voi sisältää solunsisäisten lipidivälittäjien kulutuksen, jotka toimivat allosteerisina entsyymin aktivaattorina tai jotka edistävät solunulkoisen Ca2+: n pääsyä.
Solujen aktivointi
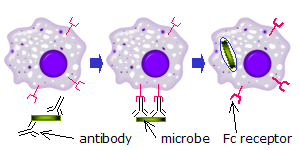
Fagosyyteillä
Kun tietylle antigeenille tai pintakomponentille spesifiset IgG -molekyylit sitoutuvat patogeeniin Fab -alueensa (fragmenttiantigeeniä sitova alue) avulla, niiden Fc -alueet osoittavat ulospäin, fagosyyttien suorassa ulottuvilla . Fagosyytit sitovat nämä Fc -alueet Fc -reseptoreillaan. Reseptorin ja vasta-aineen välille muodostuu monia alhaisen affiniteetin vuorovaikutuksia, jotka toimivat yhdessä sitomaan tiukasti vasta-aineella päällystetty mikrobi. Alhainen yksilöllinen affiniteetti estää Fc -reseptoreita sitoutumasta vasta -aineisiin antigeenin puuttuessa ja vähentää siten mahdollisuutta immuunisolujen aktivoitumiseen ilman infektiota. Tämä estää myös fagosyyttien agglutinaation (hyytymisen) vasta -aineella , kun antigeeniä ei ole. Sen jälkeen, kun patogeeni on sidottu, vuorovaikutukset Fc-alueen vasta-aineen ja Fc-reseptoreihin fagosyytti tuloksia aloittamisen fagosytoosin . Fagosyytti imee patogeenin aktiivisella prosessilla, johon liittyy Fc -alueen/Fc -reseptorikompleksin sitoutuminen ja vapautuminen, kunnes fagosyytin solukalvo sulkee patogeenin kokonaan.
NK -soluissa
NK-solujen Fc-reseptori tunnistaa IgG: n, joka on sitoutunut patogeenillä infektoidun kohdesolun pintaan ja jota kutsutaan CD16: ksi tai FcyRIII: ksi. FcγRIII: n aktivointi IgG: llä aiheuttaa sytokiinien , kuten IFN-y: n , vapautumista muille immuunisoluille ja sytotoksisia välittäjiä, kuten perforiinia ja grantsyymiä, jotka vapautuvat kohdesoluun ja edistävät solukuolemaa laukaisemalla apoptoosin . Tämä prosessi tunnetaan vasta-aineesta riippuvaisena soluvälitteisenä sytotoksisuutena (ADCC). FcγRIII NK-soluissa voi myös liittyä monomeeriseen IgG: hen (eli IgG: hen, joka ei ole sitoutunut antigeeniin). Kun näin tapahtuu, Fc -reseptori estää NK -solun aktiivisuuden.
Syöttösoluissa

IgE- vasta-aineet sitoutuvat antigeenien ja allergeenit . Nämä allergeeniin sitoutuneet IgE-molekyylit ovat vuorovaikutuksessa syöttösolujen pinnalla olevien Fcε-reseptorien kanssa . Syöttösolujen aktivointi FcRI: n sitoutumisen jälkeen johtaa prosessiin, jota kutsutaan degranulaatioksi , jolloin syöttösolu vapauttaa esimuodostettuja molekyylejä sytoplasmisista rakeistaan; nämä ovat yhdisteiden seos, mukaan lukien histamiini , proteoglykaanit ja seriiniproteaasit . Aktivoidut syöttösolut myös syntetisoivat ja erittävät lipidistä peräisin olevia välittäjiä (kuten prostaglandiineja , leukotrieenejä ja verihiutaleita aktivoivaa tekijää ) ja sytokiineja (kuten interleukiini 1 , interleukiini 3 , interleukiini 4 , interleukiini 5 , interleukiini 6 , interleukiini 13 , tuumorinekroositekijä) -alfa , GM-CSF ja useat kemokiinit Nämä välittäjät edistävät tulehdusta houkuttelemalla muita leukosyyttejä .
Eosinofiileillä
Suuret loiset, kuten helmintti (mato) Schistosoma mansoni, ovat liian suuria fagosyyttien nielemiseksi. Niillä on myös ulkoinen rakenne, jota kutsutaan integumentiksi, joka kestää makrofagien ja syöttösolujen vapauttamien aineiden hyökkäyksiä. Nämä loiset voivat kuitenkin päällystyä IgE: llä ja tunnistaa FcεRI eosinofiilien pinnalla . Aktivoidut eosinofiilit vapauttavat esimuotoiltuja välittäjiä, kuten tärkeimmän emäksisen proteiinin , ja entsyymejä , kuten peroksidaasia , joita vastaan helmintit eivät ole resistenttejä. FcεRI -reseptorin vuorovaikutus helminttiin sitoutuneen IgE: n Fc -osan kanssa saa eosinofiilin vapauttamaan nämä molekyylit samankaltaisessa mekanismissa kuin NK -solu ADCC: n aikana.
T -lymfosyyteissä
CD4+ T -solut ( kypsät T h -solut ) auttavat vasta -aineita tuottavia B -soluja. Taudin patologiassa havaitaan useita aktivoitujen efektori -CD4+ T -solujen osajoukkoja. Aiemmat Sandersin ja Lynchin vuonna 1993 yhteenvetämät tutkimukset ehdottivat kriittisiä rooleja FcR: ille CD4+ T -soluvälitteisissä immuunivasteissa ja ehdottivat yhteisen signalointikompleksin muodostamista FcR: ien ja TCR: n välillä solun pinnalla. Chauhan ja työtoverit ilmoittivat leimattujen IC: iden kolokalisoitumisen CD3 -kompleksin kanssa aktivoidulla CD4+ T -solupinnalla, mikä viittaa siten FcR: ien rinnakkaiseloon yhdessä TCR -kompleksin kanssa. Molempien näiden reseptorien havaitaan muodostavan apikaalisen rakenteen aktivoitujen CD4+ T -solujen kalvolle, mikä viittaa näiden reseptorien sivuttaisliikkeeseen. FcR: ien samanaikainen migraatio TCR- ja BCR-kompleksin kanssa havaitaan solujen pinnalla ja T: B-solusytokonjugaatit osoittavat tämän rinnakkaiselon kosketuspisteessä. Aiempi katsaus viittasi siihen, että FcR: ien ilmentyminen CD4+ T -soluissa on avoin kysymys. Tämä vahvisti nykyisen paradigman, jonka mukaan T -solut eivät ekspressoi FcR: iä, eikä näitä havaintoja koskaan kyseenalaistettu ja kokeellisesti testattu. Chauhan ja työtoverit osoittivat sitoutuneensa immuunikomplekseihin (IC), FcR -ligandiin aktivoituihin CD4+ T -soluihin. CD16a -ilmentyminen indusoidaan aktivoiduissa ihmisen naiiveissa CD4+ T -soluissa, jotka ilmentävät CD25-, CD69- ja CD98 -soluja ja ligaatio IC: hen johtaa efektorimuistisolujen syntymiseen. CD16a -signalointia välittää Sykin (pSyk) fosforylaatio.
Tutkimus ehdottaa nyt CD32a: n indusoitua ekspressiota, kun ihmisen CD4+ T -solut aktivoidaan, samanlainen kuin CD16a. CD32a: n ilmentymistä CD4+ T-soluissa ehdotti myös kolme riippumatonta tutkimusta HIV-1-tutkijoilta. CD16a: n ja CD32a: n ilmentyminen aktivoitujen CD4+ T -solujen osajoukossa on nyt vahvistettu. FcR: t solun pinnalla, kun ne sitoutuvat nukleiinihapoista koostuviin IC: iin, laukaisevat sytokiinituotannon ja säätelevät nukleiinihappoantumisreittejä. FcR: t ovat läsnä sekä solun pinnalla että sytosolissa. CD16a-signalointi ylöspäin säätää nukleiinihappoa havaitsevien maksullisten reseptorien ilmentymistä ja siirtää ne solun pinnalle. CD16a on uusi kostimulatorinen signaali ihmisen CD4+ T -soluille, jotka korvaavat onnistuneesti CD28 -tarpeen autoimmuunisuojan aikana. Autoimmuunitaustalla CD4+ T -solut ohittavat CD28 -kosignalointivaatimuksen aktivoituakseen täysin. Lisäksi CD28 -kosignaloinnin esto ei estä TFH -solujen kehittymistä, mikä on keskeinen osajoukko autoreaktiivisten plasman B -solujen tuottamiseen. Immuunihomeostaasiin tarvitaan tasapaino kostimuloivien ja estävien signaalien välillä. Liiallinen kustannustimulaatio ja/tai riittämätön yhteisestäminen johtaa toleranssin hajoamiseen ja autoimmuuniin. CD16a -välitteinen kostimulaatio antaa positiivisen signaalin aktivoiduissa CD4+ T -soluissa eikä niissä lepotilassa olevissa soluissa, joista puuttuu FcyR -ilmentyminen.
Katso myös
Viitteet
Lue lisää
- Janeway CA, Travers P, Waldport M, Shlomchik MJ (2001). "Luku 9. Humoraalinen immuunivaste" . Immunobiologia: Immuunijärjestelmä terveydessä ja sairauksissa (5. painos). New York: Garland. ISBN 978-0-8153-3642-6.
- Abbas AK, Lichtman AH, Pillai S (2012). "Luku 12: Humoraalisen immuniteetin vaikutusmekanismit". Solun ja molekyylin immunologia (7. painos). Philadelphia: Elsevier/Saunders. ISBN 978-1-4377-1528-6.
- Gerber JS, Mosser DM (helmikuu 2001). "Stimuloivat ja estävät signaalit, jotka ovat peräisin makrofagien Fcgamma -reseptoreista". Mikrobit ja infektiot . 3 (2): 131–9. doi : 10.1016/s1286-4579 (00) 01360-5 . PMID 11251299 .
- Maverakis E, Kim K, Shimoda M, Gershwin ME, Patel F, Wilken R, Raychaudhuri S, Ruhaak LR, Lebrilla CB (helmikuu 2015). "Glykaanit immuunijärjestelmässä ja autoimmuniteetin muutettu glykaaniteoria: kriittinen arvostelu" . Autoimmuniteetin lehti . 57 : 1–13. doi : 10.1016/j.jaut.2014.12.002 . PMC 4340844 . PMID 25578468 .
Ulkoiset linkit
- Fc+-reseptori Yhdysvaltain kansallisen lääketieteen kirjastossa Medical Subject Headings (MeSH)
