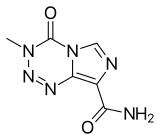
Temotsolomidi - Temozolomide
 | |
 | |
| Kliiniset tiedot | |
|---|---|
| Kauppanimet | Temodar, Temodal, Temcad, muut |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a601250 |
| Lisenssitiedot | |
| Raskaus luokka |
|
| Reitit hallinnon |
Suun kautta , suonensisäisesti |
| ATC -koodi | |
| Oikeudellinen asema | |
| Oikeudellinen asema | |
| Farmakokineettiset tiedot | |
| Biologinen hyötyosuus | melkein 100% |
| Sitoutuminen proteiineihin | 15% (10–20%) |
| Aineenvaihdunta | hydrolyysi |
| Metaboliitit | 3-metyyli- (triatsen-1-yyli) imidatsoli-4-karboksamidi (MTIC, aktiivinen laji ); temotsolomidihappo |
| Eliminaation puoliintumisaika | 1,8 tuntia |
| Erittyminen | pääasiassa munuaiset |
| Tunnisteet | |
| |
| CAS -numero | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox -kojelauta ( EPA ) | |
| ECHA InfoCard |
100,158,652 |
| Kemialliset ja fysikaaliset tiedot | |
| Kaava | C 6 H 6 N 6 O 2 |
| Moolimassa | 194,154 g · mol −1 |
| 3D -malli ( JSmol ) | |
| Sulamispiste | 212 ° C (414 ° F) (hajoaa) |
| |
| |
|
| |
Temozolomide ( TMZ ), jota myydään muun muassa tuotenimellä Temodar , on lääke, jota käytetään joidenkin aivokasvainten, kuten multiformisen glioblastooman tai anaplastisen astrosytooman, hoitoon. Se otetaan suun kautta tai infuusiona laskimoon.
Yleisimpiä haittavaikutuksia temotsolomidilla ovat pahoinvointi (huonovointisuus), oksentelu , ummetus , ruokahaluttomuus , hiustenlähtö (hiustenlähtö), päänsärky , väsymys (väsymys), kouristukset (kohtaukset), ihottuma , neutropenia tai lymfopenia (valkoisten verta (solujen määrä) ja trombosytopenia (alhainen verihiutaleiden määrä). Infuusionestettä saavilla ihmisillä voi myös olla pistoskohdan reaktioita, kuten kipua, ärsytystä, kutinaa, lämpöä, turvotusta ja punoitusta sekä mustelmia.
Temotsolomidi on alkyloiva aine, jota käytetään joidenkin aivosyöpien hoitoon; toisen linjan hoitona astrosytoomalle ja ensimmäisen linjan hoidolle glioblastooma multiformille . Olaparibi yhdessä temotsolomidin kanssa osoitti merkittävää kliinistä aktiivisuutta uusiutuneen pienisoluisen keuhkosyövän hoidossa .
Lääketieteellinen käyttö
Yhdysvalloissa temotsolomidi on tarkoitettu aikuisten hoitoon, joilla on äskettäin diagnosoitu glioblastooma multiforme samanaikaisesti sädehoidon kanssa ja myöhemmin monoterapiahoitona; tai aikuiset, joilla on tulenkestävä anaplastinen astrosytooma ja jotka ovat kokeneet taudin etenemisen lääkkeellä, joka sisältää nitrosoureaa ja prokarbatsiinia .
Euroopan unionissa temotsolomidi on tarkoitettu aikuisille, joilla on äskettäin diagnosoitu glioblastooma multiforme samanaikaisesti sädehoidon ja myöhemmin monoterapiahoitona; tai yli 3 -vuotiaat lapset, nuoret ja aikuiset, joilla on pahanlaatuinen gliooma, kuten multiforminen glioblastooma tai anaplastinen astrosytooma, ja jotka osoittavat uusiutumista tai etenemistä tavanomaisen hoidon jälkeen.
Vasta -aiheet
Temotsolomidi on vasta -aiheinen ihmisille, jotka ovat yliherkkiä sille tai vastaavalle lääkkeelle dakarbatsiinille . Temotsolomidin käyttöä ei suositella henkilöille, joilla on vaikea myelosuppressio .
Haittavaikutukset
Yleisin sivuvaikutus on luuydinsuppressio . Yleisimmät temotsolomidiin liittyvät ei-hematologiset haittavaikutukset ovat pahoinvointi ja oksentelu, jotka ovat joko itsestään rajoittavia tai helposti hallittavissa tavanomaisella antiemeettisellä hoidolla. Nämä jälkimmäiset vaikutukset ovat yleensä lieviä tai kohtalaisia (asteet 1-2). Vaikeaa pahoinvointia ja oksentelua esiintyy noin 4%. Potilaat, joilla on aiemmin esiintynyt tai on aiemmin ollut voimakasta oksentelua, saattavat tarvita antiemeettistä hoitoa ennen temotsolomidihoidon aloittamista. Temotsolomidi tulee antaa paastotilassa vähintään tunti ennen ateriaa. Antiemeettinen hoito voidaan antaa ennen temotsolomidin antamista tai sen jälkeen.
Temotsolomidi on genotoksinen , teratogeeninen ja sikiötoksinen, eikä sitä tule käyttää raskauden aikana. Imettävien naisten tulee lopettaa imetys lääkkeen käytön aikana, koska ne voivat erittyä äidinmaitoon. Yksi tutkimus osoitti, että naiset, jotka ovat käyttäneet temotsolomidia ilman samanaikaisia hedelmällisyyden säilyttämistoimenpiteitä, saavuttavat raskauden vähäisemmässä määrin myöhemmin elämässä, mutta tutkimus oli liian pieni osoittamaan tilastollista merkitystä hypoteesissa, jonka mukaan temotsolomidi aiheuttaisi naisten hedelmättömyyden riskin . Temotsolomidilla voi olla miespotilailla genotoksisia vaikutuksia. Miehiä kehotetaan olemaan isättymättä lapselle hoidon aikana tai kuuteen kuukauteen hoidon jälkeen ja etsimään neuvoja siittiöiden kylmäkonservoinnista ennen hoitoa, koska temotsolomidihoidon vuoksi on mahdollista saada peruuttamaton hedelmättömyys.
Hyvin harvoin temotsolomidi voi aiheuttaa akuutin hengitysvajeen tai maksavaurion.
Vuorovaikutukset
Koska temotsolomidi ei metaboloidu maksassa ja sillä on alhainen affiniteetti plasman proteiineihin , sen odotetaan olevan vähäisiä yhteisvaikutuksia. Potilastietojen analyysi ei osoittanut vuorovaikutusta useiden muiden lääkkeiden kanssa; Poikkeuksena on valproiinihappo , joka hidastaa hieman temotsolomidin poistumista kehosta. Lääkkeen yhdistäminen muiden myelosuppressanttien kanssa voi lisätä myelosuppression riskiä.
Farmakologia
Toimintamekanismi
Temotsolomidin terapeuttinen hyöty riippuu sen kyvystä alkyloida / metyloida DNA: ta, joka esiintyy useimmiten guaniinitähteiden N-7- tai O-6-asemissa . Tämä metylaatio vahingoittaa DNA: ta ja laukaisee kasvainsolujen kuoleman. Jotkut kasvainsolut kykenevät kuitenkin korjaamaan tämäntyyppiset DNA -vauriot ja siten heikentämään temotsolomidin terapeuttista tehokkuutta ilmentämällä O -6 -alkyyliguaniini -DNA -alkyylitransferaasia (AGT), jota ihmisillä on O -6 -metyyliguaniini -DNA -metyylitransferaasin koodaama ( MGMT ) -geeni. Joissakin kasvaimissa MGMT -geenin epigeneettinen hiljentäminen estää tämän entsyymin synteesin, minkä seurauksena tällaiset kasvaimet ovat herkempiä temotsolomidin aiheuttamalle tappamiselle. Sitä vastoin AGT -proteiinin läsnäolo aivokasvaimissa ennustaa huonon vasteen temotsolomidille, ja nämä potilaat hyötyvät vain vähän temotsolomidin solunsalpaajahoidosta.
Farmakokinetiikka
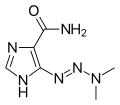
Temotsolomidi imeytyy nopeasti ja lähes kokonaan suolistosta ja läpäisee helposti veri -aivoesteen ; aivo -selkäydinnesteessä oleva pitoisuus on 30% veriplasman pitoisuudesta . Syöminen ruoan kanssa pienentää maksimipitoisuuksia plasmassa 33% ja käyrän alla olevaa aluetta 9%. Vain 15% (10–20%) aineesta sitoutuu veriplasman proteiineihin. Temotsolomidi on aihiolääke ; se hydrolysoituu spontaanisti fysiologisessa pH: ssa 3-metyyli- (triatsen-1-yyli) imidatsoli-4-karboksamidiksi (MTIC). MTIC jakautuu monometyylihydratsiiniksi , luultavasti aktiiviseksi metylointiaineeksi, ja 5-aminoimidatsoli-4-karboksamidiksi (AIC). Muita metaboliitteja ovat temotsolomidihappo ja tunnistamattomat hydrofiiliset aineet.
Plasman puoliintumisaika on 1,8 tuntia. Aine ja sen metaboliitit erittyvät pääasiassa virtsan kautta.
MTIC, aktiivinen metaboliitti
AIC (osa luonnossa esiintyvää AICA -ribonukleotidia )
Liittyvä lääke dakarbatsiini vertailua varten
Kemiallisia ominaisuuksia
Temotsolomidi on imidatsotetratsiinijohdannainen. Se liukenee hieman veteen ja vesipitoisiin happoihin ja hajoaa 212 ° C: ssa (414 ° F). Äskettäin havaittiin, että temotsolomidi on räjähde, joka on alustavasti luokiteltu YK -luokkaan 1 .
Historia
Agentti on kehittänyt Malcolm Stevens ja hänen ryhmänsä Aston University vuonna Birminghamissa, Englannissa .
Se hyväksyttiin lääketieteelliseen käyttöön Euroopan unionissa tammikuussa 1999 ja Yhdysvalloissa elokuussa 1999. Laskimonsisäinen formulaatio hyväksyttiin Yhdysvalloissa helmikuussa 2009.
Tutkimus
Laboratoriotutkimukset ja kliiniset tutkimukset ovat alkaneet tutkia mahdollisuutta lisätä temotsolomidin syövänvastaista tehoa yhdistämällä se muihin farmakologisiin aineisiin. Esimerkiksi kliiniset tutkimukset ovat osoittaneet, että klorokiinin lisäämisestä voi olla hyötyä glioomapotilaiden hoidossa. Laboratoriotutkimukset osoittivat, että temotsolomidi tappoi aivokasvainsolut tehokkaammin, kun lisättiin vihreää teetä sisältävää epigallokatekiinigallaattia ( EGCG ) ; tämän vaikutuksen tehokkuutta ei kuitenkaan ole vielä vahvistettu aivokasvainpotilailla . Vuonna 2010 raportoidut prekliiniset tutkimukset, jotka koskivat uuden hapen diffuusion tehostavan trans-natriumkrosetinaatin (TSC) käytön tutkimuksia yhdessä temotsolomidin ja sädehoidon kanssa, ja kliininen tutkimus oli käynnissä elokuusta 2015 lähtien.
Vaikka edellä mainitut lähestymistavat ovat tutkineet, voisiko tematsolomidin ja muiden aineiden yhdistelmä parantaa hoitotulosta, on myös alettu tutkia, voiko temotsolomidimolekyylin muuttaminen itse lisätä sen aktiivisuutta. Yksi tällainen lähestymistapa fuusioi pysyvästi perillyylialkoholin , luonnollisen yhdisteen, jolla on osoitettu terapeuttista aktiivisuutta aivosyöpäpotilailla, temotsolomidimolekyyliin. Tuloksena oleva uusi yhdiste, nimeltään NEO212 tai TMZ-POH, paljasti syövän vastaisen aktiivisuuden, joka oli merkittävästi suurempi kuin kummankaan sen kahdesta emomolekyylistä, temotsolomidista ja perillyylialkoholista. Vaikka vuodesta 2016, NEO212 ei ole tutkittu ihmisillä, se on osoittanut ylivoimainen syövän terapeuttista aktiivisuutta eläinmalleissa gliooma , melanooma , ja aivometastaasi sekä triple-negatiivinen rintasyöpä .
Koska kasvainsolut, jotka ilmentävät ÄLYPELIT geeni ovat vastustuskykyisiä vaikutuksia temotsolomidin, tutkijat tutkineet onko sisällyttäminen O 6 -benzylguanine ( O 6 -BG), joka on AGT inhibiittori, voi voittaa tämän resistenssin ja parantaa lääkkeen terapeuttista tehokkuutta. Laboratoriossa tämä yhdistelmä osoitti todellakin lisääntyneen temotsolomidiaktiivisuuden kasvainsoluviljelmässä in vitro ja eläinmalleissa in vivo . Kuitenkin äskettäin päättynyt vaiheen II kliininen tutkimus aivokasvainpotilailla tuotti ristiriitaisia tuloksia; kun oli jonkin verran parantunut terapeuttinen vaikutus O 6 -BG ja temotsolomidi annettiin potilaille, joilla on temotsolomidi kestävä anaplastinen gliooman, ei näyttänyt olevan mitään merkittävää palauttaminen temotsolomidia herkkyys potilailla, joilla on temotsolomidi-resistenttejä glioblastoma multiforme .
Jotkut ponnistelut keskittyvät MGMT- geeniä ilmentävien hematopoieettisten kantasolujen suunnitteluun ennen niiden siirtämistä aivokasvainpotilaille. Tämä antaisi potilaille mahdollisuuden saada voimakkaampia temotsolomidiannoksia, koska potilaan hematopoieettiset solut olisivat vastustuskykyisiä lääkkeelle.
Suurilla temotsolomidiannoksilla korkealaatuisissa glioomissa on alhainen toksisuus, mutta tulokset ovat verrattavissa standardiannoksiin.
Nyt on kuvattu kaksi temotsolomidivaikutusten vastustuskyvyn mekanismia: 1) luontainen resistenssi, joka johtuu MGMT -puutteesta (MGMTd) ja 2) luontainen tai hankittu resistenssi MMR -puutteen (MMRd) kautta. MGMT -entsyymi on TMZ: n luoma yhteensopimattomien emästen ensimmäinen korjauslinja. Solut ovat normaalisti MGMT -taitavia (MGMTp), koska niissä on metyloimaton MGMT -promoottori, joka mahdollistaa geenin ilmentymisen normaalisti. Tässä tilassa TMZ: n aiheuttama DNA -vaurio voidaan korjata tehokkaasti kasvainsoluissa (ja normaaleissa soluissa) aktiivisella MGMT -entsyymillä. Solut voivat kasvaa ja kulkea solusyklin läpi normaalisti ilman pidätystä tai kuolemaa. Joissakin kasvaimissa solut ovat kuitenkin MGMT -puutteisia (MGMTd). Tämä johtuu useimmiten MGMT -geenipromoottorin epänormaalista metylaatiosta ja geeniekspression tukahduttamisesta. MGMTd on myös kuvattu tapahtuvan promoottorin uudelleenjärjestelyllä. MGMTd -soluissa TMZ: n aiheuttamat DNA -vauriot aktivoivat seuraavan korjausvaiheen soluissa, joissa on taitava Mismatch Repair -entsyymikompleksi (MMRp). MMRp: ssä MMR -proteiinikompleksi tunnistaa vauriot ja saa solut pysähtymään ja kuolemaan, mikä estää kasvaimen kasvua. Jos soluissa on kuitenkin yhdistetty MGMTd- ja MMR -puutos (MGMTd + MMRd), solut säilyttävät indusoidut mutaatiot ja jatkavat sykliä ja ovat resistenttejä TMZ: n vaikutuksille.
Glioomissa ja muissa syövissä MMRd: n on nyt raportoitu esiintyvän ensisijaisena MMRd: nä (luontainen tai ituradan Lynch bMMRd) tai toissijaisena MMRd: nä (hankittu - ei läsnä alkuperäisessä hoitamattomassa kasvaimessa). Jälkimmäinen tapahtuu sen jälkeen, kun kasvaimia on hoidettu tehokkaasti ja niiden sytoreduktio on suoritettu TMZ: llä ja sen jälkeen on valittu tai indusoitu MSH6-, MSH2-, MLH1- tai PMS2 -mutanttiproteiineja ja -soluja, jotka ovat MMRd- ja TMZ -resistenttejä. Jälkimmäistä kuvataan hankituksi resistenssireitiksi, jolla on hotspot -mutaatioita glioomapotilailla (MSH6 p. 1219I). Todennäköisesti on myös muita vastusreittejä.
Viitteet
Lue lisää
- Kaloshi G, Benouaich-Amiel A, Diakite F, et ai. (Toukokuu 2007). "Temotsolomidi huonolaatuisille glioomille: 1p/19q menetyksen ennustava vaikutus vasteeseen ja tulokseen" . Neurologia . 68 (21): 1831–6. doi : 10.1212/01.wnl.0000262034.26310.a2 . PMID 17515545 . Lay yhteenveto .
Ulkoiset linkit
- "Temotsolomidi" . Huumeiden tietoportaali . Yhdysvaltain kansallinen lääketieteen kirjasto.
- "Temotsolomidi (Temodal)" . Cancer Research UK .