Tromboottinen trombosytopeeninen purppura - Thrombotic thrombocytopenic purpura
| Tromboottinen trombosytopeeninen purppura | |
|---|---|
| Muut nimet | Moschcowitzin oireyhtymä, idiopaattinen tromboottinen trombosytopeeninen purppura |
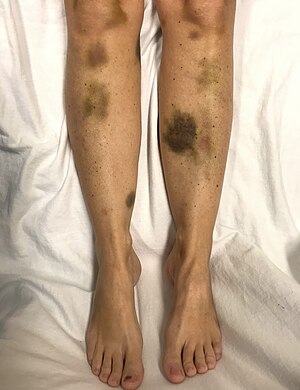 | |
| Spontaanit mustelmat naisella, jolla on kriittisesti alhaiset verihiutaleet | |
| Erikoisuus | Hematologia |
| Oireet | Suuret mustelmat , kuume , heikkous, hengenahdistus , sekavuus, päänsärky |
| Tavallinen alku | Aikuisuus |
| Syyt | Tuntematon, bakteeri -infektiot , tietyt lääkkeet, autoimmuunisairaudet , raskaus |
| Diagnostinen menetelmä | Perustuu oireisiin ja verikokeisiin |
| Differentiaalinen diagnoosi | Hemolyyttinen-ureeminen oireyhtymä (HUS), epätyypillinen hemolyyttinen ureeminen oireyhtymä (aHUS) |
| Hoito | Plasmanvaihto , immunosuppressantit |
| Ennuste | <20% kuoleman riski |
| Taajuus | 1 100 000 ihmisestä |
Tromboottinen trombosytopeeninen purppura ( TTP ) on verisairaus, joka johtaa verihyytymien muodostumiseen pienissä verisuonissa koko kehossa. Tämä johtaa alhaiseen verihiutaleiden määrään , alhaisiin punasoluihin niiden hajoamisen vuoksi ja usein munuaisten , sydämen ja aivojen toimintahäiriöihin. Oireita voivat olla suuret mustelmat , kuume , heikkous, hengenahdistus , sekavuus ja päänsärky . Toistuvia jaksoja voi esiintyä.
Noin puolessa tapauksista liipaisin tunnistetaan, kun taas muualla syy on tuntematon. Tunnettuja laukaisijoita ovat bakteeri -infektiot , tietyt lääkkeet, autoimmuunisairaudet , kuten lupus ja raskaus . Taustalla oleva mekanismi sisältää tyypillisesti vasta -aineita, jotka estävät ADAMTS13 -entsyymiä . Tämä johtaa alentuneeseen hajottaa suuret multimeerit ja von Willebrand -tekijän (vWF) pienempiin yksiköihin. Harvemmin TTP periytyy henkilön vanhemmilta , joka tunnetaan nimellä Upshaw -Schulmanin oireyhtymä , joten ADAMTS13 -toimintahäiriö on läsnä syntymästä lähtien. Diagnoosi perustuu tyypillisesti oireisiin ja verikokeisiin. Sitä voidaan tukea mittaamalla ADAMTSin13 aktiivisuutta tai vasta -aineita.
Kanssa plasma vaihto riski kuolla on laskenut enemmän kuin 90%: sta alle 20%. Myös immunosuppressantteja , kuten glukokortikoideja ja rituksimabia, voidaan käyttää. Verihiutaleiden siirtoja ei yleensä suositella.
Noin 1 100 000 ihmistä koskee. Aloitus on tyypillisesti aikuinen ja naiset kärsivät useammin. Noin 10% tapauksista alkaa lapsuudessa. Tilanne kuvattiin ensimmäisen kerran Eli Moschcowitzissa vuonna 1924. Taustalla oleva mekanismi määritettiin 1980- ja 1990 -luvuilla.
Merkit ja oireet
TTP: n merkit ja oireet voivat aluksi olla hienovaraisia ja epäspesifisiä. Monet ihmiset kokevat influenssan kaltaisen tai ripulitaudin ennen TTP: n kehittymistä. Neurologiset oireet ovat hyvin yleisiä ja vaihtelevat suuresti. Usein raportoituja oireita ovat väsymys , sekavuus ja päänsärky . Myös kohtauksia ja oireita, jotka ovat samanlaisia kuin aivohalvaus, voidaan myös nähdä. Muita oireita ovat, mutta eivät rajoitu niihin, keltaisuus tai ihon kalpeus, nopea syke tai hengenahdistus tai tarkan kokoiset violetit tai punertavat pisteet iholla, joita kutsutaan petechioiksi.
Kun TTP etenee, verihyytymiä muodostuu pieniin verisuoniin (mikrovaskulaatio) ja verihiutaleet (hyytymissolut) kuluvat. Tämän seurauksena voi esiintyä mustelmia ja harvoin verenvuotoa. Mustelmia esiintyy usein purppurana , kun taas yleisin verenvuotopaikka, jos sitä ilmenee, on nenästä tai ikenistä. Myös suurempia mustelmia ( ekkoosia ) voi kehittyä. TTP: n klassinen esitys, jota esiintyy alle 10 prosentilla ihmisistä, sisältää viisi lääketieteellistä merkkiä. Nämä ovat:
- Kuume
- Henkisen tilan muutokset
- Trombosytopenia
- Heikentynyt munuaisten toiminta
- Hemolyyttinen anemia ( mikroangiopaattinen hemolyyttinen anemia ).
Korkea verenpaine ( hypertensio ) voidaan todeta tutkimuksessa.
Syyt
TTP, kuten muutkin mikroangiopaattiset hemolyyttiset anemiat (MAHA), johtuu verihiutaleiden spontaanista aggregaatiosta ja hyytymisen aktivoitumisesta pienissä verisuonissa. Verihiutaleet kuluvat aggregaatioprosessissa ja sitovat vWF: ää. Nämä verihiutale-vWF-kompleksit muodostavat pieniä verihyytymiä, jotka kiertävät verisuonissa ja aiheuttavat punasolujen leikkautumista, mikä johtaa niiden repeytymiseen ja skistosyyttien muodostumiseen . Kaksi parhaiten ymmärrettyä TTP-syytä johtuvat autoimmuunista ja perinnöllisestä ADAMTS13-puutteesta (tunnetaan Upshaw-Schülmanin oireyhtymänä). Suurin osa jäljellä olevista tapauksista on toissijaisia jonkin muun tekijän vuoksi.
Autoimmuuni
Tuntematon syy TTP tunnettiin pitkään idiopaattisena TTP: nä, mutta vuonna 1998 suurin osa tapauksista osoittautui johtuvan ADAMTS13 -entsyymin vasta -aineiden estämisestä . Vähentyneen ADAMTS13: n suhde TTP: n patogeneesiin tunnetaan Furlan-Tsai-hypoteesina kahden riippumattoman tutkijaryhmän jälkeen, jotka julkaisivat tutkimuksensa samassa New England Journal of Medicine -lehdessä . Nämä tapaukset luokitellaan nyt autoimmuunisairaudeksi ja tunnetaan autoimmuunisairautena TTP: nä (ei pidä sekoittaa immuuni/idiopaattiseen trombosytopeeniseen purppuraan ).
ADAMTS13 on metalloproteinaasi, joka vastaa von Willebrand -tekijän (vWF) hajoamisesta , proteiinista, joka yhdistää verihiutaleet, verihyytymät ja verisuonen seinämän veren hyytymisprosessissa. Erittäin suuret vWF -multimeerit ovat alttiimpia hyytymiseen. Siksi ilman vWF: n asianmukaista katkaisua ADAMTS13: lla hyytyminen tapahtuu nopeammin, erityisesti mikroverisuonistossa, verisuonijärjestelmän osassa, jossa vWF on aktiivisin suuren leikkausjännityksen vuoksi . Idiopaattisessa TTP: ssä vakavasti vähentynyt (<5%normaalista) ADAMTS13 -aktiivisuus voidaan havaita useimmilla (80%) ihmisillä, ja inhibiittoreita löytyy usein tästä alaryhmästä (44–56%).
Geneettinen
Tämä tila voi olla myös synnynnäinen. Tällaiset tapaukset voivat johtua mutaatioista ADAMTS13 -geenissä. Tätä perinnöllistä TTP -muotoa kutsutaan Upshaw -Schulmanin oireyhtymäksi . Ihmisillä, joilla on tämä perinnöllinen ADAMTS13 -puutos, on yllättävän lievä fenotyyppi, mutta he kehittävät TTP: tä kliinisissä tilanteissa, joissa von Willebrand -tekijä on lisääntynyt, esim. Infektio. Ilmoitusten mukaan alle 1% kaikista TTP -tapauksista johtuu Upshaw -Schulmanin oireyhtymästä. Ihmisillä, joilla on tämä oireyhtymä, on yleensä 5-10% normaalista ADAMTS-13-aktiivisuudesta.
Toissijainen
Toissijainen TTP diagnosoidaan, kun henkilön historiassa mainitaan yksi TTP: hen liittyvistä tunnetuista ominaisuuksista. Se muodostaa noin 40% kaikista TTP -tapauksista. Ennaltaehkäiseviä tekijöitä ovat:
- Syöpä
- Luuydinsiirto
- Raskaus
-
Lääkkeen käyttö:
- Antiviraaliset lääkkeet ( asykloviiri )
- Tietyt kemoterapialääkkeet , kuten gemsitabiini ja mitomysiini C
- Kiniini
- Oksimorfoni
- Ketiapiini
- Bevasitsumabi
- Sunitinibi
- Verihiutaleiden aggregaation estäjät ( tiklopidiini , klopidogreeli ja prasugreeli )
- Immunosuppressantit ( siklosporiini , mitomysiini , takrolimuusi /FK506, interferoni-a )
- Hormonimuutokset (estrogeenit, ehkäisyvalmisteet, hormonikorvaushoito)
- HIV-1- infektio
Sekundaarisen TTP: n mekanismi on huonosti ymmärretty, koska ADAMTS13 -aktiivisuus ei yleensä ole niin masentunut kuin idiopaattisessa TTP: ssä, eikä estäjiä voida havaita. Todennäköinen etiologia voi sisältää ainakin joissakin tapauksissa endoteelivaurioita, vaikka verisuonten tukkeutumiseen johtavien trombien muodostuminen ei välttämättä ole välttämätöntä toissijaisen TTP: n patogeneesissä. Näitä tekijöitä voidaan pitää myös toissijaisen aHUS: n muodona; ihmiset, joilla on nämä ominaisuudet, ovat siksi mahdollisia ehdokkaita antimplementtihoidolle.
Patofysiologia
Taustalla oleva mekanismi sisältää tyypillisesti auto-vasta-ainevälitteisen ADAMTS13- entsyymin estämisen , metalloproteaasin , joka on vastuussa suurten von Willebrand -tekijän (vWF) multimeerien katkaisemisesta pienemmiksi yksiköiksi. VWF: n kiertävien multimeerien lisääntyminen lisää verihiutaleiden tarttumista endoteelivaurion alueille , erityisesti kun arteriolit ja kapillaarit kohtaavat, mikä puolestaan johtaa pienten verihiutaleiden muodostumiseen, joita kutsutaan trombiksi. Koska verihiutaleet kuluvat trombien muodostumiseen, tämä johtaa sitten kiertävien verihiutaleiden määrän vähenemiseen, mikä voi sitten aiheuttaa hengenvaarallisia verenvuotoja. Mikroskooppisten hyytymien läpi kulkevat punasolut altistuvat leikkausjännitykselle , joka vahingoittaa niiden kalvoja, mikä johtaa punasolujen repeämiseen verisuonissa, mikä puolestaan johtaa anemiaan ja skistosyyttien muodostumiseen. Näiden verihyytymien esiintyminen pienissä verisuonissa vähentää verenkiertoa elimiin, mikä johtaa soluvammoihin ja elinvaurioihin .
Diagnoosi
Differentiaalinen diagnoosi
TTP: lle on tunnusomaista tromboottinen mikroangiopatia (TMA), verihyytymien muodostuminen koko kehon pieniin verisuoniin, mikä voi johtaa mikroangiopaattiseen hemolyyttiseen anemiaan ja trombosytopeniaan. Tällä ominaisuudella on kaksi samanlaista oireyhtymää, hemolyyttinen-ureeminen oireyhtymä (HUS) ja epätyypillinen hemolyyttinen ureeminen oireyhtymä (aHUS). Näin ollen näiden TMA: ta aiheuttavien sairauksien differentiaalidiagnoosi on välttämätöntä. TMA: n lisäksi kussakin näistä sairauksista voi esiintyä yksi tai useampi seuraavista oireista: neurologiset oireet (esim. Sekavuus, aivokouristuskohtaukset); munuaisten vajaatoiminta (esim. kohonnut kreatiniini , vähentynyt arvioitu glomerulusten suodatusnopeus [eGFR], epänormaali virtsa -analyysi); ja ruoansulatuskanavan (GI) oireet (esim. ripuli pahoinvointi/oksentelu, vatsakipu, gastroenteriitti. Toisin kuin HUS ja aHUS, TTP: n tiedetään johtuvan ADAMTS13 -proteiinin hankitusta puutteesta, joten laboratoriotesti osoittaa ≤5% normaalista ADAMTS13 -tasosta on osoitus TTP: stä. Yli 5%: n ADAMTS13-tasot yhdessä positiivisen shiga-toksiinin/enterohemorragisen E. colin (EHEC) -testin kanssa osoittavat todennäköisemmin HUS: a, kun taas shiga-toksiinin/EHEC: n puuttuminen voi vahvistaa aHUS-diagnoosin .
Hoito
Käsittelemättömän TTP: n suuren kuolleisuuden vuoksi oletettu TTP -diagnoosi tehdään silloinkin, kun vain mikroangiopaattinen hemolyyttinen anemia ja trombosytopenia havaitaan ja hoito aloitetaan. Verensiirto on vasta -aiheista tromboottisessa TTP: ssä, koska se ruokkii koagulopatiaa. 1990 -luvun alusta lähtien plasmafereesistä on tullut TTP: n suosituin hoito. Tämä on verenvaihdolla johon poistaminen henkilön veren plasman läpi afereesin ja korvaaminen luovuttajan plasmaa ( tuore plasma tai cryosupernatant ); Menettely on toistettava päivittäin estäjän poistamiseksi ja oireiden lievittämiseksi. Jos afereesi ei ole käytettävissä, tuoretta jäädytettyä plasmaa voidaan infusoida, mutta turvallisesti annettava määrä on rajoitettu nesteen ylikuormituksen vaaran vuoksi. Plasmainfuusio yksinään ei ole yhtä hyödyllinen kuin plasmanvaihto. Yleensä annetaan kortikosteroideja ( prednisoni tai prednisoloni ). Rituksimabia , monoklonaalista vasta -ainetta , joka on suunnattu CD20 -molekyyliin B -lymfosyyteissä , voidaan käyttää diagnoosissa; tämän uskotaan tappavan B -solut ja vähentävän siten estäjän tuotantoa. Vahvempi suositus rituksimabille on olemassa silloin, kun TTP ei reagoi kortikosteroideihin ja plasmafereesiin.
Kaplasitsumabi on vaihtoehtoinen vaihtoehto TTP: n hoidossa, koska sen on osoitettu nopeuttavan taudin paranemista verrattuna lumelääkettä saaneisiin. Kaplasitsumabin käyttöön liittyi kuitenkin lisääntynyt verenvuototaipumus tutkituilla.
Ihmiset, joilla on tulenkestävä tai uusiutuva TTP, voivat saada lisää immunosuppressiivista hoitoa, esim. Vinkristiini , syklofosfamidi , syklosporiini A tai pernanpoisto .
Lapset, joilla on Upshaw-Schülmanin oireyhtymä, saavat ennaltaehkäisevää plasmaa kahden tai kolmen viikon välein; tämä ylläpitää ADAMTS -toiminnan riittävää tasoa13. Jotkut sietävät pidempiä aikavälejä plasman infuusioiden välillä. Lisäplasmainfuusioita voi olla tarpeen tapahtumien, kuten leikkauksen, käynnistämiseksi; Vaihtoehtoisesti verihiutaleiden määrää voidaan seurata tarkasti näiden tapahtumien ympärillä ja plasmaa annetaan, jos määrä laskee.
Mittaukset veren laktaattidehydrogenaasin , verihiutaleet, ja schistocytes avulla seurataan taudin etenemistä tai peruutuksen. ADAMTS13-aktiivisuutta ja inhibiittoritasoja voidaan mitata seurannan aikana, mutta niillä, joilla ei ole oireita, rituksimabin käyttöä ei suositella.
Ennuste
Kuolleisuus on noin 95% hoitamattomissa tapauksissa, mutta ennuste on kohtuullisen suotuisa (80–90% eloonjääminen) ihmisille, joilla idiopaattinen TTP on diagnosoitu ja hoidettu aikaisin plasmafereesillä .
Epidemiologia
TTP: n esiintyvyys on noin 4-5 tapausta miljoonaa ihmistä kohti vuodessa. Idiopaattista TTP: tä esiintyy useammin naisilla ja afrikkalaisilla ihmisillä, ja autoimmuunisairauksista, kuten systeemisestä lupus erythematosuksesta, johtuva TTP esiintyy useammin afrikkalaista alkuperää olevilla ihmisillä, vaikka muut toissijaiset muodot eivät osoita tätä jakautumista. Raskaana olevien naisten ja naisten synnytyksen jälkeisen ajanjakson aikana joissakin tutkimuksissa oli huomattava osa (12–31%) tapauksista; TTP vaikuttaa noin jokaiseen 25 000 raskauteen.
Historia
TTP kuvasivat alun perin Eli Moschcowitz klo Beth Israel Hospital in New Yorkissa vuonna 1925. Moschcowitz johtuvan sairauden (virheellisesti, kuten nyt tiedossa) ja myrkyllinen syy. Moschcowitz huomasi, että hänen potilaallaan, 16-vuotiaalla tytöllä, oli anemia, pieniä ja suuria mustelmia, mikroskooppinen hematuria ja ruumiinavauksessa levinneet mikrovaskulaariset trombit. Vuonna 1966 16 uuden tapauksen ja 255 aiemmin raportoidun tapauksen tarkastelu johti klassisen oireiden ja löydösten (esim. Trombosytopenia, mikroangiopaattinen hemolyyttinen anemia, neurologiset oireet, munuaisten vajaatoiminta, kuume) muodostamiseen. tässä sarjassa kuolleisuuden todettiin olevan erittäin korkea (90%).
Vaikka vastaus verensiirtoon oli havaittu aiemmin, vuoden 1978 raportti ja myöhemmät tutkimukset osoittivat, että veriplasma oli erittäin tehokas parantamaan sairausprosessia. Vuonna 1991 raportoitiin, että plasmanvaihto tarjoaa paremman vasteen verrattuna plasman infuusioon. Vuonna 1982 tauti oli yhdistetty epänormaalin suuriin von Willebrand -tekijän multimeereihin. Puutteellinen proteaasi tunnistettiin TTP -potilailla vuonna 1998. ADAMTS13: n sijainti ihmisen genomissa tunnistettiin vuonna 2001.
Viitteet
Ulkoiset linkit
| Luokitus | |
|---|---|
| Ulkoiset resurssit |

