Sjögrenin oireyhtymä - Sjögren syndrome
| Sjögrenin oireyhtymä | |
|---|---|
| Muut nimet | Sjögrenin oireyhtymä, siccan oireyhtymä |
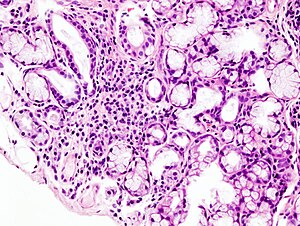 | |
| Kuva mikroskoopilla fokaalisesta imusolmukkeesta Sjögrenin oireyhtymään liittyvässä pienessä sylkirauhasessa. | |
| Ääntäminen | |
| Erikoisuus |
Immunologia , reumatologia |
| Oireet | Kuiva suu , kuivat silmät , muut kuivuusalueet |
| Komplikaatiot | Lymfooma |
| Tavallinen alku | Keski-ikä |
| Kesto | Pitkäaikainen |
| Syyt | Autoimmuunisairaus (tuntematon syy) |
| Diagnostinen menetelmä | Kudosbiopsia , verikokeet |
| Differentiaalinen diagnoosi | Lääkkeiden sivuvaikutus, ahdistuneisuus , sarkoidoosi , amyloidoosi |
| Hoito | Keinotekoiset kyyneleet , tulehdusta vähentävät lääkkeet, leikkaus |
| Ennuste | Normaali elinajanodote |
| Taajuus | ~ 0,7% |
Sjögrenin oireyhtymä ( SjS , SS ) on pitkäaikainen autoimmuunisairaus, joka vaikuttaa kehon kosteutta tuottaviin (kyynel- ja sylki) rauhasiin ja vaikuttaa usein vakavasti muihin elinjärjestelmiin, kuten keuhkoihin, munuaisiin ja hermostoon. Ensisijaisia oireita ovat kuivuus ( suun kuivuminen ja silmien kuivuminen ), kipu ja väsymys . Muita oireita voivat olla kuiva iho , emättimen kuivuus, krooninen yskä, käsien ja jalkojen tunnottomuus, väsymys , lihas- ja nivelkivut sekä kilpirauhasongelmat . Myös kärsivillä on suurempi riski (15%) lymfoomaan .
Vaikka tarkka syy on epäselvä, sen uskotaan sisältävän geneettisen yhdistelmän ja ympäristön laukaisijan , kuten altistumisen virukselle tai bakteerille . Se voi ilmetä muista terveysongelmista riippumatta (primaarinen Sjögrenin oireyhtymä) tai jonkin muun sidekudoshäiriön (toissijainen Sjögrenin oireyhtymä) seurauksena. Sjögrenin oireyhtymä voi liittyä muihin autoimmuunisairauksiin, mukaan lukien nivelreuma (RA), systeeminen lupus erythematosus (SLE) tai systeeminen skleroosi. Tulehdus , joka johtaa vähitellen vahingoittaa rauhaset. Diagnoosi tehdään kosteutta tuottavien rauhasien biopsialla ja verikokeilla spesifisten vasta-aineiden löytämiseksi . On biopsia on tyypillisesti lymfosyyttejä sisällä rauhaset.
Vaikka Sjögrenin oireyhtymä on yksi yleisimmistä autoimmuunisairauksista, sillä ei ole erityisiä ja ei-invasiivisia diagnostisia testejä, ja hoito on suunnattu henkilön oireiden hallintaan . Silmien kuivumista, keinotekoisia kyyneleitä , tulehdusta vähentäviä lääkkeitä, pistotulppia tai kyynelkanavien sulkemista voidaan kokeilla. Suun kuivumista varten voidaan käyttää purukumia (mieluiten sokeritonta), siemailuvettä tai syljen korviketta . Niille, joilla on nivel- tai lihaskipuja, voidaan käyttää ibuprofeenia . Kuivuutta aiheuttavat lääkkeet, kuten antihistamiinit , voidaan myös lopettaa. Tarkin olemassa oleva diagnostinen testi vaatii huulibiopsian.
Taudin kuvasi vuonna 1933 Henrik Sjögren , jonka mukaan se on nimetty; on kuitenkin olemassa useita aiempia kuvauksia oireista kärsivistä ihmisistä. Tämä vaikuttaa 0,2–1,2 prosenttiin väestöstä, joista puolet on ensisijainen ja puolet toissijainen. Naiset kärsivät noin 10 kertaa niin usein kuin miehet. Vaikka tauti alkaa yleensä keski -iässä , kuka tahansa voi vaikuttaa siihen. Niiden joukossa, joilla ei ole muita autoimmuunisairauksia, elinajanodote on ennallaan.
Merkit ja oireet
Sjögrenin oireyhtymän tunnusmerkki on suun kuivuminen ja keratoconjunctivitis sicca (kuivat silmät). Myös emättimen kuivuutta , kuivaa ihoa ja kuivaa nenää voi esiintyä. Myös muut kehon elimet voivat vaikuttaa, mukaan lukien munuaiset, verisuonet, keuhkot, maksa, haima ja aivot.
Ihon kuivumista joillakin ihmisillä SS voi johtua lymfosyyttinen infiltraatio osaksi ihoon rauhaset . Oireet voivat kehittyä salakavalasti, ja diagnoosia ei usein harkita useaan vuoteen, koska sicca voi johtua lääkkeistä, kuivasta ympäristöstä tai ikääntymisestä tai sitä ei voida pitää sellaisena, että sen vakavuus edellyttää perusteellista tutkimusta. taustalla oleva autoimmuunisairaus.
Sjögrenin oireyhtymä voi vahingoittaa elintärkeitä elimiä oireilla, jotka voivat tasaantua tai pahentua tai mennä remissioon , kuten muidenkin autoimmuunisairauksien yhteydessä. Jotkut ihmiset voivat kokea vain lieviä oireita silmien ja suun kuivumisesta, kun taas toisilla on oireita vakavasta sairaudesta. Monet potilaat voivat hoitaa ongelmia oireenmukaisesti . Toiset kokevat näön hämärtyminen , vakio silmävaivaa toistuvia suun infektiot , turvonnut korvasylkirauhasista , dysfonia ( laulu häiriöt kuten käheys), ja nielemisvaikeuksia ja syöminen. Heikottava väsymys ja nivelkipu voivat heikentää vakavasti elämänlaatua. Joillekin potilaille voi kehittyä munuaisten toiminta (autoimmuuni tubulointerstitiaalinen nefriitti ), joka johtaa proteinuriaan (ylimääräinen proteiini virtsassa), virtsan keskittymishäiriöön ja distaaliseen munuaistiehyiden asidoosiin .
Komplikaatiot
Edellä käsitellyistä komplikaatioista raskaana olevilla naisilla, joilla on anti-Ro/SS-A- ja anti-La/SS-B-vasta-aineita, on lisääntynyt vastasyntyneen lupus erythematosus ja synnynnäinen sydämen lohko, joka vaatii sydämentahdistinta . Tyypin I kryoglobulinemia on tunnettu Sjögrenin oireyhtymän komplikaatio.
Sjögrenin oireyhtymä voi vaikuttaa sellaisiin elimiin kuin maksa, haima, munuaiset, keuhkot ja keskushermosto.
Liittyvät ehdot
Sjögrenin oireyhtymään liittyy useita muita sairauksia, joista monet ovat autoimmuuni- tai reumaattisia häiriöitä, kuten keliakia , fibromyalgia , SLE (lupus) , autoimmuuninen kilpirauhastulehdus , multippeliskleroosi ja spondyloartropatia ja useita pahanlaatuisia sairauksia , pääasiassa ei-Hodgkin-lymfooma .
Syyt
Sjögrenin oireyhtymän syy on tuntematon, mutta se voi olla geneettisten, ympäristöllisten ja muiden tekijöiden yhdistelmän vaikutus, kuten monien muiden autoimmuunisairauksien tapauksessa. Mukana voi olla noin 20 autovasta -ainetta.
Genetiikka
Autoimmuunisairauksien korkean esiintymisen havaitseminen perheissä, joilla on ollut Sjögrenin oireyhtymä, liittyy geneettiseen taipumukseen oireyhtymään. Tutkimukset polymorfismeja on HLA (HLA)-DR ja HLA-DQ -geenin alueet Sjögrenin potilaalla ilmenee ero herkkyydessä oireyhtymä seurauksena eri tuloksena autovasta- tuotantoa.
Hormonit
Koska Sjögrenin oireyhtymään liittyy suuri esiintyvyys naisilla, sukupuolihormonien , erityisesti estrogeenin , uskotaan vaikuttavan humoraalisiin ja soluvälitteisiin immuunivasteisiin, jotka vaikuttavat alttiuteen oireyhtymään. Androgeenien katsotaan yleensä estävän autoimmuunia. Hiirimalleilla tehdyt tutkimukset viittaavat siihen, että estrogeenin puutos stimuloi autoantigeenien esittelyä aiheuttaen Sjögrenin kaltaisia oireita.
Mikrokimerismi
Microchimerism sikiön solujen (jälkeläisiä imusoluissa vuonna äidin verenkiertoon ) voi synnyttää autoimmuniteetin naisilla, jotka ovat aiemmin olleet raskaana . Autoimmuunipotentiaalin muodostuminen mikrokimerismin kautta voi johtaa siirtymiseen hiljaisesta autoimmuunimuodosta ja iästä riippuvaiseen itsesietokyvyn heikkenemiseen .
Ympäristö
Virusproteiinit , imeytyneet molekyylit tai heikentyneet itserakenteet voivat käynnistää autoimmuunisuuden molekyylien matkimalla ja lisätä Sjögrenin oireyhtymän kehittymisen mahdollisuuksia. Epstein-Barrin virus , hepatiitti C ja ihmisen T-soluleukemiavirus-1 ovat Sjögrenin oireyhtymän eniten tutkittuja tartuntatauteja . Toistaiseksi näiden patogeenien ja Sjögrenin oireyhtymän kehittymisen välillä ei ole tunnistettu suoria syitä ja seurauksia. Vaurioituneet itserakenteet, jotka on kohdistettu apoptoosiin, voivat vahingossa altistua immuunijärjestelmälle, mikä laukaisee autoimmuunisuuden eksokriinisissa rauhasissa , jotka ovat usein alttiita autoimmuunivasteille.
Patogeneesi
Patogeneettiset mekanismit Sjögrenin syndrooma ei ole täysin selvitetty, mikä puute patofysiologian tiedon hallinnoinnin autoimmuunisairauksien exocrinopathy . Vaikka lukuisat tämän taudin etenemiseen vaikuttavat tekijät ovat tehneet tarkan alkuperän löytämisen ja syyn vaikeaksi, viime vuosikymmenen aikana saavutetut merkittävät edistysaskeleet ovat vaikuttaneet ehdotettuun patogeenisten tapahtumien sarjaan, jotka tapahtuvat ennen Sjögrenin oireyhtymän diagnosointia.
Sjögrenin oireyhtymää ehdotettiin alun perin erityiseksi, itseään ylläpitäväksi , immuunijärjestelmän välittämäksi eksokriinisten rauhasien, erityisesti acinaaristen ja duktaalisten solujen , menetykseksi . Vaikka tämä selittää ilmeisemmät oireet (kuten syljen ja kyynelnesteen puutteen ), se ei selitä laajempaa systeemistä vaikutusta, joka on havaittu taudin etenemisessä.
Jos on olemassa herkkä geneettinen tausta , sekä ympäristön että hormonaalisten tekijöiden uskotaan voivan laukaista imusolujen, erityisesti CD4+ T -solujen , B -solujen ja plasmasolujen , tunkeutumisen aiheuttaen sylki- ja kyynelrauhasen toimintahäiriöitä.
Sjögrenin oireyhtymä liittyy lisääntynyt tasojen aivo-selkäydinnesteessä (CSF) IL-1 RA , interleukiini 1 antagonisti . Tämä viittaa siihen, että taudin alkaa lisääntynyt aktiivisuus interleukiini 1 järjestelmä, jota seuraa itsesäätelydomeenin ylössäätely IL-1 RA: n vähentämiseksi onnistuneen sitoutumisen interleukiini-1 sen reseptoreihin. Interleukiini 1 on todennäköisesti väsymyksen merkki , mutta lisääntynyt IL -1RA havaitaan CSF: ssä ja siihen liittyy lisääntynyt väsymys sytokiinien aiheuttaman sairauskäyttäytymisen kautta . Sjögrenin oireyhtymälle on kuitenkin tunnusomaista syljen IL-1ra-tasojen lasku, mikä voi aiheuttaa suun tulehdusta ja kuivumista. Toissijaista Sjögrenin oireyhtymää sairastavilla potilailla on usein myös merkkejä ja oireita ensisijaisista reumaattisista häiriöistään, kuten systeeminen lupus erythematosus , nivelreuma tai systeeminen skleroosi .
Geneettinen taipumus
Geneettinen lokus merkittävimmin liittyy ensisijaisesti SS on major histocompatibility complex / HLA (MHC / HLA) alue, kuten on osoitettu alustavat tulokset ensimmäisen genomin laajuinen yhdistys tutkimuksessa . Tämä tutkimus sisälsi tietoja 395 eurooppalaisesta syntyperäisestä potilaasta, joilla oli primaarinen Sjögrenin oireyhtymä, ja 1 975 terveestä kontrollipotilaasta löytyneestä kohortista ja replikointitutkimuksesta, joka käsitti 1234 tapausta ja 4779 tervettä kontrollia. Lisäksi havaittiin assosiaatioita polymorfismeihin, jotka sijaitsevat kuudessa itsenäisessä lokuksessa; IRF5 , STAT4 , BLK , IL12A , TNIP1 , ja CXCR5 . Tämä viittasi myös synnynnäisen immuunijärjestelmän aktivoitumiseen , erityisesti IFN-järjestelmän kautta, B-solujen aktivointiin CXCR5-suunnatun rekrytoinnin avulla imusolmukkeisiin ja B-solureseptorin (BCR) aktivointiin, johon liittyy BLK , ja T-solujen aktivaatioon HLA-herkkyyden vuoksi ja IL-12-IFN-y-akseli.
Potilasta eri etnistä alkuperää kuljettaa eri HLA-alttiutta alleelit , joista HLA-DR ja HLA-DQ osallistuvat patogeneesissä Sjögrenin syndrooma. Esimerkiksi potilailla Pohjois- ja Länsi -Euroopasta ja Pohjois -Amerikasta esiintyy paljon B8-, DRw52- ja DR3 -geenejä. HLA -luokan II alleelit liittyvät pikemminkin tiettyjen auto -vasta -aineiden alaryhmien esiintymiseen kuin itse tautiin. Autovasta-aineilla tarkoitetaan B-solutoleranssin menettämistä, mikä johtaa vasta-aineiden tuotantoon eri elinspesifisiä ja elinten epäspesifisiä antigeenejä vastaan. Yhteys HLA: n ja SS: n välillä rajoittuu potilaisiin, joilla on anti-SSA/Ro- tai anti-SSB/La-vasta-aineita. Anti-Ro: n ja anti-La: n seropositiivisuus liittyy taudin vakavuuteen ja pidempään kestoon, ja havainnot niiden suuresta runsaudesta Sjögrenin potilaiden sylkirauhasista viittaavat niiden pakolliseen rooliin SS: n patogeneesissä.
Genetiikan lisäksi DNA: n metylaatioon , histonin asetylointiin tai mikroRNA: n ilmentymiseen liittyvällä epigeneettisellä epänormaalisuudella on luultavasti keskeinen rooli autoimmuunisairauksien, mukaan lukien Sjögrenin oireyhtymä, patogeneesissä, vaikka tämän alan tutkimus on hyvin rajallista.
Ympäristön laukaisimet
Ympäristötekijät, kuten rauhasen virusinfektio , voivat saada epiteelisolut aktivoimaan HLA-riippumattoman luontaisen immuunijärjestelmän tietullien kaltaisten reseptorien kautta . Vaikka Sjögrenin oireyhtymän patogeneesiin on liittynyt useita tarttuvia, eksogeenisiä tekijöitä, kuten Epstein-Barrin virus (EBV), ihmisen T-lymfotrooppinen virus 1 ja hepatiitti C-virus , niiden yhteys Sjögrenin oireyhtymään vaikuttaa heikolta. Vaikka EBV: tä esiintyy normaalien yksilöiden sylkirauhasissa, EBV: n uudelleenaktivoitumista Sjögrenin potilailla on raportoitu runsaasti, ja EBV -DNA: n pitoisuudet ovat lisääntyneet . Tämä osoittaa viruksen uudelleenaktivoitumisen ja imusolmukkeiden infiltraattien kyvyttömyyden hallita EBV: n replikaatiota Sjögrenin oireyhtymässä, mikä johtaa immuunivasteen alkamiseen tai jatkumiseen kohde -elimissä. Siitä huolimatta, miten EBV: n uudelleenaktivointi indusoidaan Sjögrenin oireyhtymää sairastavien potilaiden leesioissa ja mitkä erityiset molekyylimekanismit ovat mukana viruksen uudelleenaktivointiprosessissa, on vielä selvitettävä.
Tulehdus
Epiteelisolut Sjögrenin oireyhtymän leesioissa ovat aktiivisia osallistujia tulehdusprosessin indusoimiseen ja jatkamiseen. Ympäristö- ja hormonaaliset tekijät, konsertti sopivan geneettinen tausta, uskotaan laukaista Sjögrenin oireyhtymä, joka dysregulates epiteelisolujen ja mahdollistaa poikkeavan itseohjautuva ja aktivaation dendriittisolujen (DC), T-solut, ja B-solut. Dendriittisolut ovat antigeenia esittelevät solut, jotka käsittelevät antigeenimateriaalia ja esittävät sen muille T-soluille. Jälkeen muuttoliike lymfosyyttikertymiä rauhasten vastauksena kemokiinien ja erityisiä adheesiomolekyylien , T-solut ovat vuorovaikutuksessa epiteelisoluihin. Epiteelisoluja aktivoivat edelleen proinflammatoriset sytokiinit (IL-1β, IFN-y ja TNF), joita viereiset T-solut tuottavat. Plasmasytoididendriittisolujen varhainen kertyminen kohdekudoksiin, jotka tuottavat suuria määriä tyypin 1 IFN: itä, vaikuttaa tärkeältä, koska nämä solut voivat edelleen säätää immuunivastetta säätelemällä epänormaalia lymfosyyttien retentiota kudoksissa ja niiden aktivoitumista myöhemmin. IFN-a stimuloi B-solua aktivoivan tekijän (BAFF) tuotantoa epiteelisoluissa, DC-soluissa ja T-soluissa. BAFF stimuloi poikkeava B-solujen kypsymisen, mikä johtaa syntymistä itsereaktiivisten B-solut, jotka paikallisesti tuottavat autovasta-aineita, on itukeskuksen kaltainen rakenne (GC-kaltainen), joka on myös sijainnin lymphomagenesis (alkuperä lymfooma ).
Ohjelmoitu solukuolema
Apoptoosin (ohjelmoidun solukuoleman) säätelyn uskotaan vaikuttavan monenlaisten autoimmuunisairauksien patogeneesiin, vaikka sen rooli Sjögrenin oireyhtymässä on kiistanalainen. Sekä Fas ja Fas-ligandin proteiinit yli-ilmentyneet primaarisessa Sjögrenin potilailla, kun taas ekspressio BCL-1 , joka on tunnettua säädellä alaspäin apoptoosin, havaittiin pienentynyt merkittävästi acinar ja duktaalisessa epiteelisolujen Sjögrenin potilailla verrattuna terveisiin ihmisiä. In situ -tutkimukset eivät osoittaneet lisääntynyttä apoptoosia rauhasen epiteelisolujen keskuudessa, mutta osoittivat vähentynyttä apoptoosia soluttautuvien mononukleaaristen solujen keskuudessa. Vähentynyt apoptoosi liittyi myös rauhasista löytyvien autoreaktiivisten B-solujen kertymiseen. Sjögrenin oireyhtymässä ilmenneiden auto -vasta -aineiden suhdetta apoptoosiin tutkitaan edelleen.
Hormonaaliset tekijät
Sukupuolihormonien näytä vaikuttavan humoraalisten ja soluvälitteisten immuunivaste, jossa estrogeenin pidetään yhtenä suurimmista tekijöistä vastuussa sukupuoleltaan immunologisen dimorphism . Estrogeenin puutos näyttää vaikuttavan Sjögrenin oireyhtymän kehittymiseen. On oletettu, että androgeenin antaminen silmän pinnalle voi toimia tehokkaana hoitona kuiville silmille.
Diagnoosi
Sjögrenin oireyhtymän (SS) diagnosointi on monimutkaista potilaan mahdollisesti ilmenevien oireiden sekä Sjögrenin oireyhtymän ja muiden sairauksien oireiden samankaltaisuuden välillä. Myös potilaat, joilla on SS -oireita, lähestyvät eri erikoisaloja hoitoon, mikä voi vaikeuttaa diagnoosia. Koska kuivat silmät ja suun kuivuminen ovat hyvin yleisiä oireita ja niitä esiintyy usein yli 40-vuotiailla, sairastuneet ihmiset saattavat uskoa oireiden olevan ikään liittyviä, joten jätä ne huomiotta. Jotkut lääkkeet voivat aiheuttaa samanlaisia oireita kuin Sjögrenin oireyhtymä. Useiden testien yhdistelmä, joka voidaan tehdä sarjassa, voi lopulta diagnosoida Sjögrenin oireyhtymän.
Verikokeilla voidaan määrittää, onko potilaalla korkeita vasta -aineita, jotka viittaavat sairauteen, kuten antinukleaarinen vasta -aine (ANA) ja nivelreuma (koska Sjögrenin oireyhtymä esiintyy usein nivelreuman toissijaisena), jotka liittyvät autoimmuunisairauksiin . Tyypillisiä SS ANA -malleja ovat SSA/Ro ja SSB/La , joista anti-SSB/La on paljon spesifisempi; anti-SSA/Ro liittyy lukuisiin muihin autoimmuunisairauksiin, mutta esiintyy usein SS: ssä, mutta aAnti-SSA- ja anti-SSB-testit eivät usein ole positiivisia SS: ssä.
Rose Bengal testi käyttää tahra, että toimenpiteet ilmoitettava ja toiminta kyynelrauhaset . Tämä testi sisältää myrkyttömän ruusu -bengali -väriaineen asettamisen silmiin. Väriaineen erottuva väri auttaa määrittämään kyynelkalvon tilan ja toiminnan sekä kyynelien haihtumisnopeuden. Mikä tahansa erottuva värinmuutos voi ilmaista SS: n, mutta tilan vahvistaminen vaatii monia asiaan liittyviä diagnostiikkatyökaluja .
Schirmerin testi mittaa kyyneleiden tuotantoa: suodatinpaperinauhaa pidetään alaluomen sisällä viiden minuutin ajan, ja sen kosteus mitataan sitten viivaimella. Alle 5 mm: n (0,20 tuuman) nesteen tuottaminen on yleensä merkki SS: stä. Tämä mittausanalyysi vaihtelee ihmisten välillä riippuen muista silmiin liittyvistä tiloista ja lääkkeistä, joita käytetään testin aikana. Rakolamppututkimus voi paljastaa kuiviin silmän pintaa.
Suun kuivumisen ja suuontelon kuivuuden oireet johtuvat syljen vähentyneestä sylkirauhasesta ( korvasylkirauhasesta , submandibulaarisesta ja sublingvaalisesta rauhasesta ). Sylkirauhasen tilan ja syljen tuotannon tarkistamiseksi suoritetaan syljen virtausnopeustesti, jossa henkilöä pyydetään sylkemään kuppiin niin paljon kuin mahdollista ja tuloksena oleva syljenäyte kerätään ja punnitaan. Tämän testin tulokset voivat määrittää, toimivatko sylkirauhaset kunnolla. Liian vähän sylkeä voi tarkoittaa, että henkilöllä on SS. Vaihtoehtoinen testi on stimuloimaton koko syljen virtauskeräys, jossa henkilö sylkee koeputkeen joka minuutti 15 minuutin ajan. Alle 1,5 ml: n (0,053 imp fl oz; 0,051 US fl oz) keräämistä pidetään positiivisena tuloksena.
Huuli / sylkirauhasen biopsia otetaan kudosnäyte, joka voi paljastaa lymfosyytit ryhmittyneet noin sylkirauhaset, ja vahingoittaa nämä rauhaset tulehdus. Tämä testi sisältää kudosnäytteen poistamisen henkilön sisähuulista/sylkirauhasesta ja sen tutkinnan mikroskoopilla . Lisäksi suoritetaan sialogrammi , erityinen röntgentesti , joka osoittaa, onko sylkirauhasen kanavissa (eli parotid-kanavassa ) tukos ja suuhun virtaavan syljen määrä.
Radiologinen toimenpide on saatavana luotettavana ja tarkana testinä Sjögrenin oireyhtymälle. Varjoainetta ruiskutetaan parotid kanavaan, joka avautuu posken osaksi eteinen suun vastapäätä kaulan ylemmän toisen poskihampaiden . Histopatologisten tutkimusten pitäisi osoittaa fokaalinen lymfosyyttinen sialadeniitti . Objektiivista näyttöä sylkirauhasten osallistuminen on testattu kautta ultraääni tutkimukset, taso stimuloimattomassa koko syljen, joka on korvasylkirauhasessa sialography tai syljen skintigrafiaa , ja autovasta-aineita Ro (SSA) ja / tai La (SSB) antigeenejä.
Sjögrenin oireyhtymä voidaan sulkea pois ihmisiltä, joilla on aiemmin ollut pään ja kaulan sädehoitoa , hankittu immuunipuutosoireyhtymä , aiemmin esiintynyt lymfooma , sarkoidoosi , siirte-isäntäsairaus ja antikolinergisten lääkkeiden käyttö .
Ehkäisy
Sjögrenin oireyhtymälle (SS) ei ole olemassa ehkäisymekanismia, koska se on monimutkainen autoimmuunisairautena, mutta elämäntapamuutokset voivat vähentää SS: n kehittymiseen liittyviä riskitekijöitä tai vähentää tilan vakavuutta potilaille, joilla on jo diagnoosi. Ruokavalio liittyy vahvasti tulehdukseen, jota havaitaan monissa autoimmuunisairauksissa, mukaan lukien SS. Kokeellinen tutkimus totesi, että SS-potilailla on usein osoittavat suurta herkkyyttä gluteenia , että suoraan liittyy tulehdus. Kohtuullinen liikunta on hyödyllistä myös SS -potilailla, mikä vähentää pääasiassa keuhkotulehduksen vaikutusta.
Hoito
Sjögrenin oireyhtymän parannuskeinoa tai erityishoitoa ei tiedetä palauttavan pysyvästi rauhasen eritystä . Sen sijaan hoito on yleensä oireenmukaista ja tukevaa.
Silmähuolto
Kosteutta korvaavat hoidot, kuten keinotekoiset kyyneleet, voivat helpottaa kuivien silmien oireita. Jotkut potilaat, joilla on vakavampia ongelmia, käyttävät suojalaseja paikallisen kosteuden lisäämiseen tai asettavat pistotulppia pitämään kyyneleet silmän pinnalla pidempään.
Lisäksi syklosporiinia (Restasis) on saatavana reseptillä kroonisen kuivan silmän hoitoon tukahduttamalla kyynelien eritystä häiritsevä tulehdus. Saatavilla on myös reseptilääkkeitä , jotka edistävät syljen virtausta, kuten cevimeline (Evoxac) ja pilokarpiini. Salagenia , valmistettua pilokarpiinin muotoa , voidaan käyttää kyyneleiden sekä syljen tuottamiseen suussa ja suolistossa. Se on peräisin jaborandi -kasvista .
Emättimen kuivuus
Naisilla, joilla on Sjögrenin oireyhtymä, raportoidaan usein emättimen kuivuutta, vulvodyniaa ja dyspareuniaa (kivulias yhdyntä ); henkilökohtaisia voiteluaineita suositellaan vähentämään ärsytystä tai kipua, joka voi johtua emättimen ja vulvaalisten alueiden kuivumisesta .
Tuki- ja liikuntaelimistö
Ei-steroidisia tulehduskipulääkkeitä (NSAID) voidaan käyttää tuki- ja liikuntaelimistön oireiden hoitoon. Henkilöille, joilla on vakavia komplikaatioita , voidaan määrätä kortikosteroideja tai immunosuppressiivisia lääkkeitä ja joskus laskimonsisäisiä immunoglobuliineja . Myös sairautta muuttavat reumalääkkeet , kuten metotreksaatti, voivat olla hyödyllisiä. Hydroksiklorokiini (Plaquenil) on toinen vaihtoehto, ja sitä pidetään yleensä turvallisempana kuin metotreksaattia. Näillä määrätyillä lääkkeillä on kuitenkin useita sivuvaikutuksia , kuten pahoinvointi , ruokahaluttomuus , huimaus , hiustenlähtö , vatsakipu/-krampit , päänsärky , maksatoksisuus ja lisääntynyt infektioriski . Myös ne, jotka ottavat lääkkeitä immuunijärjestelmän tukahduttamiseksi, kehittyvät todennäköisemmin syöpään myöhemmin.
Systeeminen
Systeemisten oireiden, kuten väsymyksen, nivelkivun, myosiitin ja neuropatian , hoitoon käytetään usein biologisia immunosuppressiivisia lääkkeitä, kuten rituksimabia ja belimumabia, jotka toimivat B- solupatologian kautta ja joilla on vähemmän toksisia profiileja kuin perinteisillä immunosuppressiivisilla hoito-ohjelmilla.
Hammashoito
Ennaltaehkäisevä hammashoito on myös välttämätöntä (ja potilas usein jättää sen huomiotta), koska kserostomiaan liittyvä syljen puute luo ihanteellisen ympäristön onteloita aiheuttavien bakteerien lisääntymiselle . Hoitoihin kuuluu kotona käytettävä paikallinen fluoridihammaskiilteen vahvistaminen ja hammashygienistin suorittamat usein suorittamat hampaiden puhdistukset. Olemassa olevia onteloita on myös käsiteltävä, koska hampaan ulottuvia onteloita ei voida hoitaa tehokkaasti pelkällä hampaiden puhdistuksella, ja niillä on suuri riski levitä hampaan massaan , mikä johtaa elinvoiman menettämiseen ja uutto- tai juuritarpeeseen kanavahoito . Tämä hoito -ohjelma on sama kuin kaikilla kserostomiapotilailla, kuten pään ja kaulan sädehoidolla, joka usein vahingoittaa sylkirauhasia; nämä rauhaset ovat alttiimpia säteilylle kuin muut kehon kudokset.
Ennuste
Julkaistut tutkimukset Sjögrenin oireyhtymän potilaiden selviytymisestä ovat rajallisia eri suhteissa, ehkä johtuen suhteellisen pienistä otoskokoista ja siitä, että toissijainen Sjögrenin oireyhtymä liittyy muihin autoimmuunisairauksiin. Useiden tutkimusten tulokset osoittavat, että muihin autoimmuunisairauksiin verrattuna Sjögrenin oireyhtymään liittyy pahanlaatuisen non-Hodgkin-lymfooman , valkosolujen syövän, esiintyvyys. Noin 5%: lla SS -potilaista kehittyy jonkinlainen pahanlaatuinen imusolmuke . Potilailla, joilla on vakavia tapauksia, kehittyy paljon todennäköisemmin lymfoomia kuin potilailla, joilla on lieviä tai kohtalaisia tapauksia. Yleisimpiä lymfoomia ovat syljen ulkopuoliset marginaalivyöhykkeen B-solulymfoomat ( MALT-lymfoomat sylkirauhasissa) ja diffuusi suuri B-solulymfooma .
Lymfomageneesia ensisijaisissa Sjögrenin oireyhtymäpotilaissa pidetään monivaiheisena prosessina, ja ensimmäinen vaihe on autoimmuunisten B -solujen krooninen stimulaatio, erityisesti B -solut, jotka tuottavat reumatoidista tekijää sairauden kohteena olevissa kohdissa. Tämä lisää onkogeenisten mutaatioiden esiintymistiheyttä , mikä johtaa toimintahäiriöihin autoimmuunisen B-solun aktivaation tarkistuspisteissä ja muuttuu pahanlaatuiseksi. Tutkimuksen havainto on johtanut autoimmuunisten B -solujen jatkuvaan stimulaatioon, mikä johtaa hienovaraisiin itävään poikkeavuuksiin geeneissä, joilla on erityisiä seurauksia B -soluissa, mikä on alttius lymfoomalle.
Pahanlaatuisen NHL: n huomattavasti suuremman ilmaantuvuuden lisäksi Sjögrenin potilailla on vain vähäistä tai kliinisesti merkityksetöntä elintoimintoihin liittyvän toiminnan heikkenemistä, mikä selittää Sjögrenin potilaiden kuolleisuuden vain vähäisen nousun verrattuna muuhun väestöön.
Sjögrenin oireyhtymään liittyy suuri sairauskuormitus, ja sen on osoitettu heikentävän merkittävästi elämänlaatua ja vaikuttavan merkittävästi työkykyyn lisääntyneen vammaisuuden vuoksi. QoL: n lasku on samanlainen kuin muissa kroonisissa sairauksissa, kuten nivelreumassa , lupuksessa ja fibromyalgiassa .
Epidemiologia
Sjögrenin oireyhtymä (SS) on toiseksi yleisin reumaattinen autoimmuunisairaus, nivelreuman ja systeemisen lupus erythematosuksen jälkeen . SS -kursseissa ei ole maantieteellisiä eroja. Sjögrenin oireyhtymää on raportoitu kaikilla maailman alueilla, vaikka alueellisia määriä ei ole tutkittu hyvin. Leviämisen määrittämisperusteista riippuen tutkimukset arvioivat SS: n esiintyvyyden 500 000 - 2 miljoonan ihmisen välillä Yhdysvalloissa. Laajemmat tutkimukset SS -esiintyvyydestä vaihtelevat laajasti, ja joidenkin raporttien mukaan esiintyvyys on jopa 3% väestöstä. Muutamat tutkimukset ovat raportoineet, että oireyhtymän ilmaantuvuus vaihtelee kolmesta kuuteen kuuteen / 100 000 vuodessa.
Yhdeksän kymmenestä SS -potilaasta on naisia. Naisilla esiintyvyyden lisäksi epidemiologisina riskitekijöinä on todettu ensimmäisen asteen sukulainen, jolla on autoimmuunisairaus ja aiemmat raskaudet. Huolimatta miesten pienemmästä riskistä, ensisijainen SS miehillä on yleensä vakavampi taudin muoto. Rotuun ja etnisyyteen liittyvä rooli taudin esiintymisessä on tuntematon.
Vaikka Sjögrenin oireyhtymää esiintyy kaikissa ikäryhmissä, keskimääräinen alkamisikä on 40-60 -vuotiaita, vaikka jopa puolet kaikista tapauksista voidaan jättää diagnosoimatta tai ilmoittamatta. SS: n esiintyvyys lisääntyy yleensä iän myötä.
Sjögrenin oireyhtymää raportoidaan 30-50%: lla nivelreumaa sairastavista ja 10-25%: lla systeemistä lupus erythematosusta.
Historia
Jan Mikulicz-Radecki (1850–1905) on yleensä saanut ensimmäisen SS-kuvauksen. Vuonna 1892 hän kuvasi 42-vuotiasta miestä, jolla oli korvasylkirauhasen ja kyynelrauhasen laajentuminen, joka liittyi pyöreän solun infiltraattiin ja asinaariseen atrofiaan . Kuitenkin ne kriteerit, jotka Mikulicz vahvistettu diagnoosi usein johtanut väärän diagnoosin ja Mikulicz oireyhtymä . Monet sairaudet, kuten tuberkuloosi , infektiot, sarkoidoosi ja lymfooma, ovat samankaltaisia kuin Mikuliczin oireyhtymä. Siitä huolimatta termiä "Mikuliczin oireyhtymä" käytetään edelleen satunnaisesti kuvaamaan lymfosyyttisten infiltraattien esiintymistä sylkirauhasen biopsioissa.
Vuonna 1930 Jönköpingissä , Ruotsissa , silmälääkäri Henrik Sjögren (1899–1986) havaitsi potilaan, jolla oli alhaiset eritteet kyynel- ja sylkirauhasista. Sjögren esitteli termin keratoconjunctivitis sicca kuivan silmän oireeksi ( keratoconjunctivitis ). Vuonna 1933 hän julkaisi väitöskirjansa, jossa kuvattiin 19 naista, joista suurin osa oli vaihdevuodet ohittaneita ja joilla oli niveltulehdus. Sjögren selvensi, että keratoconjunctivitis sicca, joka johtuu veden puutteesta, ei liity A -vitamiinin puutteesta johtuvaan kseroftalmiaan . Sjögrenin väitöskirjaa ei otettu hyvin vastaan, koska tarkastajien lautakunta kritisoi joitain kliinisiä näkökohtia.
Laajan tutkimuksen ja tiedonkeruun jälkeen Sjögren julkaisi tärkeän asiakirjan vuonna 1951, jossa kuvattiin 80 potilasta, joilla oli keratoconjunctivitis sicca , joista 50: llä oli myös niveltulehdus. Hänen myöhemmät hänen paperiinsa liittyvät konferenssimatkat johtivat kansainväliseen kiinnostukseen Sjögrenin oireyhtymään. Termin "keratoconjunctivitis sicca" keksi Sjögren itse ja se alkoi kirjallisuudessa tunnistaa Sjögrenin oireyhtymäksi, vaikka sillä voi nyt olla yleisempi käyttö.
Tutkimus

Monitekijöiden autoimmuunisairauksien, kuten SS: n, tutkimus keskittyy häiriöön liittyvän tiedon laajentamiseen, diagnostisten työkalujen parantamiseen ja keinojen löytämiseen häiriön ehkäisemiseksi, hallitsemiseksi ja parantamiseksi. Britannia Ensisijainen Sjögrenin syndrooma rekisterin, kudoksen Biopankin otettujen näytteiden tutkimuksen tukemana Medical Research Council, UK , perustettiin vuonna 2010. Se tukee kliinisiä kokeita ja geneettiset tutkimukset Sjögrenin syndrooma on avoinna niille, jotka haluavat osallistua tutkimuksiin ja tautia tutkiville tutkijoille.
Kuten muutkin autoimmuunisairaudet, ihmisen leukosyyttiantigeeni vaikuttaa suuresti alttiuteen Sjögrenin oireyhtymälle. DQA1*05: 01, DQB1*02: 01 ja DRB1*03: 01 alleelit tunnistettiin riskitekijöiksi , kun taas DQA1*02: 01, DQA1*03: 01 ja DQB1*05: 01 alleelien havaittiin olevan suojaavia tekijöitä taudin vuoksi. Myös alleelien ja tietyn rodun välinen suhde selvitettiin. HLA-DQ2 ja HLA-B8 esiintyvät yleensä valkoihoisilla potilailla, kun taas HLA-DR5 liittyy kreikkalaisiin ja israelilaisiin potilaisiin. Tulevaisuudessa voidaan suorittaa useita genomin laajuisia assosiaatiotutkimuksia keskeisten riskivaihtoehtojen tunnistamiseksi.
Sjögrenin oireyhtymään liittyviä viruksia ovat ihmisen T-lymfotrooppinen virus tyyppi 1 ( HTLV-1 ), Epstein-Barr-virus (EBV), ihmisen immuunikatovirus (HIV), hepatiitti delta-virus (HDV) ja hepatiitti C -virus (HCV) .
Jotkut tutkimukset ovat osoittaneet, että A- ja D -vitamiinin puute liittyvät sairauteen. D -vitamiinin puutteen havaittiin liittyvän neurologisiin ilmenemismuotoihin ja lymfooman esiintymiseen potilaiden keskuudessa, mutta A -vitamiinipitoisuudet liittyivät käänteisesti sairauden ekstraglandulaarisiin ilmenemismuotoihin.
Sylki on Sjögrenin oireyhtymän mahdollinen diagnostinen työkalu, koska sylkiosa muuttuu taudin puhkeamisen jälkeen. Diagnoosi voi olla helpompaa uudella pienikokoisella tekniikalla, jota kutsutaan laboratorioksi sirulla .
Mitä tulee lääkkeisiin , vuonna 2007 tutkittiin useita monoklonaalisia vasta-aineita . Lupaavimmat näyttivät olevan anti- CD20- rituksimabi ja anti- CD22- epratatsumabi , kun taas anti- TNF-α ja IFN-α vaikuttivat vähemmän tehokkailta.
Vuonna 2014 Sjögrenin oireyhtymäsäätiö ilmoitti viiden vuoden tavoitteesta puolittaa taudin keskimääräinen diagnosointiaika.
Merkittäviä tapauksia
- Shannon Boxxilla ( Yhdysvaltain olympiajalkapallon pelaaja) on sekä Sjögrenin oireyhtymä että lupus .
- Carrie Ann Inaba (laulaja-näyttelijä) on kansallisen tietoisuuden suurlähettiläs ja Sjögrenin oireyhtymäsäätiön tiedottaja.
- Venus Williamsilla (maailmanmestari tennispelaaja ) on diagnosoitu Sjögrenin oireyhtymä ja hän sanoi kamppaillut väsymyksen kanssa vuosia.
- Stephen McPhail (Irlannin, Leedsin ja Cardiff Cityn ammattilaisjalkapalloilija) diagnosoitiin lymfooma ja Sjögrenin oireyhtymä 29 -vuotiaana.
Viitteet
- Osa tämän artikkelin alkuperäisestä tekstistä on saatu NIH: n julkisesta resurssista
Ulkoiset linkit
- Sjögrenin oireyhtymä NHS Choicesissa
- Sjögrenin oireyhtymä - Yhdysvaltain kansallinen niveltulehduslaitos sekä tuki- ja liikuntaelimistön ja ihosairaudet
- Yhdysvaltain Sjögrenin säätiö
- Hinta, EJ; Rauz, S; Tappuni, AR; Sutcliffe, N; Hackett, KL; Barone, F; Granata, G; Ng, WF; Fisher, BA; Bombardieri, M; Astorri, E; Empson, B; Larkin, G; Crampton, B; Bowman, SJ; British Society for Rheumatology Standards, Guideline and Audit Working, ryhmä. (1. lokakuuta 2017). "British Society for Reumatology -ohje aikuisten Sjögrenin oireyhtymän hoitoon" . Reumatologia . 56 (10): e24 – e48. doi : 10.1093/reumatology/kex166 . PMID 28957550 .
| Luokitus | |
|---|---|
| Ulkoiset resurssit |


