Maksatoksisuus - Hepatotoxicity
| Maksatoksisuus | |
|---|---|
| Muut nimet | Lääkkeen aiheuttama maksavaurio (DILI), toksinen maksasairaus, toksiinin aiheuttama maksasairaus, lääkkeen aiheuttama maksasairaus, lääkkeen aiheuttama maksavaurio, hepatogeeninen myrkytys |
 | |
| Lääkkeen aiheuttama hepatiitti ja granulomaatti . Muut syyt suljettiin pois laajoilla tutkimuksilla. Maksan biopsia . H&E tahra . | |
| Erikoisuus | Gastroenterologia |
| Komplikaatiot | Kirroosi , maksan vajaatoiminta |
| Alempia termejä |
|---|
| Myrkyllinen hepatiitti Toksiinin aiheuttama hepatiitti |
Maksatoksisuus ( maksatoksisuudesta ) merkitsee kemiallisia maksavaurioita . Lääkkeen aiheuttama maksavaurio on akuutin ja kroonisen maksasairauden syy, joka johtuu erityisesti lääkkeistä.
Maksalla on keskeinen rooli kemikaalien muuttamisessa ja puhdistamisessa, ja se on altis näiden aineiden aiheuttamalle myrkyllisyydelle. Tietyt lääkeaineet (esim. Parasetamoli ) yliannoksina ja joskus jopa terapeuttisilla alueilla (esim. Halotaani ) voivat vahingoittaa elintä. Muut kemialliset aineet, kuten laboratorioissa ja teollisuudessa käytetyt aineet, luonnonkemikaalit (esim. Mikrosyktiinit ) ja kasviperäiset lääkkeet (kaksi merkittävää esimerkkiä ovat kava , mekanismi tuntematon ja raunioyrtti pyrrolitsidiinialkaloidipitoisuutensa kautta) voivat myös aiheuttaa hepatotoksisuutta. Maksavaurioita aiheuttavia kemikaaleja kutsutaan hepatotoksiineiksi .
Yli 900 lääkettä on liittynyt aiheuttamaan maksavaurioita (katso LiverTox, ulkoinen linkki alla), ja se on yleisin syy lääkkeen vetämiseen markkinoilta. Maksatoksisuus ja lääkkeiden aiheuttama maksavaurio aiheuttavat myös huomattavan määrän yhdisteen epäonnistumisia, mikä korostaa tarvetta myrkyllisyyden ennustemalleille (esim. DTI) ja lääkeseulontamäärityksille, kuten kantasoluista peräisin oleville hepatosyyttimaisille soluille, jotka pystyvät havaitsemaan myrkyllisyys lääkkeen kehitysprosessin alkuvaiheessa. Kemikaalit aiheuttavat usein subkliinisen maksavaurion, joka ilmenee vain epänormaaleina maksaentsyymikokeina .
Lääkkeen aiheuttama maksavaurio aiheuttaa 5% kaikista sairaalahoidoista ja 50% akuuteista maksan vajaatoiminnasta .
Syyt
Haittavaikutukset luokitellaan tyypin A (luontainen tai farmakologinen) tai tyypin B (yksilöllinen) tyypiksi. Tyypin A lääkereaktio aiheuttaa 80% kaikista toksisuuksista.
Lääkkeet tai toksiinit, joilla on farmakologinen (tyypin A) hepatotoksisuus, ovat niitä, joilla on ennustettavissa oleva annos-vaste-käyrä (korkeammat pitoisuudet aiheuttavat enemmän maksavaurioita) ja hyvin karakterisoituja toksisuusmekanismeja, kuten maksakudoksen vahingoittaminen suoraan tai aineenvaihduntaprosessin estäminen. Kuten parasetamolin yliannostuksen tapauksessa , tämäntyyppinen vahinko tapahtuu pian jonkin myrkyllisyysrajan saavuttamisen jälkeen. Hiilitetrakloridia käytetään yleisesti akuutin tyypin A maksavaurion aiheuttamiseen eläinmalleissa.
Idiosynkraattinen (tyyppi B) vamma ilmenee ilman varoitusta, kun aineet aiheuttavat arvaamattomille henkilöille ennustamatonta maksatoksisuutta, joka ei liity annokseen ja jolla on vaihteleva latenssiaika. Tämän tyyppisellä vammalla ei ole selkeää annos-vaste- eikä ajallista suhdetta, eikä useimmiten ole ennustavia malleja. Idiosynkraattinen hepatotoksisuus on johtanut useiden lääkkeiden poistamiseen markkinoilta jopa tiukan kliinisen testauksen jälkeen osana FDA: n hyväksymisprosessia; Troglitatsoni (Rezulin) ja trovafloksasiini (Trovan) ovat kaksi erinomaista esimerkkiä markkinoilta vedetyistä omituisista hepatotoksiineista.
Yrtti -kava on aiheuttanut useita tapauksia, joissa on ominaista maksavaurioita, jotka vaihtelevat kaikkialla oireettomista kuolemaan.
Sienilääkityksen ketokonatsolin suun kautta antamiseen on liittynyt maksatoksisuutta, mukaan lukien jotkut kuolemantapaukset; tällaiset vaikutukset näyttävät kuitenkin rajoittuvan annoksiin, jotka on otettu yli 7 päivän ajan.
Parasetamoli
Parasetamoli, joka tunnetaan myös nimellä asetaminofeeni ja jonka tuotenimet ovat Tylenol ja Panadol, on yleensä hyvin siedetty määrätyllä annoksella, mutta yliannostus on yleisin syy lääkkeiden aiheuttamaan maksasairauteen ja akuuttiin maksan vajaatoimintaan maailmanlaajuisesti. Maksavaurioita ei johdu itse lääkeaine, vaan toksisen metaboliitin ( N -asetyyli- p -bentsokinoni-imiiniä (NAPQI)), jota tuottaa sytokromi P-450-entsyymien maksassa. Normaalioloissa tämä metaboliitti detoksikoidaan konjugoimalla glutationin kanssa vaiheen 2 reaktiossa. Yliannostuksessa syntyy suuri määrä NAPQI: tä, joka hukuttaa vieroitusprosessin ja johtaa maksasoluvaurioon. Typpioksidilla on myös rooli toksisuuden indusoimisessa. Maksavaurion riskiin vaikuttavat useat tekijät, mukaan lukien nautittu annos, samanaikainen alkoholin tai muiden lääkkeiden nauttiminen, nauttimisen ja vastalääkkeen välinen aika jne. kroonisissa alkoholisteissa. Veren tason mittaaminen on tärkeää ennusteen arvioinnissa, korkeampi taso ennustaa huonompaa ennustetta. Anto Asetyylikysteiini , prekursori glutationi, voi rajoittaa vakavuus maksavaurion sieppaamalla toksisia NAPQI. Ne, joille kehittyy akuutti maksan vajaatoiminta, voivat silti toipua spontaanisti, mutta saattavat vaatia elinsiirtoa, jos huonoja ennusteita , kuten enkefalopatiaa tai koagulopatiaa, on läsnä (katso King's College Criteria ).
Ei-steroidiset tulehduskipulääkkeet
Vaikka yksittäiset kipulääkkeet aiheuttavat harvoin maksavaurioita niiden laajan käytön vuoksi, tulehduskipulääkkeet ovat nousseet suureksi ryhmäksi lääkkeitä, joilla on maksatoksisuutta. Sekä annoksesta riippuvaisia että omituisia reaktioita on dokumentoitu. Aspiriini ja fenyylibutatsoni liittyvät luontaiseen maksatoksisuuteen; Ibuprofeenin, sulindaakin, fenyylibutatsonin, piroksikaamin, diklofenaakin ja indometasiinin kanssa on yhdistetty omituista reaktiota.
Glukokortikoidit
Glukokortikoidit on nimetty siten, että ne vaikuttavat hiilihydraattimekanismiin. Ne edistävät glykogeenin varastointia maksassa. Suurentunut maksa on harvinainen sivuvaikutus pitkäaikaiseen steroidien käyttöön lapsilla. Pitkäaikaisen käytön klassinen vaikutus sekä aikuisilla että lapsilla on steatoosi .
Isoniatsidi
Isoniatsidi (INH) on yksi yleisimmin käytetyistä tuberkuloosilääkkeistä; siihen liittyy lievä maksaentsyymien kohoaminen jopa 20%: lla potilaista ja vaikea maksatoksisuus 1-2%: lla potilaista.
Muut hydratsiinijohdannaiset
On myös tapauksia, joissa muita hydratsiinin johdannainen lääkkeiden, kuten MAO: n estäjien masennuslääke iproniatsidin , liittyy maksavaurioita. Feneltsiiniin on liittynyt epänormaaleja maksakokeita. Antibiooteista voi kehittyä toksisia vaikutuksia.
Luonnonmukaiset tuotteet
Esimerkkejä ovat alfa-amanitiinia sisältävät sienet, kava ja aflatoksiinia tuottavat muotit. Pyrrolitsidiinialkaloidit , joita esiintyy joissakin kasveissa, voivat olla myrkyllisiä. Vihreä teeuute on kasvava syy maksan vajaatoimintaan, koska se on sisällytetty useampiin tuotteisiin.
Vaihtoehtoisia korjaustoimenpiteitä
Esimerkkejä ovat: Ackee -hedelmät , Bajiaolian , Kamferi , Copaltra , Sykasiini , Garcinia , Kava -lehdet , pyrrolitsidiinialkaloidit , Hevoskastanjanlehdet , Valerian , Comfrey . Kiinalaiset kasviperäiset lääkkeet: Jin Bu Huan , Ma-huang , Shou Wu Pian , Bai Xian Pi .
Teollinen myrkky
Esimerkkejä ovat arseeni , hiilitetrakloridi ja vinyylikloridi .
Mekanismi
Lääkkeen aiheuttamaan maksatoksisuuteen vaikuttavat tekijät |
|---|
|
Lääkkeet poistetaan edelleen markkinoilta maksatoksisuuden myöhäisen havaitsemisen vuoksi. Ainutlaatuisen aineenvaihduntansa ja läheisen suhteen ruoansulatuskanavan vuoksi maksa on altis lääkkeiden ja muiden aineiden aiheuttamille vammoille. 75% maksaan tulevasta verestä tulee suoraan ruoansulatuskanavan elimistä ja pernasta portaalin laskimoiden kautta, jotka tuovat lääkkeitä ja ksenobiootteja lähes laimentamattomassa muodossa. Useat mekanismit ovat vastuussa joko maksavaurion aiheuttamisesta tai vaurioitumisprosessin pahenemisesta.
Monet kemikaalit vahingoittavat mitokondrioita , solunsisäistä organellia, joka tuottaa energiaa. Sen toimintahäiriö vapauttaa liikaa hapettimia, jotka puolestaan vahingoittavat maksasoluja. Joidenkin entsyymien aktivointi sytokromi P-450 -järjestelmässä, kuten CYP2E1, johtaa myös oksidatiiviseen stressiin. Vahinkoa maksasolujen ja sappiteiden solujen johtaa kertymistä sappihapon sisällä maksassa . Tämä edistää maksavaurioita. Ei- parenkymaaliset solut, kuten Kupfferin solut , rasvan varastoinnin liposyyttien , ja leukosyytit (ts neutrofiilien ja monosyyttien ) on myös rooli mekanismi.
Lääkkeiden aineenvaihdunta maksassa
Ihmiskeho tunnistaa lähes kaikki lääkkeet vieraiksi aineiksi (esim. Ksenobiootit ) ja altistaa ne erilaisille kemiallisille prosesseille (eli aineenvaihdunnalle ), jotta ne soveltuisivat eliminoitumiseen. Tämä sisältää kemiallisia muunnoksia (a) vähentää rasvaliukoisuutta ja (b) muuttaa biologista aktiivisuutta. Vaikka melkein kaikilla kehon kudoksilla on jonkin verran kykyä metaboloida kemikaaleja, sileä endoplasminen verkkokalvo maksassa on tärkein "aineenvaihdunnan selvityskeskus" sekä endogeenisille kemikaaleille (esim. Kolesteroli , steroidihormonit, rasvahapot , proteiinit ) että ulkoisille aineille (esim. , huumeet, alkoholi). Maksan keskeinen rooli kemikaalien puhdistamisessa ja muuntamisessa tekee siitä alttiita lääkkeiden aiheuttamille vammoille.
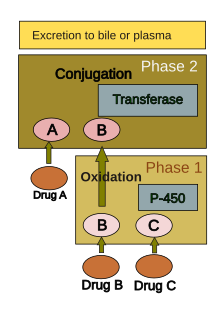
Lääkeaineenvaihdunta jaetaan yleensä kahteen vaiheeseen: vaihe 1 ja vaihe 2 . Vaiheen 1 reaktion uskotaan valmistavan lääkettä vaiheeseen 2. Kuitenkin monet yhdisteet voivat metaboloitua suoraan vaiheen 2 avulla. Vaiheen 1 reaktio sisältää hapettumisen , pelkistämisen , hydrolyysin , nesteytyksen ja monia muita harvinaisia kemiallisia reaktioita. Nämä prosessit pyrkivät lisäämään lääkkeen vesiliukoisuutta ja voivat tuottaa metaboliitteja, jotka ovat kemiallisesti aktiivisempia ja mahdollisesti myrkyllisiä. Suurin osa vaiheen 2 reaktioista tapahtuu sytosolissa ja niihin liittyy konjugaatio endogeenisten yhdisteiden kanssa transferaasientsyymien kautta . Kemiallisesti aktiiviset faasin 1 tuotteet tehdään suhteellisen inertteiksi ja sopiviksi eliminoimiseksi tässä vaiheessa.
Ryhmä entsyymejä, jotka sijaitsevat endoplasmisessa verkkokalvossa, tunnetaan sytokromi P-450: nä , on tärkein maksassa metaboloivien entsyymien perhe. Sytokromi P-450 on päätteen oksidaasi komponenttina elektroninsiirtoketju . Se ei ole yksittäinen entsyymi, vaan koostuu läheisesti toisiinsa liittyvästä 50 isoformin perheestä ; kuusi niistä metaboloi 90% lääkkeistä. Yksittäisiä P-450-geenituotteita on valtavasti erilaisia, ja tämän heterogeenisyyden ansiosta maksa voi suorittaa hapetuksen monille kemikaaleille (mukaan lukien lähes kaikki lääkkeet) vaiheessa 1. P-450-järjestelmän kolmella tärkeällä ominaisuudella on rooli lääkkeen aiheuttama toksisuus:
- 1. Geneettinen monimuotoisuus:
Jokainen P-450-proteiini on ainutlaatuinen ja vastaa (jossain määrin) lääkkeiden metabolian vaihtelusta yksilöiden välillä. Geneettiset vaihtelut ( polymorfismi ) P-450-aineenvaihdunnassa on otettava huomioon, kun potilailla on epätavallinen herkkyys tai vastustuskyky lääkkeen vaikutuksille tavanomaisilla annoksilla. Tällainen polymorfismi on myös vastuussa vaihtelevasta lääkevasteesta potilailla, joilla on eri etninen tausta.
- 2. Muutos entsyymiaktiivisuudessa:
| Voimakkaat induktorit | Voimakkaat estäjät | Alustat |
|---|---|---|
|
Rifampisiinin , karbamatsepiini , fenobarbitaali , fenytoiini , ( mäkikuisma ), |
Amiodaroni , simetidiini , siprofloksasiini , flukonatsoli , fluoksetiini , erytromysiini , isoniatsidi , diltiatseemi |
Kofeiini , klotsapiini , omepratsoli , losartaani , teofylliini |
Monet aineet voivat vaikuttaa P-450-entsyymimekanismiin. Lääkkeet ovat vuorovaikutuksessa entsyymiperheen kanssa monin tavoin. Lääkkeitä, jotka muuttavat sytokromi P-450 -entsyymiä, kutsutaan joko estäjiksi tai indusoijiksi. Entsyymin estäjät estävät yhden tai useamman P-450-entsyymin metabolisen aktiivisuuden. Tämä vaikutus ilmenee yleensä välittömästi. Toisaalta induktorit lisäävät P-450-aktiivisuutta lisäämällä sen synteesiä. Indusoivan lääkkeen puoliintumisajasta riippuen entsyymiaktiivisuuden lisääntyminen kestää yleensä jonkin aikaa.
- 3. Kilpailun esto:
Joillakin lääkkeillä voi olla sama P-450-spesifisyys ja ne estävät siten kilpailevasti niiden biologisen muutoksen. Tämä voi johtaa entsyymin metaboloimien lääkkeiden kertymiseen. Tämäntyyppinen lääkkeiden vuorovaikutus voi myös vähentää myrkyllisen substraatin muodostumisnopeutta.
Loukkaantumismallit
| Vamman tyyppi: | Hepatosellulaarinen | Kolestaattinen | Sekoitettu |
|---|---|---|---|
| ALT | ≥ Kaksinkertainen nousu | Normaali | ≥ Kaksinkertainen nousu |
| ALP | Normaali | ≥ Kaksinkertainen nousu | ≥ Kaksinkertainen nousu |
| ALT: ALP -suhde | Korkea, ≥5 | Alhainen, ≤2 | 2–5 |
| Esimerkkejä |
Asetaminofeeni Allopurinoli Amiodarone HAART NSAID |
Anabolinen steroidi Klooripromatsiini Klopidogreeli Erytromysiini Hormonaalinen ehkäisy |
Amitriptyliini , Enalapril Carbamazepine Sulfonamidia Fenytoiini |
Kemikaalit aiheuttavat laajan valikoiman kliinisiä ja patologisia maksavaurioita. Biokemiallisia markkereita (esim. Alaniinitransferaasi , alkalinen fosfataasi ja bilirubiini ) käytetään usein osoittamaan maksavaurioita. Maksavaurio määritellään joko (a) ALAT -arvon nousuksi yli kolme kertaa normaalin ylärajan (ULN) ylärajaan, (b) ALP -tasoon yli kaksi kertaa ULN -arvoon tai (c) kokonaisbilirubiinipitoisuuteen yli kaksi kertaa ULN -arvoon verrattuna kohonnut ALT tai ALP. Maksavaurioita luonnehditaan edelleen hepatosellulaarisiin (pääasiassa alaniinitransferaasiarvojen nousu) ja kolestaattisiin (alkalisen fosfataasin nousu) tyyppeihin. Ne eivät kuitenkaan sulje toisiaan pois, ja loukkaantumisia esiintyy usein.
Lääkkeen aiheuttamasta vauriosta johtuvan maksavaurion erityisiä histo-patologisia kuvioita käsitellään alla.
Alueellinen nekroosi
Tämä on yleisin lääkkeiden aiheuttama maksan solujen nekroosia , jossa vamma on pitkälti rajoittuu tiettyyn vyöhykkeeseen maksan lobule . Se voi ilmetä erittäin korkeana ALAT -tasona ja vakavana maksan toimintahäiriönä, joka johtaa akuuttiin maksan vajaatoimintaan .
- Syitä ovat:
- Parasetamoli , hiilitetrakloridi
Hepatiitti
Tässä mallissa hepatosellulaarinen nekroosi liittyy tulehdussolujen tunkeutumiseen. Huumeiden aiheuttamaa hepatiittia voi olla kolmenlaisia. (A) virushepatiitti on yleisin, jos histologiset piirteet ovat samanlaisia kuin akuutti virushepatiitti. (B) polttopisteessä tai ei-spesifisessä hepatiitissa solunekroosin hajanaiset kohdat voivat liittyä lymfosyyttiseen soluttautumiseen. (C) krooninen hepatiitti on kliinisesti, serologisesti ja histologisesti hyvin samankaltainen kuin autoimmuunihepatiitti .
- Syyt:
- a) Virushepatiitti: Halotaani , isoniatsidi , fenytoiini
- (b) Fokusalinen hepatiitti: Aspiriini
- c) Krooninen hepatiitti: metyylidopa , diklofenaakki
Kolestaasi
Maksavaurio johtaa sappivirtauksen heikkenemiseen ja tapauksia hallitsee kutina ja keltaisuus. Histologiassa voi esiintyä tulehdusta (kolestaattinen hepatiitti) tai se voi olla lievää (ilman parenkymaalista tulehdusta). Harvinaisissa tapauksissa se voi tuottaa primaarisen sappikirroosin kaltaisia piirteitä johtuen pienten sappitiehyiden asteittaisesta tuhoutumisesta ( häviävän kanavan oireyhtymä ).
- Syyt:
- (a) Bland: Suun kautta otettavat ehkäisypillerit , anabolinen steroidi , androgeenit
- b) Tulehdukselliset: Allopurinoli , co-amoxiclav , karbamatsepiini
- (c) Duktal: klooripromatsiini , flukloksasilliini
Steatoosi
Maksatoksisuus voi ilmetä triglyseridien kerääntymisenä, mikä johtaa joko pieneen pisaraan (mikrovesikulaarinen) tai suureen pisaraan (makrovesikulaariseen) maksaan. On olemassa erillinen steatoosityyppi, jolla fosfolipidien kertyminen johtaa samanlaiseen malliin kuin sairaudet, joilla on perinnöllisiä fosfolipidien aineenvaihduntahäiriöitä (esim. Tay – Sachsin tauti )
- Syyt:
- a) Mikrovesikulaarinen: Aspiriini ( Reyen oireyhtymä ), ketoprofeeni , tetrasykliini (erityisesti jos se on vanhentunut)
- (b) Macrovesicular: Parasetamoli , metotreksaatti
- (c) Fosfolipidoosi: Amiodaroni , parenteraalinen kokonaisravitsemus
- d) Antiviraalinen : nukleosidianalogit
- (e) Kortikosteroidi
- (f) Hormonaalinen: tamoksifeeni
Granulooma
Lääkkeen aiheuttamat maksan granuloomat liittyvät yleensä muiden kudosten granuloomiin, ja potilailla on tyypillisesti systeeminen vaskuliitti ja yliherkkyys. Yli 50 huumetta on osallisena.
- Syyt:
- Allopurinoli , fenytoiini , isoniatsidi , kiniini , penisilliini , kinidiini
Verisuonivauriot
Nämä johtuvat verisuonten endoteelin vammasta.
- Syyt:
- Venoocclusiivinen sairaus : kemoterapia -aineet, pensastee
- Peliosis hepatis : Anaboliset steroidit
- Maksan laskimotukos : Suun kautta otettavat ehkäisyvalmisteet
Kasvain
Kasvaimia on kuvattu pitkäaikaisessa altistumisessa joillekin lääkkeille tai toksiineille. Yleensä raportoidaan maksasolusyöpä, angiosarkooma ja maksan adenoomat.
Diagnoosi
Tämä on edelleen haaste kliinisessä käytännössä, koska luotettavia markkereita ei ole. Monet muut olosuhteet johtavat samanlaisiin kliinisiin ja patologisiin kuviin. Hepatotoksisuuden diagnosoimiseksi on löydettävä syy -yhteys toksiinin tai lääkkeen käytön ja sitä seuraavan maksavaurion välillä, mutta se voi olla vaikeaa, varsinkin jos epäillään omituista reaktiota. Useiden lääkkeiden samanaikainen käyttö voi lisätä monimutkaisuutta. Kuten asetaminofeenin toksisuuden kohdalla, vakiintunut, annoksesta riippuvainen farmakologinen hepatotoksisuus on helpompi havaita. Useita kliinisiä asteikkoja, kuten CIOMS /RUCAM -asteikko ja Maria- ja Victorino -kriteerit, on ehdotettu syy -yhteyden määrittämiseksi rikkovan lääkkeen ja maksavaurion välillä. CIOMS/RUCAM -asteikko sisältää pisteytysjärjestelmän, joka luokittelee epäilyn " varmaksi tai erittäin todennäköiseksi" (pisteet> 8), "todennäköiseksi" (pisteet 6-8), "mahdolliseksi" (pisteet 3-5), "epätodennäköiseksi" (pisteet) 1–2) ja "poissuljettu" (pisteet ≤ 0). Kliinisessä käytännössä lääkärit painottavat enemmän samankaltaisuuden olemassaoloa tai puuttumista potilaan biokemiallisen profiilin ja epäillyn myrkyllisyyden tunnetun biokemiallisen profiilin välillä (esim. Kolestaattinen vaurio amoksisilliini-klauvonihapossa ).
Hoito
Useimmissa tapauksissa maksan toiminta palautuu normaaliksi, jos rikkova lääke lopetetaan aikaisin. Lisäksi potilas voi tarvita tukihoitoa. In asetaminofeeni myrkyllisyys , kuitenkin, ensimmäinen loukkaus voi olla kohtalokas. Fulminantti maksan vajaatoiminta lääkkeen aiheuttamasta maksatoksisuudesta saattaa edellyttää maksansiirtoa. Aiemmin oli käytetty allergisia piirteitä sisältäviä glukokortikoideja ja kolestaattisissa tapauksissa ursodeoksikoolihappoa, mutta niiden tehokkuutta ei ole vahvistettu.
Ennuste
Seerumin bilirubiinipitoisuuden nousu yli 2 kertaa ULN ja siihen liittyvä transaminaasiarvojen nousu on pahaenteinen merkki. Tämä viittaa vakavaan maksatoksisuuteen ja johtaa todennäköisesti kuolleisuuteen 10–15%: lla potilaista, varsinkin jos rikkovaa lääkettä ei lopeteta ( Hy: n laki ). Tämä johtuu siitä, että se vaatii maksavaurioita merkittävästi bilirubiinin erittymisen heikentämiseksi, joten vähäinen heikentyminen (jos sappitukos tai Gilbertin oireyhtymä puuttuu ) ei aiheuttaisi keltaisuutta. Muita huonoja lopputuloksen ennustajia ovat vanhuus, naisten sukupuoli, korkea AST .
Lääkkeet poistettu
Seuraavat terapeuttiset lääkkeet poistettiin markkinoilta pääasiassa maksatoksisuuden vuoksi: troglitatsoni , bromfenaakki , trovafloksasiini , ebrotidiini , nimesulidi , nefatsodoni , ksimelagatraani ja pemoliini .
Katso myös
Huomautuksia
Viitteet
- Friedman, Scott E .; Grendell, James H .; McQuaid, Kenneth R. (2003). Nykyinen diagnoosi ja hoito gastroenterologiassa. New York: Lang Medical Books/McGraw-Hill. s. 664–679. ISBN 978-0-8385-1551-8 .
- Dixit, Vaibhav A. (2019). "Yksinkertainen malli monimutkaisen lääkemyrkyllisyysongelman ratkaisemiseksi". Toksikologia, tutkimus. 8 (2): 157171. doi: 10.1039/C8TX00261D. PMC 6417485. PMID 30997019 .
- Ostapowicz G, Fontana RJ, Schiødt FV, et ai. (2002). "Akuutin maksan vajaatoiminnan prospektiivisen tutkimuksen tulokset 17: ssä Yhdysvaltain kolmannen asteen hoitokeskuksessa". Ann. Harjoittelija. Med. 137 (12) .947–54. doi: 10.7326/0003-4819-1371220021217000007. PMID 12484709 . S2CID 11390513.
- Pirmohamed M, Breckenridge AM, Kitteringham NR, Park BK (1998). "Huumeiden haittavaikutukset". BMJ. 316 (7140): 12958. doi: 10.1136/bmj.316.7140.1295. PMC 1113033. PMID 9554902 .
- Manov I, Motanis H, Frumin I, Iancu TC (2006). "Tulehduskipulääkkeiden ja kipulääkkeiden maksatoksisuus: ultrastruktuuriset näkökohdat". Acta Pharmacol. Synti. 27 (3): 259–72. doi: 10.1111/j.1745-7254.2006.00278.x. PMID 16490160 . S2CID 26874901.
- Alpers DH, Sabesin SM (1982). Schiff L; Schiff ER (toim.). Maksan sairaudet. Philadelphia: JB Lippincott. s. 813–45
- Chalasani, Naga P .; Hayashi, Paul H .; Bonkovsky, Herbert L .; Navarro, Victor J .; Lee, William M .; Fontana, Robert J .; Harjoitusparametrikomitea American College of Gastroenterology (2014). "ACG Clinical Guideline: The Diagnosis and Management of Idiosyncratic Drug-Induced Maksavaurio". American Journal of Gastroenterology. 109 (7): 950966. doi: 10.1038/ajg.2014.131. PMID 24935270 . S2CID 2417493
- Patel T, Roberts LR, Jones BA, Gores GJ (1998). "Apoptoosin dysregulaatio maksasairauden mekanismina: yleiskatsaus". Semin. Maksa Dis. 18 (2): 105–14. doi: 10.1055/s-2007-1007147. PMID 9606808
- Mumoli N, Cei M, Cosimi A (2006). "Huumeisiin liittyvä maksatoksisuus". N. Engl. J. Med. 354 (20): 21913, kirjoittaja, vastaus 21913. doi: 10.1056/NEJMc060733. PMID 16710915
- Bénichou C (1990). "Huumeiden aiheuttamien maksasairauksien kriteerit. Raportti kansainvälisestä konsensuskokouksesta". J. Hepatol. 11 (2): 272–6. doi: 10.1016/0168-8278 (90) 90124-A. PMID 2254635
- Blazka ME, Wilmer JL, Holladay SD, Wilson RE, Luster MI. (1995) Tulehdusta edistävien sytokiinien rooli asetaminofeenin hepatotoksisuudessa. Toxicol Appl Pharmacol 1995; 133: 43-52
- Yadav V, Rai R, Yadav A, Pahuja M, Solanki S, et ai. (2012) Callicarpa macrophylla Vahlin antibakteerisen aktiivisuuden arviointi. varsiuutteet
- Siddiqui H (1993) Kasviperäisten lääkkeiden turvallisuus-yleiskatsaus. Huumeiden uutisnäkymät
- Kumar A, Rohal A, Chakraborty S, Tiwari R, Latheef SK, et ai. (2013) Ocimum sanctum (Tulsi): ihmeyrtti ja siunaus lääketieteelliseen katsaukseen. Int J Agron Plant Prod 4: 589
- Moher D, Shamseer L, Clarke M, Ghersi D, Liberati A, et ai. (2015) Järjestelmän tarkastelu- ja meta-analyysiprotokollien (PRISMA-P) 2015 lausunnon suositellut raportointikohdat. Syst Rev 4: 1
- Singh N, Verma P, Pandey BR, Bhalla M (2012) Ocimum sanctumin terapeuttinen potentiaali syövän ja säteilyaltistuksen ehkäisemisessä ja hoidossa: Yleiskatsaus. Int J Pharmacist Sci Drug Res 4: 97-104.
- Mondal S, Mirdha BR, Mahapatra SC (2009) Tulsin pyhyyden tiede (Ocimum sanctum Linn.). Intian J Physiol Pharmacol 53: 291-306.
- Devra D, Mathur KC, Agrawal RP, Bhadu I, Goyal S, et ai. (2012) Tulsin (Ocimum sanctum Linn.) Vaikutus metabolisen oireyhtymän kliinisiin ja biokemiallisiin parametreihin. J Nat Remedies 12: 63-67
- Ahmad I, Beg AZ (2001) Antimikrobiset ja kasvikemialliset tutkimukset 45 intialaisella lääkekasvilla monilääkeresistenttejä ihmisen patogeenejä vastaan. Ethnopharmacol 74: 113-123.
- Amadi J, Salami S, Eze C (2010) Afrikkalaisen basilikan (Ocimum gratissimum L.) uutteiden sienilääkkeet ja kasvikemiallinen seulonta. Agr Biol J Pohjois-Amerikka 1: 163-166.
- Ponnusam Y, Louis T, Madhavachandran V, Kumar S, Thoprani N, et ai. (2015) Antiikin yrtin antioksidanttiaktiivisuus, pyhä basilika CCl4-indusoidussa maksavauriossa rotissa. Ayurveda 2: 34-38.
- Ravi V, Parida S, Desai A, Chandramukhi A, Devi MG, et ai. (1997) Seerumin ja aivo -selkäydinnesteen tuumorinekroositekijätasojen korrelaatio japanilaisen enkefaliittipotilaiden kliinisiin tuloksiin. J Med Virol 51: 132-136.
- Kumari P, Yadav P, Verma PR, Kumar, Arya, Kumar S, et ai. (2013) Katsaus intialaisten lääkekasvien haavan paranemisominaisuuksista. Ind J Fund Appl Life Sci 3: 220-232.
- Kumar A, Agarwal K, Maurya AK, Shanker K, Bushra U, et ai. (2015) Farmakologinen ja kasvikemiallinen arviointi Ocimum sanctum -juuriuutteista sen tulehdusta, kipua lievittävää ja kuumetta alentavaa toimintaa varten. Pharmacogn Mag 11: S217.
- Ranjana T, Tripathi V (2015) Tulsin (Ocimum sanctum Linn) terapeuttinen vaikutus yleisesti ja suun terveyteen. Ayurlog: National Journal of Research in Ayurveda Science 3: 1-12.
- Suanarunsawat T, Ayutthaya WDN, Thirawarapan S, Poungshompoo S (2014) Ocimum sanctum L. -lehden vesipitoisten uutteiden antioksidatiiviset, antihyperglykeemiset ja lipidejä alentavat vaikutukset diabeettisilla rotilla. Food Nutr Sci 5: 801-811.
- Talekar, YP, Das, B., Paul, T., Talekar, DY, Apte 1, KG ja Parab, PB (2012). Ocimum sanctum Linnin vesi- ja etanoliuutteen hepatoprotektiivisen potentiaalin arviointi. In Wistar Rats. Asian Journal of Pharmaceutical and Clinical Research, 5 (4), 141-145.
- Singh V, Kumar R. (2017). Bundelkhandin alueen Allium sativumin fytokemiallisen analyysin ja antioksidanttiaktiivisuuden tutkimus. International Journal of Life Sciences Scientific Research. 3 (6): 1451-1458.
- Raaman N. (2006). Fytokemialliset tekniikat. New India Publishing Agency, New Delhi, 19-24.
- Tiwari P, Kumar B, Kaur M, Kaur G, Kaur H. (2011). Fytokemiallinen seulonta ja uuttaminen: Katsaus. Internationale Pharmaceutica Sciencia. 1 (1): 98-106.
- Auwal MS, Saka S, Mairiga IA, Sanda KA, Shuaibu A ja Ibrahim A. (2014) Acacia nilotican (Thorn mimosa) vesipitoisten ja fraktioitujen pod -uutteiden alustava fytokemiallinen ja alkuaineanalyysi. Eläinlääketieteellinen tutkimusfoorumi. 5 (2): 95-100.
- Sadasivam S, Manickam A, Biokemialliset menetelmät. (2005). Edn 3, New Age International Limited, Publishers, New Delhi. 1-4.
- Basumatary AR. (2016). Joidenkin Tabernaemontana divaricata Linnin kasvien kuoriuutteista peräisin olevien yhdisteiden alustava fytokemiallinen seulonta. käyttää Bodo -yhteisö Kokrajharin piirissä, Assamissa, Intiassa. Soveltavan tieteellisen tutkimuksen arkisto. 8 (8): 47-52
- Silva GO, Abeysundara AT, Aponso MM. (2017). Uuttomenetelmät, laadulliset ja määrälliset tekniikat kasvikemikaalien seulomiseksi kasveista. American Journal of Essential Oils and Natural Products. 5 (2): 29-32
- Jagessar RC. (2017). Passiflora edulis ja Vicia faba L. (Fabaceae) -yhdisteen etanoli- ja vesiuutteen kasvikemiallinen seulonta ja kromatografinen profiili. Journal of Pharmacognosy and Phytochemistry. 6 (6): 1714-1721
- Gul R, Jan SU, Syed F, Sherani F, Nusrat Jahan. (2017). Preliminary Phytochemical Screening, kvantitatiivinen analyysi alkaloideista ja antioksidanttiaktiivisuus raakatuotteista, jotka on saatu Ephedra intermedia Indigenous to Balochistanista. The Scientific World Journal. 1-7
- Rubin, E., Hutter, F., Proper, H. (1963). Solujen lisääntyminen ja kuitujen muodostuminen kroonisessa hiilitetrakloridimyrkytyksessä. Morfologinen ja kemiallinen tutkimus. American Journal of Pathology 42, 715.
- Recnagal, R. (1983). Hiilitetrakloridin hepatotoksisuus, status quo ja tulevaisuudennäkymät. Farmakologisen tieteen suuntaukset 4, 129–131.
- Slater, TF (1978). Biokemialliset tutkimukset maksavauriosta. Academic Press, New York, s. 1–44.
- Reitman, S., Frankel, S. (1957). Kolorimetrinen menetelmä seerumin glutamaatti -oksaloasetaattitransaminaasien määrittämiseksi. American Journal of Clinical Pathology 28, 56–63.
- Malloy, HT, Evelyn, KA (1937). Bilirubiinin määrittäminen fotometrisellä kolorimetrillä. Journal of Biological Chemistry 119, 481–490.
- Kind, PRN, Kings, EJ (1976). Seerumin bilirubiinin määrittäminen. Lehti Clinical Pathology 7, 322–330.
- Brand-Williams, W .; Cuvelier, ME; Berset, C. (1995). Vapaiden radikaalien menetelmän käyttö antioksidanttisen aktiivisuuden arvioimiseksi. LWT - Food Sci. Technol. 28, 25–30.
- Shah, NA; Khan, MR; Ahmad, B .; Noureen, F .; Rashid, U .; Khan, RA (2013) Tutkimus Sida cordatan flavonoidikoostumuksesta ja vapaiden radikaalien mahdollisuudesta. BMC -täydennys. Vaihtoehto. Med, 13, 276.
- Zengin, G .; Aktumsek, A .; Guler, GO; Cakmak, YS; Yildiztugay, E. (2011). Centaurea urvillei DC: n metanoliuutteen antioksidanttiset ominaisuudet ja rasvahappokoostumus. Tilaa Hayekiana Wagenitz. Rec. Nat. Tuotteet, 5, 123–132.
- Mitsuda, H .; Yasumoto, K .; Iwami, K. (1966). Indoliyhdisteiden antioksidatiivinen vaikutus linolihapon autooksidaation aikana. Nippon Eiyo Shokuryo Gakkaishi, 19, 210–214
- Baccanari, D .; Phillips, A .; Smith, S .; Sinski, D .; Burchall, J. (1975-12-02). "Escherichia coli -dihydrofolaattireduktaasin puhdistus ja ominaisuudet" . Biokemia . 14 (24): 5267-5273. doi : 10.1021/bi00695a006 . ISSN 0006-2960 . PMID 46 .
Ulkoiset linkit
| Luokitus |
|---|
- LiverTox Yhdysvaltain kansallisessa lääketieteen kirjastossa