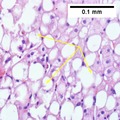
Alkoholiton rasvamaksa - Non-alcoholic fatty liver disease
| Alkoholiton rasvamaksa | |
|---|---|
| Muut nimet | NAFLD, aineenvaihduntaan (toimintahäiriöön) liittyvä rasvamaksa, MAFLD |
 | |
| Alkoholittoman rasvasairauden vaiheet, jotka etenevät terveestä steatoosiin (rasvan kertyminen), tulehdukseen, fibroosiin ja kirroosiin. | |
| Erikoisuus | Hepatologia |
| Oireet | Oireeton , maksan vajaatoiminta |
| Komplikaatiot | Kirroosi , maksasyöpä , maksan vajaatoiminta , sydän- ja verisuonitaudit |
| Kesto | Pitkäaikainen |
| Tyypit | Alkoholiton rasvamaksa (NAFL), alkoholiton steatohepatiitti (NASH) |
| Syyt | Geneettinen, ympäristöllinen |
| Riskitekijät | Lihavuus , metabolinen oireyhtymä , tyypin 2 diabetes , maksasairaus |
| Diagnostinen menetelmä | Maksan biopsia |
| Hoito | Laihtuminen (ruokavalio ja liikunta) |
| Ennuste | Riippuu tyypistä |
| Taajuus | 24% maailman väestöstä, 80% lihavista, 20% normaalipainoisista |
| Kuolemat | NASH: 2,6% kuoleman riski vuodessa |
Alkoholiton rasvahapposairaus ( NAFLD ), joka tunnetaan myös nimellä metabolinen (toimintahäiriö) liittyvä rasvamaksa ( MAFLD ), on liiallinen rasvan kertyminen maksaan ilman muuta selvää syytä, kuten alkoholin käyttöä . On olemassa kahta tyyppiä; alkoholiton rasvamaksa ( NAFL ) ja alkoholiton steatohepatiitti ( NASH ), joista jälkimmäinen sisältää myös maksatulehduksen . Alkoholiton rasvamaksa on vähemmän vaarallinen kuin NASH eikä yleensä etene NASH: ksi tai maksakirroosiksi . Kun NAFLD etenee NASH: ksi, se voi lopulta johtaa komplikaatioihin, kuten kirroosiin, maksasyöpään , maksan vajaatoimintaan tai sydän- ja verisuonitauteihin .
Lihavuus ja tyypin 2 diabetes ovat NAFLD: n vahvoja riskitekijöitä. Muita riskejä ovat ylipaino , metabolinen oireyhtymä (määritelty vähintään kolmeksi viidestä seuraavasta sairaudesta: vatsalihavuus, korkea verenpaine , korkea verensokeri , korkea seerumin triglyseridipitoisuus ja alhainen seerumin HDL -kolesteroli ), ruokavalio, jossa on paljon fruktoosia ja vanhempi ikä. NAFLD ja alkoholipitoinen maksasairaus ovat rasvaisen maksasairauden tyyppejä . Maksanäytteen ottaminen muiden mahdollisten rasvamaksan syiden poissulkemisen jälkeen voi vahvistaa diagnoosin.
NAFLD: n hoito on laihtuminen ruokavalion muutoksilla ja liikunnalla. On alustavia todisteita pioglitatsonista ja E -vitamiinista ; bariatrinen kirurgia voi parantaa tai ratkaista vakavia tapauksia. Niillä, joilla on NASH, on 2,6% suurempi riski kuolla vuodessa.
NAFLD on maailman yleisin maksasairaus, ja sitä esiintyy noin 25 prosentilla maailman väestöstä. Se on myös hyvin yleistä kehittyneissä maissa, kuten Yhdysvalloissa, ja se vaikutti noin 75-100 miljoonaan amerikkalaiseen vuonna 2017. Yli 90% lihavista, 60% diabeetikoista ja jopa 20% normaalipainoisista kehittää sen. NAFLD on johtava syy krooniseen maksasairauteen ja toiseksi yleisin syy maksansiirtoon Yhdysvalloissa ja Euroopassa vuodesta 2017. NAFLD vaikuttaa noin 20–25 prosenttiin ihmisistä Euroopassa. Yhdysvalloissa arviot viittaavat siihen, että 30–40 prosentilla aikuisista on NAFLD ja noin 3–12 prosentilla aikuisista on NASH. Vuotuinen taloudellinen taakka oli Yhdysvalloissa noin 103 miljardia dollaria vuonna 2016.
Määritelmä
Epänormaali rasvan kertyminen maksaan, jos ei ole toissijaisia rasvakudoksen syitä, kuten merkittävä alkoholin käyttö , virushepatiitti tai lääkkeet, jotka voivat aiheuttaa rasvaa maksan, luonnehtii alkoholittomalle rasvasairaudelle (NAFLD). Termi NAFLD käsittää jatkuvan maksan poikkeavuuksien alkoholittomasta rasvamaksasta (NAFL, yksinkertainen steatoosi) alkoholittomaan steatohepatiittiin (NASH). Nämä sairaudet alkavat rasvan kertymisestä maksaan (maksan steatoosi ). Maksa voi pysyä rasvaisena häiritsemättä maksan toimintaa (NAFL), mutta eri mekanismeilla ja mahdollisilla maksan loukkauksilla se voi myös kehittyä alkoholittomaksi steatohepatiitiksi (NASH), tila, jossa steatoosi yhdistyy tulehdukseen ja joskus fibroosiin ( steatohepatiitti). NASH voi sitten johtaa komplikaatioihin, kuten kirroosiin ja maksasolusyöpään .
Uutta nimeä, metaboliseen toimintahäiriöön liittyvää rasvahapposairautta, ehdotettiin sen jälkeen, kun 70% asiantuntijapaneelista ilmaisi tukevansa tätä nimeä.
Merkit ja oireet
Ihmisillä, joilla on NAFLD, ei useinkaan ole havaittavia oireita , ja NAFLD havaitaan usein vain rutiininomaisten verikokeiden tai asiaan liittyvän vatsakuvantamisen tai maksan biopsian aikana . Joissakin tapauksissa NAFLD voi aiheuttaa maksan toimintahäiriöön liittyviä oireita, kuten väsymystä, huonovointisuutta ja tylsää oikean ylä-neljänneksen vatsavaivoja . Iholla voi esiintyä lievää keltaista värimuutosta , vaikka tämä on harvinaista. NASH voi heikentää vakavasti maksan toimintaa, mikä johtaa kirroosiin , maksan vajaatoimintaan ja maksasyöpään .
Muita sairauksia
NAFLD liittyy voimakkaasti tyypin 2 diabetekseen, insuliiniresistenssiin ja metaboliseen oireyhtymään (määritelty vähintään kolmeksi viidestä seuraavasta sairaudesta: vatsalihavuus, korkea verenpaine, korkea verensokeri, korkea seerumin triglyseridipitoisuus tai alhainen seerumi) -tiheyslipoproteiini). Siihen liittyy myös hormonaalisia häiriöitä ( panhypopituitarismi , kilpirauhasen vajaatoiminta , hypogonadismi , munasarjojen monirakkulatauti ), jatkuvasti kohonneita transaminaasiarvoja , ikääntymistä ja obstruktiivisen uniapnean aiheuttamaa hypoksiaa , ja osa näistä tiloista ennustaa sairauden etenemistä.
Suurin osa normaalipainoisista ihmisistä, joihin NAFLD ("laiha NAFLD") vaikuttaa, on heikentynyt insuliiniherkkyyttä, ovat istumattomia ja heillä on lisääntynyt sydän- ja verisuonitautiriski ja kohonneet maksan lipiditasot. Nämä ovat seurausta rasvan varastointikyvyn heikkenemisestä ja mitokondrioiden toiminnan heikkenemisestä rasvakudoksessa ja maksan de novo lipogeneesin lisääntymisestä . Äskettäinen järjestelmällinen katsaus on raportoinut vakavan COVID-19-infektion riskin lisääntymisestä NAFLD-potilailla; Kuolleisuudessa ei kuitenkaan havaittu eroa NAFLD-potilaiden ja muiden kuin NAFLD-potilaiden välillä.
Riskitekijät
Genetiikka
Kaksi kolmasosaa perheistä, joilla on ollut tyypin 2 diabetes, ilmoittaa useammasta kuin yhdestä NAFLD-perheenjäsenestä. Fibroosin riski on suurempi perheenjäsenille, joilla on diagnosoitu NASH. Aasian väestöt ovat alttiimpia metaboliselle oireyhtymälle ja NAFLD: lle kuin länsimaiset vastapuolensa. Espanjalaisilla henkilöillä on suurempi NAFLD -esiintyvyys kuin valkoisilla yksilöillä, kun taas alhaisin esiintyvyys on havaittu mustilla yksilöillä. NAFLD on kaksi kertaa yleisempi miehillä kuin naisilla, mikä saattaa selittyä miesten estrogeenipitoisuuden pienenemisellä.
Kahden geenin geneettiset vaihtelut liittyvät NAFLD: hen: ei-synonyymejä yhden nukleotidin polymorfismeja (SNP) PNPLA3: ssa ja TM6SF2: ssa . Molemmat korreloivat NAFLD: n läsnäolon ja vakavuuden kanssa, mutta niiden roolit diagnoosissa ovat edelleen epäselviä. Vaikka NAFLD: llä on geneettinen komponentti, American Association for the Study of Liver Diseases (AASLD) ei suosittele perheenjäsenten seulontaa, koska perinnöllisyydestä ei ole riittävästi vahvistusta, vaikka perinnöllisestä aggregaatiosta ja kaksoistutkimuksista on jonkin verran näyttöä .
Ruokavalio
Aasian ja Tyynenmeren alueen NAFLD-työryhmän (APWG) mukaan aliravitsemus on tärkeä tekijä NAFLD: ssä ja NASH: ssa, erityisesti vähärasvaisen NAFLD: n kohdalla. Ruokavalion koostumuksella ja määrällä, erityisesti omega-6-rasvahapolla ja fruktoosilla , on tärkeä rooli sairauden etenemisessä NAFL: stä NASH: ksi ja fibroosiksi. Koliinin puute voi johtaa NAFLD: n kehittymiseen.
Elämäntapa
Tavallinen kuorsaus voi olla NAFLD: n riskitekijä, vaikka yksilöiden riskitekijät on otettu huomioon. Vakavat kuorsaustapaukset johtavat hengitysteiden tukkeutumiseen tai hengitysvaikeuksiin nukkuessa, ja ne yleensä osoittavat obstruktiivisen uniapnean (OSAS), joka on paljon vakavampi hengitystila. Hengitysteiden tukkeutuminen tai kaventuminen, jopa tilapäisesti, voi aiheuttaa kehon alentuneen veren happipitoisuuden, ja nämä hypoksiaolosuhteet toistuvat niillä, joilla on obstruktiivinen uniapnea (OSAS). Jatkuva hypoksia voi aiheuttaa erilaisia muutoksia kehossa, kuten kudosten tulehdusta, lisääntynyttä insuliiniresistenssiä ja maksavaurioita. Prospektiivisessa kohorttitutkimuksessa todettiin, että tavanomaisen kuorsauksen ja NAFLD -kehityksen välinen yhteys on merkittävä, ja trendin havaittiin olevan näkyvin laihoilla yksilöillä.
Patofysiologia
NAFLD: n ensisijainen ominaisuus on lipidien kertyminen maksaan, suurelta osin triglyseridien muodossa . Kuitenkin mekanismit, joilla triglyseridit kerääntyvät, ja syyt, joiden vuoksi kertyminen voi johtaa maksan toimintahäiriöön, ovat monimutkaisia ja epätäydellisiä. NAFLD voi sisältää steatoosia ja erilaisia merkkejä maksavauriosta: joko lobulaarinen tai portaali -tulehdus (maksavaurion muoto) tai ilmapallon rappeuma . Vastaavasti, NASH voi sisältää histologiset ominaisuuksia, kuten portaali tulehdus, polymorphonuclear solujen infiltraatteja, Mallory elimet , apoptoottisten elinten, kirkas vakuoleja ytimet, microvesicular rasvamaksa , megamitochondria , ja perisinusoidaalinen fibroosi . NASH lisää hepatosyyttien kuolemaa apoptoosin tai nekroptoosin kautta lisääntyy NASH: ssa verrattuna yksinkertaiseen steatoosiin, ja tulehdus on NASH: n tunnusmerkki.
Eräs keskusteltu mekanismi ehdottaa, että maksan steatoosi etenee steatoosiksi tulehduksen kanssa jonkin muun vamman tai toisen osuman jälkeen . Oksidatiivinen stressi , hormonaalinen epätasapaino ja mitokondrioiden poikkeavuudet ovat mahdollisia syitä tähän "toisen osuman" ilmiöön. Toinen Nutrigenomics -malli, nimeltään usea osuma, laajentaa toista osumamallia , mikä viittaa siihen, että useiden sairauksien biomarkkerit ja tekijät, kuten geenit ja ravitsemus, vaikuttavat NAFLD: n ja NASH: n etenemiseen. Tämä malli yrittää käyttää näitä tekijöitä ennustaakseen elämäntapamuutosten ja genetiikan vaikutuksia NAFLD -patologian kehittymiseen. Monet tutkijat kuvaavat NAFLD: tä monijärjestelmäsairaudeksi , koska se vaikuttaa muihin elimiin ja säätelyreitteihin kuin maksaan ja vaikuttaa niihin.
Ikääntyvien solujen kertyminen maksaan havaitaan henkilöillä, joilla on NAFLD. Hiirissä maksan ikääntyvät hepatosyytit lisäävät maksan rasvan kertymistä. NAFLD -hiirten hoidon senolyyttisilla aineilla on osoitettu vähentävän maksan steatoosia.
Perustuen geeni tyrmäys tutkimuksiin jyrsijämalleilla, on ehdotettu, että monien muiden patogeenisten tekijöiden TGFbeeta signaaleja voidaan ratkaisevasti mukana edistämässä etenemistä NASH.
Fruktoosin kulutus
Alkoholittomalla ja alkoholipitoisella rasvasairaudella on samanlaisia histologisia piirteitä, mikä viittaa siihen, että niillä saattaa olla yhteisiä patogeenisiä reittejä. Fruktoosi voi aiheuttaa maksatulehdusta ja riippuvuutta samalla tavalla kuin etanoli käyttämällä samanlaisia metabolisia reittejä, toisin kuin glukoosi. Siksi jotkut tutkijat väittävät, että alkoholittomat ja alkoholipitoiset rasvaiset maksasairaudet ovat samankaltaisempia kuin aiemmin luultiin. Lisäksi suuri fruktoosin kulutus edistää rasvan kertymistä maksaan stimuloimalla de novo lipogeneesiä maksassa ja vähentämällä rasvan beeta-hapettumista . Toisin kuin sokeri glukoosi , entsyymi fruktokinaasin nopeasti metaboloi fruktoosi. Tämä johtaa alentuneeseen solunsisäiseen adenosiinitrifosfaattiin (ATP). ATP: n väheneminen lisää oksidatiivista stressiä ja heikentää proteiinisynteesiä ja maksan mitokondrioiden toimintaa.
Insuliiniresistenssi
Insuliiniresistenssi edistää myrkyllisen rasvan kertymistä maksaan useilla tavoilla. Ensinnäkin se edistää vapaiden rasvahappojen (FFA) vapautumista rasvakudoksesta vereen. Tyypillisesti rasvakudos varastoi lipidejä triglyseridien muodossa ja vapauttaa niitä hitaasti verenkiertoon, kun insuliini on vähissä. Insuliiniresistentissä rasvakudoksissa, kuten lihavilla ja tyypin 2 diabetesta sairastavilla, enemmän triglyseridejä hajoaa FFA: ksi ja vapautuu verenkiertoon, mikä edistää maksan imeytymistä. Toiseksi insuliini edistää uusien FFA: iden tuotantoa maksassa de novo lipogeneesin kautta ; tätä maksarasvojen tuotantoa stimuloi edelleen insuliini, vaikka muut kudokset olisivat insuliiniresistenttejä. Nämä FFA: t yhdistetään takaisin triglyserideiksi maksassa muodostaen maksassa kertyneen rasvan pääainesosan. Kolme vapaiden rasvahappojen lähdettä, jotka edistävät maksan triglyseridien kertymistä, ovat verenkierrossa kiertävät FFA: t (59%), hiilihydraateista, kuten fruktoosista ja glukoosista, peräisin olevat FFA: t (26%) ja ruokavalio (14%). Huolimatta triglyseridien kertymisestä maksaan, ne eivät ole suoraan myrkyllisiä maksakudokselle. Sen sijaan muiden maksassa olevien lipidityyppien , kuten diasyyliglyserolien , fosfolipidien , keramidien ja vapaan kolesterolin , profiilin muuttamisella on tärkeämpi rooli NAFLD: n patogeneesissä.
Kun NAFLD etenee vakavuudessa NASH -pisteeseen, tämä edistää insuliiniresistenssin lisääntymistä rasvakudoksessa ja maksassa, mikä johtaa haitalliseen insuliiniresistenssiin, maksan rasvan kertymiseen ja tulehdukseen. Rasvakudos toimintahäiriö myös vähentää eritystä insuliiniherkistävä adipokine adiponectin ihmisten kanssa NAFLD. Adiponektiinillä on useita maksan suojaavia ominaisuuksia. Näitä ominaisuuksia ovat parantunut maksan rasva-aineenvaihdunta, vähentynyt de novo lipogeneesi, vähentynyt glukoosin tuotanto maksassa , tulehdusta estävät ominaisuudet ja fibroottiset ominaisuudet. Luustolihasten insuliiniresistenssillä voi myös olla rooli NAFLD: ssä. Insuliiniresistentti luustolihas ei ole yhtä tehokas glukoosin ottamisessa verenkierrosta aterian jälkeen. Tämä tehoton glukoosin otto edistää kulutettujen hiilihydraattien uudelleenjakautumista glukoosista, joka on tarkoitettu käytettäväksi luustolihasten glykogeenivarastoissa käytettäväksi substraattina maksan de novo lipogeneesissä.
Dysbioosi
Suoliston mikrobiston häiriöt näyttävät vaikuttavan NAFLD -riskiin useilla tavoilla. Ihmisillä, joilla on NASH, voi olla kohonnut veren etanolipitoisuus ja proteobakteerit (jotka tuottavat alkoholia), ja dysbioosia ehdotetaan tämän kohoamisen mekanismiksi. Suoliston mikrobiston koostumuksen muutokset voivat vaikuttaa NAFLD -riskiin monin tavoin. Nämä muutokset näyttävät lisäävän suolistokudoksen läpäisevyyttä, mikä helpottaa maksan altistumista haitallisille aineille (esim. Siirtyneet bakteerit, bakteerimyrkyt ja tulehdukselliset kemialliset signaalit ). Näiden haitallisten aineiden lisääntynyt kuljetus maksaan edistää maksatulehdusta, parantaa ravinteiden ja kalorien imeytymistä ja muuttaa koliinin aineenvaihduntaa. Korkeammat butyraattia tuottavat suolistobakteerit voivat olla suojaavia.
Liiallinen makroravinteiden saanti edistää suoliston tulehdusta ja homeostaasin häiriöitä, ja myös mikroravinteita voi olla mukana. Painon ja riskitekijöiden vähentämisen lisäksi elämäntapamuutokset voivat saada aikaan positiivisia muutoksia suoliston mikrobistossa. Erityisesti ruokavalion monimuotoisuudella voi olla rooli, joka jätettiin huomiotta eläinkokeissa, koska niissä verrataan usein länsimaista runsasrasvaista ja vähä monimuotoisuutta sisältävää ruokavaliota vähärasvaiseen mutta monimuotoisempaan ruokavalioon . Bariatrisen leikkauksen jälkeiset terveyshyödyt voivat myös sisältää muutoksia suoliston mikrobistoon lisäämällä suolen läpäisevyyttä.
Diagnoosi
NAFLD määritellään todisteilla rasvasta maksasta ilman muuta tekijää, joka voisi selittää maksan rasvan kertymisen, kuten liiallinen alkoholin käyttö (> 21 tavanomaista juomaa viikossa miehille ja> 14 naisille Yhdysvalloissa;> 30 g päivässä miehille ja> 20 g naisille Englannissa ja EU,> 140 g / viikko miehillä ja> 70 g / viikko naisten Aasiassa ja useimmat NIH kliinisissä tutkimuksissa), lääkkeen aiheuttama rasvamaksa , krooninen hepatiitti C, perinnöllisyys tai puutteita parenteraalisella ravitsemus , kuten koliini ja hormonitoiminta. Jos jokin näistä tekijöistä havaitaan, suositellaan tutkimusta vaihtoehtoisista rasvamaksan syistä, jotka eivät liity NAFLD: hen. Krooninen alkoholinkäyttö on tärkeä näkökohta.
NAFLD sisältää kaksi histologista luokkaa: NAFL ja aggressiivisempi muoto NASH. Vähintään 5% rasvaisen maksan esiintyminen on yhteistä sekä NAFL: lle että NASH: lle, mutta merkittävän lobulaarisen tulehduksen ja hepatosyyttivammojen, kuten ilmapalloilun tai Mallory -hyaliinin, ominaisuuksia esiintyy vain NASH: ssa. Suurin osa NAFL -tapauksista osoittaa tulehdusta minimaalisesti tai ei lainkaan. Perisentraalista ja perisinusoidista fibroosia esiintyy useammin aikuisilla alkaneessa NASH: ssa, kun taas portaalifibroosi on yleisempi lapsilla, joilla on häiriö. NASH edustaa NAFL: n edistyneempää vaihetta ja liittyy huonoihin tuloksiin, kuten sydän- ja verisuonitapahtumiin, kirroosiin tai maksasolusyöpään. ICD-11 ei käytä termiä NAFL, koska sen katsottiin sekoittavan NAFLD-häiriöperheeseen. Sen sijaan suositeltavat kuvaukset ovat: NAFLD ilman NASH: ta tai yksinkertainen steatoosi ja "NASH". Myös fibroosin tai kirroosin kanssa tai ilman modifioija täydentää diagnostista kuvausta.
Verikokeet
Kohonneet maksaentsyymit ovat yleisiä. Mukaan National Institute for Health and Care Excellence (NICE) suuntaviivoissa sitä disadvised testata entsyymien tasoja sulkea pois NAFLD, koska ne ovat usein normaalin rajoissa jopa edenneessä taudissa.
Verikokeita, jotka ovat hyödyllisiä diagnoosin vahvistamiseksi tai muiden sulkemiseksi pois, ovat punasolujen sedimentaatioaste , glukoosi , albumiini ja munuaisten toiminta . Koska maksa on tärkeä veren hyytymiseen käytettävien proteiinien valmistuksessa , suoritetaan usein hyytymiseen liittyviä tutkimuksia, erityisesti INR ( kansainvälinen normalisoitu suhde ). Ihmisillä, joilla on rasvamaksa ja siihen liittyvä tulehdusvaurio (steatohepatiitti), verikokeita käytetään yleensä virushepatiitin (hepatiitti A, B, C ja herpesvirukset , kuten Epstein-Barr-virus tai sytomegalovirus ), vihurirokon ja autoimmuunisairauksien poissulkemiseen. Alhainen kilpirauhasen toiminta on yleisempi NASH-potilailla, mikä havaitaan määrittämällä kilpirauhasta stimuloiva hormoni . Joitakin biomarkkeripohjaisia verikokeita on kehitetty ja ne voivat olla hyödyllisiä diagnoosissa.
Vaikka verikokeilla ei voida diagnosoida NAFLD: tä, maksan fibroosin kiertävät seerumin biomarkkerit voivat antaa kohtalaisia arvioita maksafibroosin ja kirroosin diagnosoinnissa. Aasian ja Tyynenmeren yhdistys suosittelee , että transaminaasimaksan entsyymi- aspartaattiaminotransferaasin (AST) ja verihiutaleiden suhde, joka tunnetaan AST/verihiutale-suhdeindeksinä (APRI-pisteet), ja Fibrotest ovat ensisijaisia ei-invasiivisia kirroosin testejä. maksasta (APASL). Useat muut pisteet, kuten FIB-4-pisteet ja NAFLD-fibroosipisteet, voivat myös heijastaa maksan fibroosin taakkaa, ja aiemmat tutkimukset ovat vahvistaneet, että nämä pisteet voivat ennustaa kuolleisuuden ja maksasyövän tulevaa kehitystä.
Kuvantaminen

Maksan ultraäänitutkimus tai magneettikuvaus (MRI) voi diagnosoida steatoosin, mutta ei fibroosia, ja suositellaan varhaisen kirroosin havaitsemisen varmistamista ultraäänellä muilla diagnostisilla menetelmillä. European Association for Study of maksan (EASL) suosittelee seulomalla rasvamaksa aina NAFLD epäillään koska tämä on vahva ennustaja taudin kehittyminen ja ennakoi tulevia tyypin 2 diabeteksen, sydän- ja verisuonitapahtumien ja verenpainetauti . Näitä ei-invasiivisia menetelmiä voidaan käyttää NAFLD-seulontaan, mutta niitä ei hyväksytä korvaamaan maksan biopsiaa NAFLD- eikä NASH-kliinisissä tutkimuksissa, koska vain maksan biopsia voi määrittää maksapatologian.
CT -skannaus ja MRI ovat tarkempia kirroosin havaitsemisessa kuin tavanomainen ultraääni. Ohimenevää elastografiaa suositellaan maksafibroosin ja kirroosin alustavaan arviointiin, ja se auttaa ennustamaan komplikaatioita ja ennustetta, mutta tulosten tulkinta punnitaan huolellisesti rajoittavien tekijöiden, kuten steatoosin, korkean BMI: n, alhaisemman maksafibroosin ja kapean läsnäolon läsnä ollessa kylkiluiden väliset välilyönnit (intercostal -välilyönnit). Kuitenkin ohimenevä elastografia voi epäonnistua ihmisillä, joilla on maksan esiportaalihypertensio . Ohimenevää elastografiaa ei pidetä korvaavana maksan biopsiassa.
Magneettinen resonanssielastografia (MRE) on kehittymässä oleva menetelmä, jolla voidaan arvioida tarkasti maksan fibroosi ja jota APASL suosittelee. MRE: llä on hyvä herkkyys mitata maksarasvaa ja erinomainen tarkkuus fibroosin havaitsemiseksi NAFLD: ssä BMI: stä ja tulehduksesta riippumatta, ja sitä ehdotetaan luotettavammaksi vaihtoehdoksi diagnosoida NAFLD ja sen eteneminen NASH: ksi verrattuna ultraääni- ja verikokeisiin.
Maksan biopsia
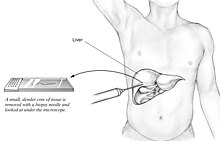

Maksabiopsia (kudos tutkimus) on ainoa testi laajalti hyväksytty (kultainen standardi) lopullisesti diagnosoinnissa ja erottaa NAFLD (mukaan lukien NAFL ja NASH) muiden maksasairauden muotojen, ja sitä voidaan käyttää arvioimaan vakavuuden tulehduksen ja tuloksena fibroosia. Kuitenkin, koska useimmat ihmiset, joihin NAFLD vaikuttaa, ovat todennäköisesti oireettomia, maksan biopsia aiheuttaa liian suuren tavanomaisen diagnoosin riskin, joten muita menetelmiä suositellaan, kuten maksan ultraääni tai maksan magneettikuvaus . Nuorille suositellaan maksan ultraäänitutkimusta, mutta biopsia on edelleen paras todiste. Maksan biopsia on myös kultainen standardi maksafibroosin havaitsemiseksi ja sen etenemisen arvioimiseksi. Säännölliset maksan toimintakokeet eivät ole riittävän herkkiä NAFLD: n havaitsemiseksi, ja biopsia on ainoa menetelmä, joka voi erottaa NAFL: n luotettavasti NASH: sta.
Maksakudoksen saamiseksi on saatavilla useita maksan biopsiatekniikoita. Perkutaaninen maksan biopsia on edelleen yleisin käytäntö. Biopsiat voidaan tehdä myös laskimoon, joko leikkauksen aikana tai laparoskopialla , erityisesti ihmisille, joilla on vasta -aiheita perkutaaniseen lähestymistapaan. Maksan biopsia voidaan myös ohjata kuvaan, reaaliajassa tai ei, mikä on suositeltavaa joissakin kliinisissä tilanteissa, kuten ihmisillä, joilla on tunnettuja maksan sisäisiä vaurioita, aiempi vatsan sisäinen leikkaus, jolla voi olla adheesiota, pieni maksa, joka on vaikea lyömäsoittimille, lihaville ihmisille ja ihmisille, joilla on ilmeinen askites. Elintoimintoja on seurattava usein sen jälkeen (vähintään 15 minuutin välein biopsian jälkeisessä tunnissa).
AASLD -ohjeiden mukaan maksabiopsiaa voidaan harkita NAFLD -potilailla, joilla on lisääntynyt riski saada steatohepatiitti, johon liittyy tai ei ole edennyt fibroosi, mutta vain silloin, kun kaikki muut kilpailevat krooniset maksasairaudet (kuten alkoholisairaus) on suljettu pois. Metabolisen oireyhtymän, NAFLD-fibroosipisteen (FIB-4) tai maksan jäykkyyden (mitattuna värähtelyohjatulla ohimenevällä elastografialla tai MRE: llä ) läsnäolo voi tunnistaa yksilöitä, joilla on suurempi riski saada steatohepatiitti tai pitkälle edennyt fibroosi.
AASLD ja ICD-11 katsovat, että kliinisesti hyödyllinen patologiaraportointi tekee eron "NAFL: n (steatoosi), NAFL: n kanssa, jolla on tulehdus, ja NASH: n (steatoosi, johon liittyy lobaari- ja portaalitulehdus ja maksasolujen ilmapalloilu)", jossa kuvataan fibroosin esiintyminen tai puuttuminen ja valinnaisesti kommentoidaan vakavuus. EASL suosittelee rasvaisen maksan etenemisen esto (FLIP) -algoritmia ilmapallon arvioimiseksi ja NAFLD: hen liittyvän maksavaurion luokittelemiseksi, ja NAFLD-aktiivisuustuloksen (NAS) käyttöä NASH: n vakavuuden arvioimiseksi sen diagnoosin sijasta. He pitävät myös steatoosia, aktiivisuutta ja fibroosia (SAF) pisteinä tarkana ja toistettavana pisteytysjärjestelmänä. AASLD suosittelee NAS -pisteytysjärjestelmän käyttöä SAF -pisteillä tai ilman niitä, jos se katsotaan aiheelliseksi. Aasian ja Tyynenmeren alueen NAFLD-työryhmä ei suosittele NAS: n käyttöä, koska sitä pidetään epäinformatiivisena NAFLD: lle ja sopimattomaksi diagnosoida NASH.
Maksafibroosin arviointia varten perkutaaninen maksan biopsia, kuvaopastuksella tai ilman, on vasta -aiheinen yhteistyöhön osallistumattomille ihmisille. Transjugulaarinen maksan biopsia on tarkoitettu kaikille henkilöille, joilla on diffuusi maksasairaus ja joka tarvitsee biopsian, mutta jolla on vasta -aihe perkutaaniselle biopsialle tai joka tarvitsee hemodynaamisen arvioinnin diagnostisiin tarkoituksiin. Potilaalle, jolla on kliinisesti ilmeinen askiitti, suositellaan transvenoosista maksan biopsiaa perkutaanisen lähestymistavan sijasta, vaikka perkutaaninen biopsia on hyväksyttävä vaihtoehtoinen tapa askitesin poistamisen jälkeen.
Hallinto
NAFLD takaa hoidon riippumatta siitä, onko sairastunut ylipainoinen vai ei. NAFLD on ehkäistävissä oleva kuolinsyy . Ohjeita on saatavana American Association for the Study of Liver Diseases (AASLD), American Association of Clinical Endocrinologists (AACE) National Institute for Health and Care Excellence (NICE), European Association for the Study of the Liver (EASL) ja Aasian ja Tyynenmeren alueen NAFLD-työryhmä.
Elämäntapa
Painonpudotus on tehokkain hoito NAFLD: lle. 4–10%: n painonpudotusta suositellaan, ja 10–40%: n laihtuminen kääntää NASH: n kokonaan ilman kirroosia. Jäsennelty painonpudotusohjelma auttaa ihmisiä, joilla on NAFLD, laihtumaan enemmän kuin pelkästään neuvoja. Tämäntyyppinen ohjelma johtaa myös parannuksiin NAFLD: ssä, joka mitataan verikokeilla, ultraäänellä, kuvantamisella tai maksan biopsioilla. Vaikka fibroosi paranee elämäntapatoimenpiteillä ja laihtumisella, on olemassa vain vähän todisteita kirroosin parantumisesta.
Parannetun ruokavalion ja liikunnan yhdistelmä ei yksinään näytä parhaiten auttavan hallitsemaan NAFLD: tä ja vähentämään insuliiniresistenssiä. Motivaatiotuki, kuten kognitiivinen käyttäytymisterapia , on hyödyllistä, koska useimmat NAFLD -potilaat eivät näe tilansa sairautena ja siksi heillä on heikko motivaatio muuttua.
Korkeamman intensiteetin käyttäytymispainonpudotushoidot (ruokavalio ja liikunta yhdistettynä) voivat aiheuttaa enemmän laihtumista kuin matalamman intensiteetin. Laihtuminen liittyy biomarkkereiden, NAFLD-luokan ja NASH: n mahdollisuuksien pienenemiseen, mutta niiden vaikutus pitkäaikaiseen terveyteen ei ole vielä tiedossa. Vuoden 2019 järjestelmällinen katsaus ehdottaa näin ollen suuntaviivojen muuttamista näiden hoitojen suosittamiseksi NAFLD: n hallintaan.
Ruokavalio
NAFLD: n hoito sisältää tyypillisesti neuvontaa ravinnon ja kalorien rajoittamisen parantamiseksi . Ihmiset, joilla on NAFLD, voivat hyötyä kohtalaisesta vähähiilihydraattiseen ruokavalioon ja vähärasvaiseen ruokavalioon. Välimeren ruokavalio osoitti myös lupaavia tuloksia 6 viikon tutkimuksessa, jossa NASH: n aiheuttama tulehdus ja fibroosi vähenivät riippumatta painonpudotuksesta. Alustavat todisteet tukevat ruokavalion toimenpiteitä henkilöillä, joilla on rasvainen maksa ja jotka eivät ole ylipainoisia.
EASL suosittelee 500–1000 kcal: n energianrajoitusta viikossa vähemmän kuin normaali päivittäinen ruokavalio ( erittäin vähäkalorinen ruokavalio ). Tavoite on 7–10%: n laihtuminen lihaville/ylipainoisille NAFLD-rasvoille, jotka ovat vähärasvaisia tai kohtalaisia ja kohtalainen tai runsashiilihydraattinen ruokavalio tai vähähiilihydraattinen ketogeeninen tai runsaasti proteiinia sisältävä ruokavalio, kuten Välimeren ruokavalio, ja vältetään kaikki juomat ja fruktoosia sisältävät elintarvikkeet.
Alkoholi on raskauttava tekijä, ja AASLD suosittelee, että ihmiset, joilla on NAFLD tai NASH, välttävät alkoholin käyttöä. EASL sallii alkoholin kulutuksen alle 30 grammaa päivässä miehille ja 20 grammaa päivässä naisille. Kahvin kulutuksen rooli NAFLD -hoidossa on epäselvä, vaikka jotkut tutkimukset osoittavat, että säännöllisellä kahvinkulutuksella voi olla suojaavia vaikutuksia.
E -vitamiini ei paranna vakiintunutta maksafibroosia niillä, joilla on NAFLD, mutta näyttää parantavan tiettyjä maksan toiminnan merkkejä ja vähentävän maksan tulehdusta ja rasvaisuutta joillakin NAFLD -potilailla. Aasian ja Tyynenmeren työryhmä neuvoo, että E-vitamiini voi parantaa maksan tilaa ja aminotransferaasitasoja, mutta vain aikuisilla, joilla ei ole diabetesta tai kirroosia ja joilla on NASH. NICE -suositukset suosittelevat E -vitamiinia vaihtoehtona lapsille ja aikuisille, joilla on pitkälle edennyt maksafibroosi, riippumatta siitä, onko henkilöllä diabetes mellitus.
Yrttiyhdisteet, kuten silymariini ( maito -ohdakkeen siemenuute), kurkumiini, kurkumauute ja vihreä tee näyttävät parantavan NAFLD -biomarkkereita ja vähentävän NAFLD -laatua. Tutkimukset viittaavat yhteyteen suolistossa elävien mikroskooppisten organismien (mikrobiota) ja NAFLD: n välillä. Arvioinnit raportoivat probioottien ja synbioottien (probioottien ja prebioottien yhdistelmät ) käytön liittyvän maksan tulehduksen maksaspesifisten merkkiaineiden, maksan jäykkyyden ja steatoosin paranemiseen NAFLD-potilailla.
Liikunta
Painonpudotus voi parantaa NAFLD: tä, ja sitä suositellaan erityisesti lihaville tai ylipainoisille ihmisille. samanlaiset fyysiset aktiviteetit ja ruokavalio ovat suositeltavia ylipainoisille NAFLD -potilaille kuin muillekin lihaville ja ylipainoisille ihmisille. Vaikka fyysinen aktiivisuus on laihdutuksessa vähemmän tärkeä kuin ruokavalion mukauttaminen (kalorien saannin vähentämiseksi), NICE neuvoo liikuntaa vähentämään maksan rasvaa, vaikka kokonaispainon lasku ei tapahtuisi. Painonpudotus liikunnan tai ruokavalion kautta on tehokkain tapa vähentää maksan rasvaa ja auttaa NASH: ta ja fibroosin remissiota. Liikunta yksin voi estää tai vähentää maksan steatoosia, mutta ei tiedetä, voiko se parantaa kaikkia muita maksan näkökohtia; siksi suositellaan yhdistettyä lähestymistapaa ruokavalion ja liikunnan kanssa. Aerobinen harjoittelu voi olla tehokkaampaa kuin vastusharjoittelu, vaikka tulokset ovat ristiriitaisia. Voimakas harjoittelu on parempi kuin kohtalainen harjoittelu, koska vain voimakas harjoitus vähensi mahdollisuuksia NAFLD: n kehittymiseen NASH: ksi tai pitkälle edenneeksi fibroosiksi. EASL suosittelee 150–200 minuuttia viikossa 3–5 kohtalaisen voimakkaan aerobisen liikunnan tai kestävyysharjoituksen aikana. Koska molemmat vähentävät tehokkaasti maksan rasvaa, on edullista käyttää pragmaattista lähestymistapaa liikunnan valinnassa, joka ottaa huomioon yksilön mieltymykset siitä, mitä he voivat säilyttää pitkällä aikavälillä. Mikä tahansa sitoutuminen fyysiseen toimintaan tai lisääntyminen edelliseen tasoon verrattuna on parempi kuin istuminen.
Lääkitys
Lääkityshoidolla pyritään ensisijaisesti parantamaan maksasairautta, ja se rajoittuu yleensä niihin, joilla on biopsialla todistettu NASH ja fibroosi.
Yksikään NAFLD- tai NASH -lääkitys ei ollut saanut hyväksyntää vuodesta 2018, vaikka diabeteslääkkeet voivat auttaa maksan rasvan menetyksessä. Vaikka monet hoidot näyttävät parantavan biokemiallisia markkereita, kuten alaniinitransaminaasitasoja , useimmat eivät kumoa histologisia poikkeavuuksia tai paranna tuloksia.
Insuliiniherkistäviä aineita ( metformiini ja tiatsolidiinidionit , kuten pioglitatsoni ) ja liraglutidia ei suositella erityisesti NAFLD: lle, koska ne eivät paranna suoraan maksan tilaa. Ne voidaan antaa diabeetikoille riskien huolellisen arvioinnin jälkeen insuliiniresistenssin ja komplikaatioiden riskin vähentämiseksi. Itse asiassa tiatsolidiinidionilääkkeisiin liittyvät sivuvaikutukset, joihin kuuluvat osteopenia , lisääntynyt murtumariski, nesteen kertyminen, kongestiivinen sydämen vajaatoiminta , virtsarakon syöpä ja pitkäaikainen painonnousu, ovat rajoittaneet niiden hyväksymistä. Näiden sivuvaikutusten vuoksi AASLD suosittelee pioglitatsonin käyttöä vain henkilöille, joilla on biopsialla todistettu NASH, ja Aasian ja Tyynenmeren työryhmä suosittelee niitä vain henkilöille, joilla on NAFLD ja joilla on tunnettuja diabeettisia ongelmia. AASLD neuvoo kuitenkin olemaan käyttämättä metformiinia, koska tutkimukset eivät olleet vakuuttavia maksan histologisen tilan parantumisesta. Vaikka insuliiniresistenssi ja seerumin aminotransferaasit paranivat, tämä ei johtanut NASH -parannuksiin. NICE tarjoaa samanlaisia ohjeita AASLD: lle pioglitatsonin suhteen ja suosittelee sen antamista toissijaisessa hoidossa aikuisille, joilla on pitkälle edennyt maksafibroosi riippumatta siitä, onko heillä diabetes.
Statiinilääkkeet näyttävät parantavan maksan histologiaa ja maksan biokemian merkkejä NAFLD -potilailla. Koska NAFLD -potilailla on suurempi sydän- ja verisuonisairauksien riski, statiinihoito on aiheellista. AASLD: n ja EASL: n mukaan NAFLD -potilailla ei ole suurempi riski vakavasta maksavauriosta statiineista. Vaikka statiineja on turvallista käyttää NASH -kirroosia sairastavilla ihmisillä, AASLD ehdottaa, että niitä vältetään ihmisillä, joilla on dekompensoitu kirroosi. Ohjeissa suositellaan statiineja dyslipidemian hoitoon ihmisille, joilla on NAFLD. NICE -ohjeiden mukaan statiinit voivat jatkaa, ellei maksaentsyymitasot kaksinkertaistuvat kolmen kuukauden kuluessa statiinien aloittamisesta. Hoidon pentoksifylliini ei suositella.
Vuodesta 2018 lähtien AASLD tai Aasian ja Tyynenmeren työryhmä eivät suosittele obetikoolihappoa tai elafibranoria NASH-hoidon epäjohdonmukaisten tulosten ja turvallisuuteen liittyvien huolenaiheiden vuoksi.
Omega-3-rasvahapot voivat vähentää maksan rasvaa ja parantaa veren lipidiprofiilia, mutta eivät näytä parantavan maksan histologiaa (fibroosi, kirroosi, syöpä). NICE ei suosittele omega-3-rasvahappolisää, koska satunnaistetut tutkimukset eivät olleet vakuuttavia. Aiemmissa systemaattisissa katsauksissa havaittiin, että omega-3-rasvahappojen lisäys NAFLD/NASH-potilailla, jotka käyttävät yhtä grammaa vuorokaudessa tai enemmän (mediaaniannos neljä grammaa päivässä, kun hoidon kesto on keskimäärin kuusi kuukautta), on liittynyt maksan rasvan paranemiseen. AASLD-ohjeiden mukaan "omega-3-rasvahappoja ei tule käyttää NAFLD- tai NASH-hoitona, mutta niiden voidaan katsoa hoitavan hypertriglyseridemiaa potilailla, joilla on NAFLD".
Leikkaus

Bariatrinen kirurgia on tehokas menetelmä lihaville ja diabeetikoille, joilla on NAFLD, laihtumisen indusoimiseksi ja NASH -tulehduksen, mukaan lukien fibroosi, vähentämiseksi tai ratkaisemiseksi ja pitkäikäisyyden parantamiseksi. AASLD: n osalta bariatrinen kirurgia voidaan harkita vain NASH: n tapauksessa tapauskohtaisesti kokeneen bariatric-leikkausohjelman avulla. Jotkut ihmiset voivat todella kehittää uusia tai huonontuneita NAFLD -ominaisuuksia.
Noin 92% NAFLD -potilaista näki steatoosin paranemisen ja 70% täydellistä paranemista bariatrisen leikkauksen jälkeen.
Ennen leikkausta tapahtuvaa ruokavaliota, kuten vähäkalorista ruokavaliota tai erittäin vähäkalorista ruokavaliota, suositellaan yleensä maksan tilavuuden vähentämiseksi 16–20%. Leikkausta edeltävä laihtuminen on ainoa leikkauksen jälkeiseen laihtumiseen liittyvä tekijä. Leikkausta edeltävä laihtuminen voi lyhentää leikkausaikaa ja sairaalahoitoa, vaikka ei ole riittävästi näyttöä siitä, vähentääkö leikkausta edeltävä laihtuminen pitkäaikaista sairastuvuutta vai komplikaatioita. Painon lasku ja maksan koon pieneneminen voivat olla riippumattomia kalorien rajoituksen määrästä.
NAFLD: n APWG suosittelee bariatrista leikkausta hoitovaihtoehtona niille, joilla on luokan II liikalihavuus ( BMI > 32,5 kg/m 2 aasialaisille, 35 kg/m 2 valkoihoisille). He pitävät sen vaikutuksia maksan komplikaatioiden parantamiseen vielä todistamattomina, mutta se lisää tehokkaasti pitkäikäisyyttä parantamalla sydän- ja verisuonitekijöitä.
Leikkaus aiheuttaa enemmän riskejä NASH -kirroosia sairastaville henkilöille, ja yleisen sairastuvuuden arvioidaan olevan 21%. Ihmisille, joilla on NAFLD ja joilla on erilaistumaton kirroosi, APWG suosittelee tutkimusta kirroosin syyn sekä henkilön maksan toiminnan selvittämiseksi ja onko heillä portaalihypertensio.
Seulonta
EASL pitää sydän- ja verisuonijärjestelmän seulontaa pakollisena, koska NAFLD-tulokset johtavat usein sydän- ja verisuonikomplikaatioihin , jotka voivat ilmetä subkliinisenä ateroskleroosina , joka on suurin osa NAFLD: hen liittyvistä kuolemista. NAFLD -potilailla on suuri sydän- ja verisuonisairauksien ja kuolleisuuden riski, ja " sydän- ja verisuonitautien riskitekijöiden aggressiivinen muuttaminen on perusteltua kaikille NAFLD -potilaille", AASLD: n mukaan.
AASLD suosittelee lisäksi ihmisille, joilla on kirroosi NASH, seulomaan järjestelmällisesti mahalaukun ja ruokatorven suonikohjut ja maksasyöpä . He eivät suosittele rutiininomaisia maksan biopsioita ja maksasyövän seulontaa ei-kirroosipotilaille, joilla on NASH, mutta tällainen seulonta tapahtuu joskus tapauskohtaisesti.
Myös NAFLD -potilaita voidaan harkita hepatosellulaarisen karsinooman (maksasyövän) ja gastroesofageaalisten suonikohjujen seulontaan . NICE suosittelee NAFLD: n säännöllistä seulontaa pitkälle edenneen maksafibroosin varalta aikuisille ja joka toinen vuosi lapsille, jotka käyttävät tehostettua maksafibroosia (ELF). Seurantaa suositellaan ihmisille, joilla on liikalihavuus ja insuliiniresistenssi, käyttämällä insuliiniresistenssin homeostaasimallin arviointia (HOMA-IR). Ihmiset, joilla on NASH, joilla on fibroosi ja hypertensio, ansaitsevat tarkempaa seurantaa, koska taudin etenemisen riski on suurempi.
Elinsiirto
NAFLD on toiseksi yleisin indikaatio maksansiirrolle Yhdysvalloissa ja Euroopassa vuodesta 2017. NAFLD/NASH: sta odotetaan tulevan maksansiirron johtava syy vuoteen 2020 mennessä.
Ihmisille, joilla on NASH ja loppuvaiheen maksasairaus, maksan vajaatoiminta tai maksasyöpä, maksansiirto on hyväksytty menettely EASL: n mukaan. Ihmiset, joilla on NASH -kirroosi NASH ja joita harkitaan maksansiirrolle, vaativat systemaattisen arvioinnin sydän- ja verisuonitaudeista (ovatko oireet ilmeisiä vai eivät).
Kokonaiselossaolo on verrattavissa muiden sairauksien jälkeiseen elinsiirtoon. Ihmiset, joilla on NASH-kirroosi ja joille suoritetaan maksansiirto, kuolevat todennäköisemmin elinsiirron jälkeen sydän- ja verisuonisairauksien tai kroonisen munuaissairauden vuoksi . Nämä NASH -potilaat ovat usein vanhempia ja ovat siten alttiimpia näille komplikaatioille. Näistä syistä ja muista syistä yksilöitä, joilla on sairas lihavuus ( BMI ≥ 40 kg/m 2 ) ja NASH, joilla on kirroosi, voidaan pitää kelpaamattomina maksansiirtoon, kunnes he noudattavat elämäntapamuutoksia ruumiinpainon vähentämiseksi. Diabeetikoilla, joilla on huono verensokeri, on samanlaisia riskejä, ja optimaalinen verensokeri on välttämätöntä ennen elinsiirtoa.
Aasian ja Tyynenmeren työryhmän ohjeissa suositellaan, että terveydenhuollon tarjoajat keskustelevat elämäntapamuutoksista ennen elinsiirtoa ja sen jälkeen, jotta voidaan vähentää mahdollisia leikkausriskejä ja auttaa NAFLD -hoidossa elinsiirron jälkeen.
Poikkeuksellisissa olosuhteissa tehtiin samanaikainen bariatrinen leikkaus ja maksansiirto.
Elinsiirron jälkeen maksan biopsia on paras tapa seurata elinsiirron jälkeisen fibroosin kehittymistä, ja merkittävä fibroosi tai portaalinen hypertensio vuoden kuluttua siirrosta ennustaa nopeaa etenemistä ja siirteen menettämistä ja osoittaa kiireellisen toimenpiteen tarpeen.
Aiheeseen liittyvät komplikaatiot
NAFLD/NASH: hon liittyvää maksasyöpää ei hoideta erityisellä tavalla, ja sitä hoidetaan maksasyöpää koskevien yleisten ohjeiden mukaisesti.
Ennuste
Keskimääräisen etenemisnopeuden maksafibroosin yhdestä vaiheesta seuraavaan ihmisillä, joilla on NASH, arvioidaan olevan seitsemän vuotta verrattuna 14 vuoteen NAFLD: n kanssa. Etenemisvaihe vaihtelee yksilöiden eri kliinisten ilmentymien mukaan. Fibroosi NASH -potilailla eteni nopeammin kuin ihmisillä, joilla oli NAFLD. Lihavuus ennustaa huonomman pitkän aikavälin lopputuloksen kuin laihoilla yksilöillä. Aasian ja Tyynenmeren alueella noin 25% NAFLD-tapauksista etenee NASH: iin alle kolmessa vuodessa, mutta vain pienelle osalle (3,7%) kehittyy pitkälle edennyt maksafibroosi. Kansainvälinen tutkimus osoitti, että NAFLD-potilailla oli 10 vuoden eloonjäämisaste 81,5%.
NAFLD on riskitekijä fibroosille, kohonneelle verenpaineelle, krooniselle munuaissairaudelle, eteisvärinälle , sydäninfarktille, iskeemiselle aivohalvaukselle ja sydän- ja verisuonitautien aiheuttamalle kuolemalle. Vaikka NAFLD voi aiheuttaa kirroosia ja maksan vajaatoimintaa ja maksasyöpää, useimmat kuolemat NAFLD -potilaiden keskuudessa johtuvat sydän- ja verisuonitaudeista. Erään meta-analyysin 34000 ihmisiä NAFLD yli seitsemän vuotta, nämä henkilöt on 65% suurempi riski sairastua kuolemaan johtavia tai ei-fataalin kardiovaskulaaristen tapahtumien verrattuna niihin ilman NAFLD.
NAFLD ja NASH lisäävät maksasyövän riskiä. NAFLD: n aiheuttama kirroosi ja maksasyöpä olivat toinen syy maksansiirtoon Yhdysvalloissa vuonna 2017. Maksasyöpä kehittyy NASH: ssa ilman kirroosia 45%: ssa tapauksista, ja NASH -kirroosia sairastavilla ihmisillä on lisääntynyt maksasyövän riski. NASH: aan liittyvä maksasyövän määrä kasvoi nelinkertaiseksi vuosina 2002–2012 Yhdysvalloissa, mikä on enemmän kuin mikään muu maksasyövän syy. NAFLD on kolmanneksi yleisin maksasyövän riskitekijä. NAFLD: n ja NASH: n havaittiin pahenevan kirroosissa 2–3%: lla ja 15–20%: lla ihmisistä 10–20 vuoden aikana. Kirroosia esiintyy vain noin 50 prosentilla NAFLD -potilaista ja maksasyövästä, joten maksasyöpä ja kirroosi eivät aina liity toisiinsa.
NAFLD voi olla metabolisen oireyhtymän edeltäjä, vaikka kaksisuuntainen vaikutus on mahdollinen. Fibroosin esiintyminen ja vaihe ovat voimakkaimmat maksan aiheuttamien tapahtumien ja kuolleisuuden, erityisesti NAFLD: n, ennustavat tekijät.
Epidemiologia
NAFLD -esiintyvyys kasvaa nopeasti sekä lihavuus että diabetes, ja siitä on tullut yleisin maksasairauksien syy kehittyneissä maissa aikuisille, nuorille ja lapsille. NAFLD -potilaiden prosenttiosuus on 9-36,9% eri puolilla maailmaa. Noin 20 prosentilla Yhdysvalloista ja 25 prosentilla Aasian ja Tyynenmeren alueen väestöstä on alkoholiton rasvamaksa. Euroopassa esiintyy samanlaista esiintyvyyttä, vaikka tietoja on vähemmän. NAFLD on yleisin Lähi -idässä (32%) ja Etelä -Amerikassa (30%), kun taas Afrikassa on alhaisimmat hinnat (13%). 2000-luvulle verrattuna NAFL ja NASH kasvoivat 2-kertaisesti ja 2,5-kertaisesti 2010-luvulla Yhdysvalloissa.
NAFLD ja NASH ovat yleisempiä latinalaisamerikkalaisissa - mikä johtuu korkeasta lihavuudesta ja tyypin 2 diabeteksesta latinalaisamerikkalaisissa väestöissä, keskitasosta valkoisissa ja alhaisimmassa mustissa. NAFLD: n havaittiin olevan kaksi kertaa yleisempi miehillä kuin naisilla. Sillä vaikeasti lihavilla yksilöt, esiintyvyys NAFLD nousee yli 90%, ja niille, joilla on diabetes , yli 60%, ja jopa 20%: normaalipainoisilla ihmistä. NAFLD on läsnä 65-90 prosentilla ihmisistä, joilla oli bariatrinen leikkaus, ja jopa 75 prosentilla heistä on NASH. Ultrasonografian ja protonien NMR -spektroskopiatutkimukset viittaavat siihen, että NAFLD tai NASH vaikuttaa vaikuttavan noin 25 prosenttiin väestöstä.
Vaikka tauti liittyy yleisesti lihavuuteen, merkittävä osa sairastuneista on normaalipainoisia tai laihoja. Laiha NAFLD vaikuttaa 10–20 prosenttiin amerikkalaisista ja eurooppalaisista ja noin 25 prosenttiin aasialaisista. PNPLA3 voi olla merkityksellinen NAFLD: n etenemiselle laihoilla ihmisillä. Siten ihmiset, jotka kärsivät NAFLD: stä, ansaitsevat hoidon riippumatta lihavuuden esiintymisestä tai puuttumisesta.
1–19 -vuotiailla lapsilla esiintyvyyden todettiin olevan noin 8% väestöstä ja jopa 34% tutkimuksissa, joissa oli tietoja lasten liikalihavuusklinikoista.
Suurin osa kryptogeenisestä kirroosista uskotaan johtuvan NASH: sta. NAFLD -esiintyvyyden odotetaan kasvavan tasaisesti, 25 prosentista vuonna 2018 33,5 prosenttiin ihmisistä, joilla on NAFLD maailmanlaajuisesti vuonna 2030, ja 20 prosentista ennustettuun 27 prosenttiin NAFLD -potilaista etenee NASH: ksi.
Historia
Ensimmäinen tunnustettu lihavuuteen liittyvä alkoholiton rasvamaksa havaittiin vuonna 1952 Samuel Zelmanin toimesta. Zelman aloitti tutkinnan havaittuaan rasvan maksan sairaalan työntekijällä, joka joi yli kaksikymmentä pulloa Coca-Colaa päivässä. Sitten hän suunnitteli puolitoista vuotta kestäneen oikeudenkäynnin 20 lihavalle ihmiselle, jotka eivät olleet alkoholisteja. Rasva maksa oli kuitenkin yhteydessä diabetekseen ainakin vuodesta 1784 lähtien - havainto nousi jälleen 1930 -luvulla. Koe -eläimillä tehdyt tutkimukset viittasivat koliinin riittämättömyyteen 1920 -luvulla ja liialliseen sokerin kulutukseen vuonna 1949.
Nimi "alkoholiton steatohepatiitti" (NASH) määritettiin myöhemmin vuonna 1980 Jurgen Ludwigin ja hänen kollegoidensa Mayo Clinicin toimesta tietoisuuden lisäämiseksi tämän patologian olemassaolosta, koska vastaavat raportit hylättiin aiemmin "potilaiden valheina". Tätä paperia sivuutettiin tuolloin enimmäkseen, mutta lopulta sitä pidettiin merkittävänä paperina, ja 1990-luvun puolivälistä lähtien ehtoa alkoi tutkia intensiivisesti, ja aiheesta järjestettiin useita kansainvälisiä kokouksia vuodesta 1998 lähtien. laajempaa NAFLD -termiä alettiin käyttää vuoden 2002 tienoilla. Diagnostisia kriteerejä alettiin laatia, ja vuonna 2005 NIH NASH Clinical Research Networkin patologiakomitea ehdotti NAS -pisteytysjärjestelmää.
Yhteiskunta ja kulttuuri
Poliittiset suositukset
EASL suosittelee, että Euroopan kansanterveysviranomaiset "rajoittavat sokerilla makeutettujen juomien ja teollisesti jalostettujen elintarvikkeiden mainostamista ja markkinointia, joissa on runsaasti tyydyttyneitä rasvoja, sokeria ja suolaa", sekä "verotoimenpiteitä sokerilla makeutettujen juomien kulutuksen estämiseksi ja lainsäädäntöä varmistettava, että elintarviketeollisuus parantaa jalostettujen elintarvikkeiden merkintöjä ja koostumusta "sekä" maksan sairauksia koskevat julkiset tiedotuskampanjat korostamalla, että se ei liity vain liialliseen alkoholinkulutukseen ".
Lobbaus
Ranskassa ranskalainen aikakauslehti fr: Canard Enchainé tuomitsi Ranskan alkoholittomien juomien syndikaatin "Boissons Rafraîchissantes de France" (johon kuuluivat virvoitusjuomien valmistajat, kuten Coca-Cola France, Orangina, PepsiCo France) kuluttajien harhaanjohtamisesta. viestinnän verkkosivustollaan "Parempi ymmärrys NASH-patologiasta", jossa selitetään, että "NASH-patologiaa kutsutaan joskus soodasairaudeksi kielen väärinkäytön tai valitettavan semanttisen pikavalinnan takia, koska se ei liity suoraan alkoholittomien juomien kulutukseen". Tämä sivu ja muut samalla verkkosivustolla olevat sivut, kuten "Sano ei väärälle tiedolle", on poistettu siitä lähtien.
Lapset
Lasten NAFLD: stä ilmoitettiin ensimmäisen kerran vuonna 1983. Se on yleisin krooninen maksasairaus lasten ja nuorten keskuudessa ainakin vuoden 2007 jälkeen, ja se vaikuttaa 10–20 prosenttiin Yhdysvalloista vuonna 2016. NAFLD liittyy metaboliseen oireyhtymään , joka on riskitekijöitä, jotka edistävät sydän- ja verisuonitautien ja tyypin 2 diabeteksen kehittymistä. Tutkimukset ovat osoittaneet, että erityisesti vatsan lihavuus ja insuliiniresistenssi vaikuttavat merkittävästi NAFLD: n kehittymiseen. Samanaikaisiin maksasairauksiin, kuten hepatiitti C: hen ja sydän- ja verisuonitauteihin, kuten ateroskleroosiin, liittyy myös lisääntynyt NAFLD -riski. Jotkut lapset diagnosoitiin jo kahden vuoden ikäisinä, ja diagnoosin keski -ikä oli 11–13 vuotta. Keski-ikä on yleensä yli 10 vuotta, koska lapset voivat myös ilmoittaa epäspesifisistä oireista ja siksi niitä on vaikea diagnosoida NAFLD: lle.
Pojilla todetaan todennäköisemmin NAFLD kuin tytöillä. Ylipaino tai jopa painonnousu lapsuudessa ja murrosiässä liittyy NAFLD-riskin lisääntymiseen myöhemmässä elämässä, ja aikuisten NAFLD-ennustettiin 31 vuoden seurantakokeessa lapsuuden riskitekijöiden mukaan lukien BMI, plasman insuliinitasot, miehet sukupuoli, geneettinen tausta (PNPLA3- ja TM6SF2 -muunnelmat) ja alhainen syntymäpaino, nouseva riskitekijä aikuisuuden NAFLD: lle. Eräässä tutkimuksessa yksinkertaista steatoosia esiintyi jopa 45%: lla lapsista, joilla oli kliininen epäily NAFLD: stä. Yksinkertaista steatoosia sairastavilla lapsilla on huonompi ennuste kuin aikuisilla, ja huomattavasti enemmän heistä etenee NAFLD: stä NASH: iin verrattuna aikuisiin. Itse asiassa 17-25%: lla NAFLD-lapsista kehittyy NASH yleensä ja jopa 83%: lla lapsilla, joilla on vaikea liikalihavuus (verrattuna 29%: iin aikuisilla), mikä viittaa edelleen siihen, että maksan fibroosi näyttää olevan aggressiivisempi kliininen kulku lapsilla verrattuna aikuisille.
NAFLD: n varhainen diagnosointi lapsilla voi auttaa estämään maksasairauden kehittymisen aikuisikään. Tämä on haastavaa, koska useimmat lapset, joilla on NAFLD, ovat oireettomia, ja vain 42–59% osoittaa vatsakipua. Muita oireita saattaa esiintyä, kuten oikean yläkvadrantin kipu tai acanthosis nigricans , joista jälkimmäistä esiintyy usein NASH -lapsilla. Suurentunut maksa esiintyy 30–40%: lla NAFLD -lapsista.
AASLD suosittelee diagnostista maksabiopsiaa lapsille, kun diagnoosi on epäselvä tai ennen mahdollisesti hepatotoksisen lääketieteellisen hoidon aloittamista. EASL ehdottaa fibroositestien, kuten elastografian , akustisen säteilyvoiman impulssikuvantamisen ja seerumin biomarkkereiden käyttöä biopsioiden määrän vähentämiseksi. Jatkossa NICE -ohjeet suosittelevat, että terveydenhuollon tarjoajat tarjoavat lapsille säännöllistä NAFLD -seulontaa pitkälle edenneen maksafibroosin suhteen joka toinen vuosi käyttämällä tehostettua maksafibroosin (ELF) verikoetta. Useat tutkimukset viittaavat myös magneettiresonanssielastografiaan vaihtoehtona vähemmän luotettavalle ultraäänitutkimukselle.
Intensiiviset elämäntapamuutokset, mukaan lukien liikunta ja ruokavalion muutokset, ovat AASLD: n ja EASL: n mukaan ensimmäinen hoitolinja, koska ne parantavat maksan histologiaa ja aminotransferaasitasoja. Farmakologisen hoidon kannalta AASLD ja EASL eivät suosittele metformiinia, mutta E -vitamiini voi parantaa joidenkin lasten maksan terveyttä. NICE suosittelee E -vitamiinin käyttöä lapsille, joilla on pitkälle edennyt maksafibroosi riippumatta siitä, onko heillä diabetes tai ei. Ainoa hoito, jonka on osoitettu olevan tehokas lapsuuden NAFLD: ssä, on laihtuminen.
Jotkut todisteet osoittavat, että äidin aliravitsemus tai aliravitsemus lisää lapsen alttiutta NASH: lle ja nopeuttaa sen etenemistä.
Tutkimus
Diagnoosi ja biomarkkerit
Koska maksan biopsiaan perustuva NAFLD -diagnoosi on invasiivinen ja vaikeuttaa epidemiologian arviointia, on tärkeä tutkimusprioriteetti löytää tarkkoja, edullisia ja ei -invasiivisia menetelmiä NAFLD -taudin ja sen etenemisen diagnosoimiseksi ja seurantaan. Haku näillä biomarkkereita ja NAFLD, NAFL ja NASH liittyy lipidomics , lääketieteellinen kuvantaminen , proteomiikka , verikokeita, ja pisteytysjärjestelmät.
Katsauksen mukaan protonitiheysrasvafraktion estimaattia magneettikuvauksella (MRI-PDFF) voidaan pitää tarkimpana ja tasaisimpana kullan standarditestinä maksan steatoosin kvantifioimiseksi. He suosittelevat ultraäänipohjaista ohimenevää elastografiaa, jotta diagnosoidaan tarkasti sekä fibroosi että kirroosi rutiininomaisessa kliinisessä ympäristössä. ja plasman sytokeratiini 18 (CK18) -fragmenttitasot ovat kohtalaisen tarkka steatohepatiitin biomarkkeri. Kuitenkin ohimenevä elastografia voi epäonnistua ihmisillä, joilla on maksan esiportaalihypertensio.
Lääkkeiden kehittäminen
Lääkkeiden kehittäminen NASH: lle on erittäin aktiivista ja etenee nopeasti. Uusia lääkkeitä suunnitellaan kohdistumaan erilaisiin maksan sisäisiin alueisiin, lipidien ja glukoosin homeostaasin säätelystä hapettumisstressiin ja mitokondrioiden kohteisiin hepatosyyteissä, tulehdussignaaleihin hepatosyyteissä ja solunsisäisiin kohteisiin, jotka liittyvät maksan tähtisolujen aktivoitumiseen ja fibrogeneesiin. Vuodesta 2021 alkaen on käynnissä keskeisiä tutkimuksia obetikolihapolle ( FXR- agonisti), Resmetiromille ( THRβ- agonisti), belaptiinille ( galektiini-3- estäjä) ja Aramcholille ( SCD1- estäjä).
Katso myös
- Hanhenmaksa , siipikarjassa aiheutettu rasvahappo, jonka patofysiologia on homologinen NAFLD: n kanssa ihmisillä
Viitteet
Ulkoiset linkit
- NIH- sivu alkoholittomasta steatohepatiitista
- Mayo Clinic -sivu NAFLD: ssä
| Luokitus | |
|---|---|
| Ulkoiset resurssit |